后起之秀MET靶向疗法用于初治MET 14跳变患者 ORR达68%!
MET驱动基因被认为是继EGFR/ALK之后肺癌精准治疗领域又一重要的分子治疗靶点。近年来有多项研究聚焦MET驱动基因的靶向治疗。MET基因异常包括突变、扩增、重排和过表达,“众里寻他千百度”,不断有研究显示,MET外显子14跳跃突变和MET扩增才是有效的生物标志物,2020 ASCO大会上,GEOMETRY mono-1研究发表了2篇摘要分别公布了队列1a、队列5a和队列6在MET外显子14跳跃突变和MET扩增患者中的疗效,近日,研究结果正式结果发表于《NEJM》杂志。
MET信号通路的激活与多个瘤种相关,MET外显子14跳跃突变见于3%~4%的非小细胞肺癌(NSCLC)患者中,通常不与其他驱动基因突变同时存在,且与预后差相关,MET扩增见于1%~6%的NSCLC患者中。
既往研究显示,在NSCLC患者中,经筛选的MET过表达患者并没有明显的获益,而MET外显子14跳跃突变和高水平MET扩增目前已成为潜在的预测生物标志物。
卡马替尼(INC280),是一种高选择性MET受体酪氨酸激酶抑制剂,初步临床数据显示,卡马替尼单药在MET异常突变NSCLC患者中显示出较低毒性,且疗效良好。
01研究方法
GEOMETRY mono-1是一项多队列II期研究,旨在评估卡马替尼在MET异常晚期NSCLC患者中的疗效和安全性。研究纳入18岁及以上IIIB或IV期任意组织学类型NSCLC患者,患者无EGFR或ALK突变,至少一个可测量病灶。根据既往治疗情况和MET状态将患者分组。入组患者接受卡马替尼(400mg,每日2次)治疗。主要终点为由孤立评审委员会评估(IRC)的总缓解率(ORR),次要终点为IRC评估的缓解持续时间(DOR)。
02研究结果
共364例晚期NSCLC患者纳入研究(图1),队列1~5中共纳入97例MET外显子14跳跃突变患者,210例MET扩增患者。队列1~4患者曾接受过一线或二线治疗,队列5a和5b为初治患者。
MET外显子14跳跃突变对比MET扩增更常见于女性、从不吸烟患者。
扩增队列6共纳入34例患者,3例为MET扩增(基因拷贝数≥10),31例为至少接受过一线治疗的MET外显子14跳跃突变患者。
数据截止时,共23例MET外显子14跳跃突变初治患者纳入队列7,目前无研究数据。
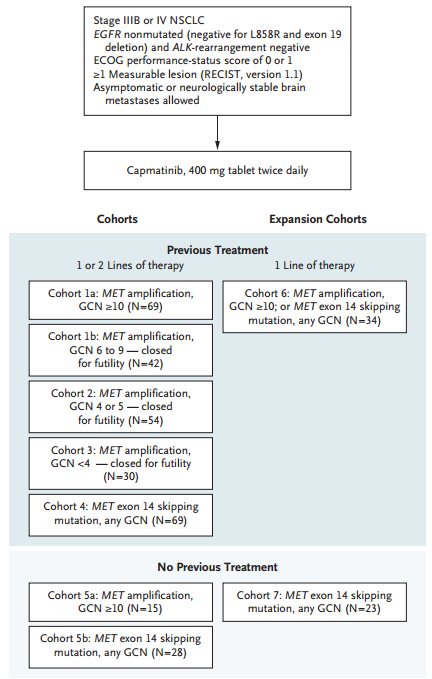
图1 研究设计图
➤疗效
MET外显子14跳跃突变晚期NSCLC患者
在经治晚期患者中,由IRC评估的ORR为41%(共69例),初治患者的ORR为68%(共28例)(表1,图2A),经治和初治患者的中位DOR分别为9.7个月和12.6个月(表1)。
表1 疗效分析
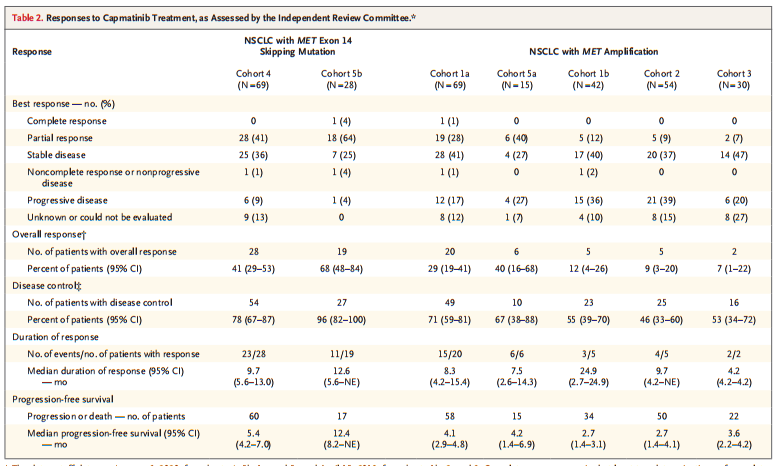
患者对卡马替尼治疗的应答很迅速,大多数患者(82%经治患者,68%初治患者)在开始治疗后的第一次肿瘤评估时就产生了肿瘤缓解。
经治和初治患者中,由IRC评估的中位PFS分别为5.4个月和12.4个月,研究者评估的结果与IRC评估的结果相当。
在14例基线有脑转移的MET外显子14跳跃突变NSCLC患者中,13例患者可评估,10例为经治患者,3例为初治患者,其中12例患者被评估为颅内疾病控制,有7例患者产生了颅内缓解(3例曾接受过脑部放射治疗),其中4例完全缓解。在第一次评估时即观察到颅内缓解。
扩增队列6包括31例曾接受过一线治疗的MET外显子14跳跃突变患者,结果与队列4保持一致,队列6患者的ORR为48%。
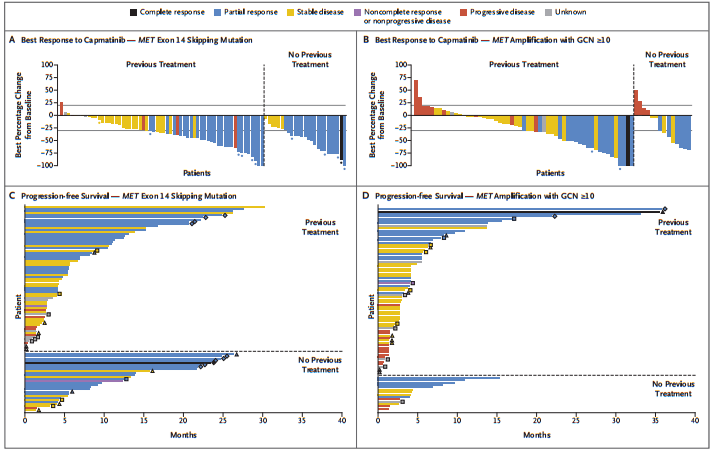
图2 肿瘤缓解情况
MET扩增晚期NSCLC患者
基因拷贝数6~9、4~5、<4患者的ORR分别为12%、9%和7%。因几乎无疗效,中期分析时终止了研究。
卡马替尼在基因拷贝数在≥10患者中显示出抗肿瘤活性,但ORR低于预设阈值,经治和初治患者中,由IRC评估的ORR分别为29%(共69例)和40%(共15例)(表1,图2B)。
20例和6例经治和初治患者的中位DOR分别为8.3个月和7.5个月(图2D),中位PFS分别为4.1个月和4.2个月。
➤安全性
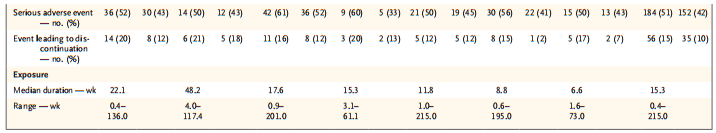
在所有队列共364例患者中,最常见的不良事件为外周水肿、恶心和呕吐,67%患者发生了3级或4级不良事件(表2)。
表2 安全性分析
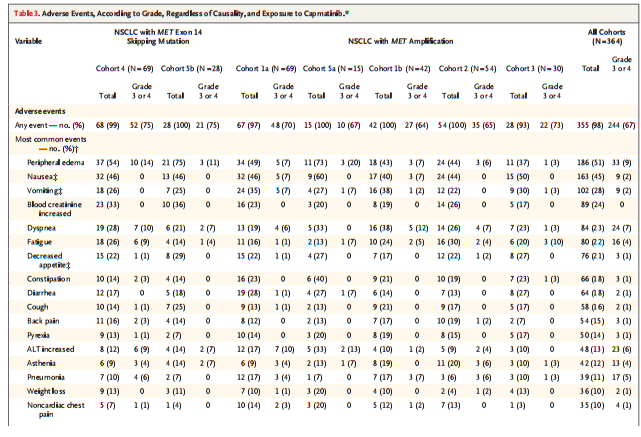
03研究结论
卡马替尼在MET外显子14跳跃突变晚期NSCLC患者中显示了有临床意义的抗肿瘤活性,表现出明显的抗肿瘤活性,尤其是在初治患者中,IRC评估的ORR达到68%,疾病控制率为96%。在MET扩增患者中,高基因拷贝数对比低基因拷贝数患者的疗效更优。
参考文献:
Wolf J, Seto T, Han JY, et al. Capmatinib in MET Exon 14-Mutated or MET-Amplified Non-Small-Cell Lung Cancer. N Engl J Med. 2020;383(10):944-957. doi:10.1056/NEJMoa2002787