CheckMate153研究:免疫治疗待到何时?
针对免疫治疗最佳治疗周期仍未有定论,既往III期临床研究涵盖了2年到疾病进展为止不等的免疫治疗时长,目前并未有足够证据显示免疫治疗应用越长预后越好,此外还需考虑到高昂免疫治疗费用及持续治疗带来毒副反应。PACIFIC研究显示1年免疫治疗维持可显著提高不可切除局部晚期NSCLC生存预后,另一项来自KEYNOTE-010研究显示完成2年免疫治疗晚期NSCLC患者,在随访截止时间内仅有32%患者出现复发,其中56%的患者再次接受免疫治疗同样取得较好临床疗效。近期,《临床肿瘤杂志》(Journal of Clinical Oncology)发表了全球首个针对免疫治疗周期的随机对照IIIb/IV期研究,为这一亟待解决临床问题提供了高级别循证依据。
研究背景
免疫治疗最佳周期时长仍是悬而未决的临床问题,一方面延长免疫治疗能否改善预后并不明确,另一方面早期停药可能会导致疾病短期复发并错失挽救机会。2018年发表的CheckMate017/CheckMate057研究显示,纳武利尤治疗2年和接受纳武利尤治疗直到疾病进展的两组相比较在3年总生存率上无显著差异(18% vs. 17%),KEYNOTE-001研究同样显示,在帕博利珠单抗治疗2年和应用帕博利珠单抗治疗直到疾病进展的两组之间无3年生存率显著差异(23% vs. 21%),但上述结果均来自亚组探索性分析,无法明确定论免疫治疗的最佳周期。CheckMate153研究是首个探索免疫治疗周期的随机对照IIIb/IV期研究,同时纳入以社区为主患者群体,更加真实反映临床治疗实际情况。
研究方法
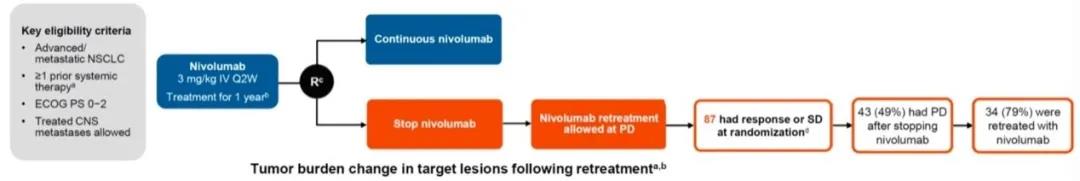
CheckMate153是一项IIIb/IV期多中心随机对照研究,入组患者既往接受过至少一线系统性治疗的晚期或转移性NSCLC(不考虑PD-L1表达水平),局部晚期患者接受辅助、新辅助化疗或放化疗后6个月内出现进展的同样可入组该研究。初期的试验设计是入组患者在1年纳武利尤单抗处理后随机分为两组,继续接受为期一年的纳武利尤单抗治疗,或是持续接受纳武利尤治疗直到出现疾病进展或其他问题(药物副反应或患者主观不愿再接受治疗)。2014年,在首例1年纳武利尤单抗预先处理完成之前,研究人员对试验方案作出了调整。在1年纳武利尤单抗处理完成后,患者分别继续纳武利尤单抗治疗,或停用纳武利尤直至出现疾病进展再次使用纳武利尤单抗(图1)。该研究主要研究终点为3度及以上毒副反应发生率,次要研究终点为严重不良反应事件发生率和临床转归,探索性研究终点包括安全性,总生存(OS)及患者报告临床结局(PROs)。在2014年的试验设计调整之后,研究增加了对随机分组后终点的探索。从随机分配的时间点开始,在那些完成1年纳武利尤单抗处理后继续接受治疗的患者中,对安全性和耐受性、无进展生存(PFS)、OS和客观反应率进行了评估。
研究结果
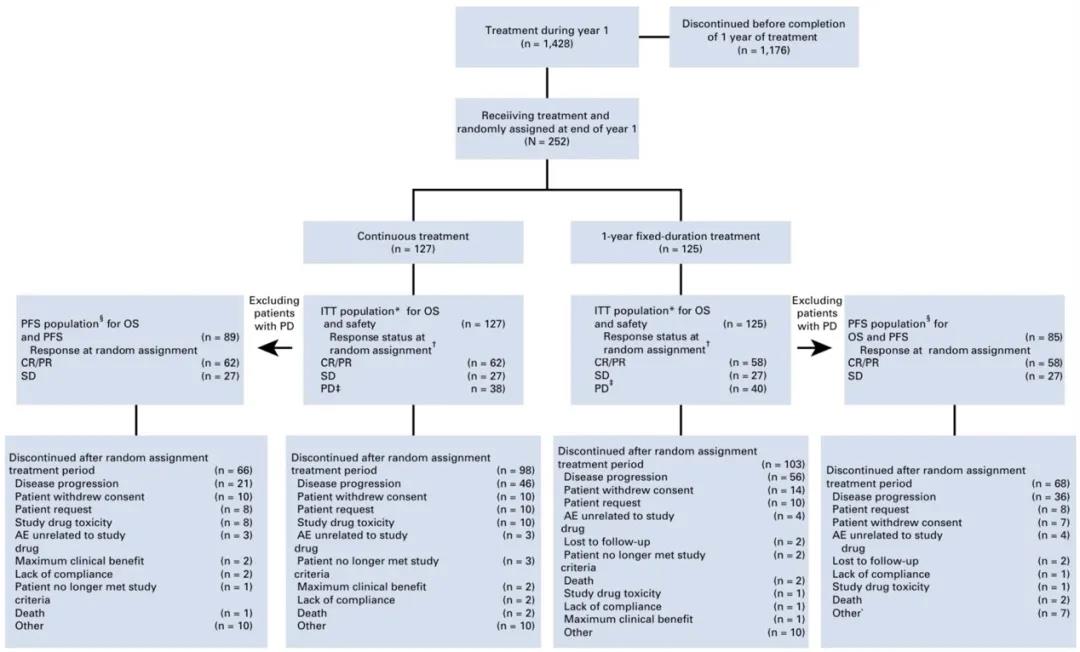
研究共筛选1428例患者,其中252例患者接受1年纳武利尤单抗治疗后随机分配至两组,127例继续接受纳武利尤单抗治疗(继续治疗组),125例停用纳武利尤单抗直至出现疾病进展接受纳武利尤单抗再处理(1年治疗组)。其中有78例患者在随机分配之前的纳武利尤单抗治疗期间存在疾病进展(持续治疗组38例,1年治疗组40例,研究者评估有临床获益),除此之外其他的未进展患者均被纳入PFS统计。两组除鳞癌在继续治疗组占比较低外,其余基线特征均无明显差异,所有患者均随访超过1年以上。
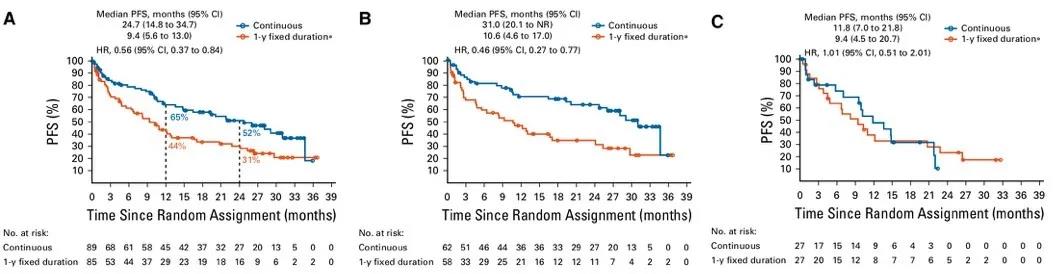
在纳武利尤单抗治疗无进展患者中,继续治疗组中位PFS显著优于1年治疗组(24.7月 vs. 9.4月),两组1年和2年PFS率分别为64.6% vs. 44.0%和51.9% vs. 30.7%。与1年治疗组相比,完全缓解(CR)和部分缓解(PR)患者继续接受纳武利尤单抗治疗获得了更长的中位PFS(31月 vs. 10.6月),而对于疾病稳定(SD)的患者,两组中位PFS无显著统计差异(11.8月 vs. 9.4月)(图2)。
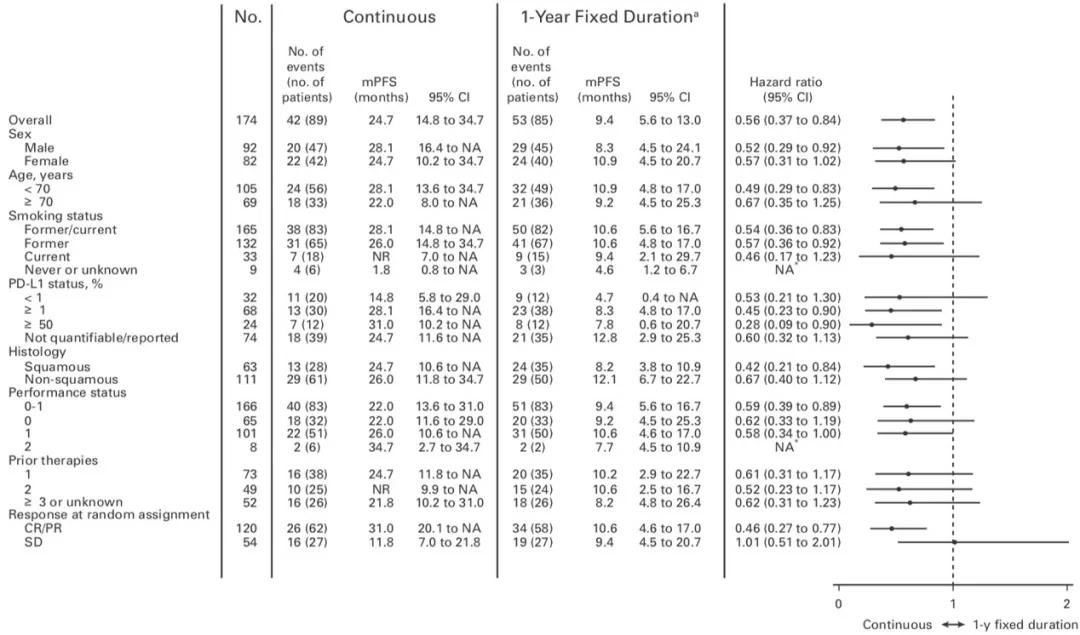
亚组分析显示大部分临床特征在继续治疗组中均有PFS获益趋势(图3)。
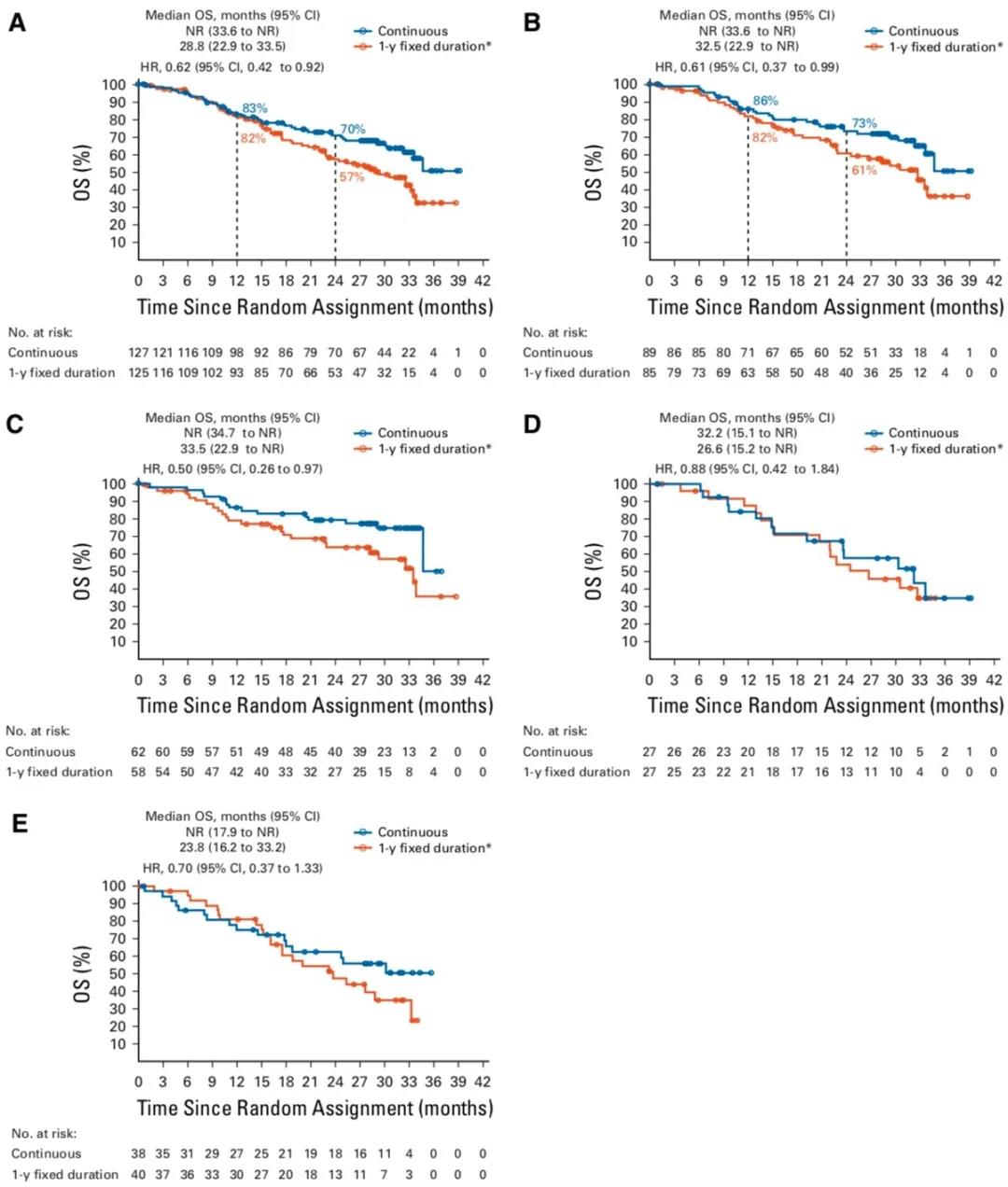
在所有入组患者中,继续治疗组中位OS显著优于1年治疗组(未达到 vs. 28.8月),1年生存率两组相近,而2年总生存率上,继续治疗组显示出更大获益(70.4% vs. 56.8%)。在无进展患者群体中,继续治疗组同样显示出中位OS和2年OS率获益,尤其是随机分组时评估PR或CR的患者获益最大,对于SD或PD患者,尽管中位OS没有显著差异,但从远期生存率上均看到继续治疗组预后改善的趋势(图4)。
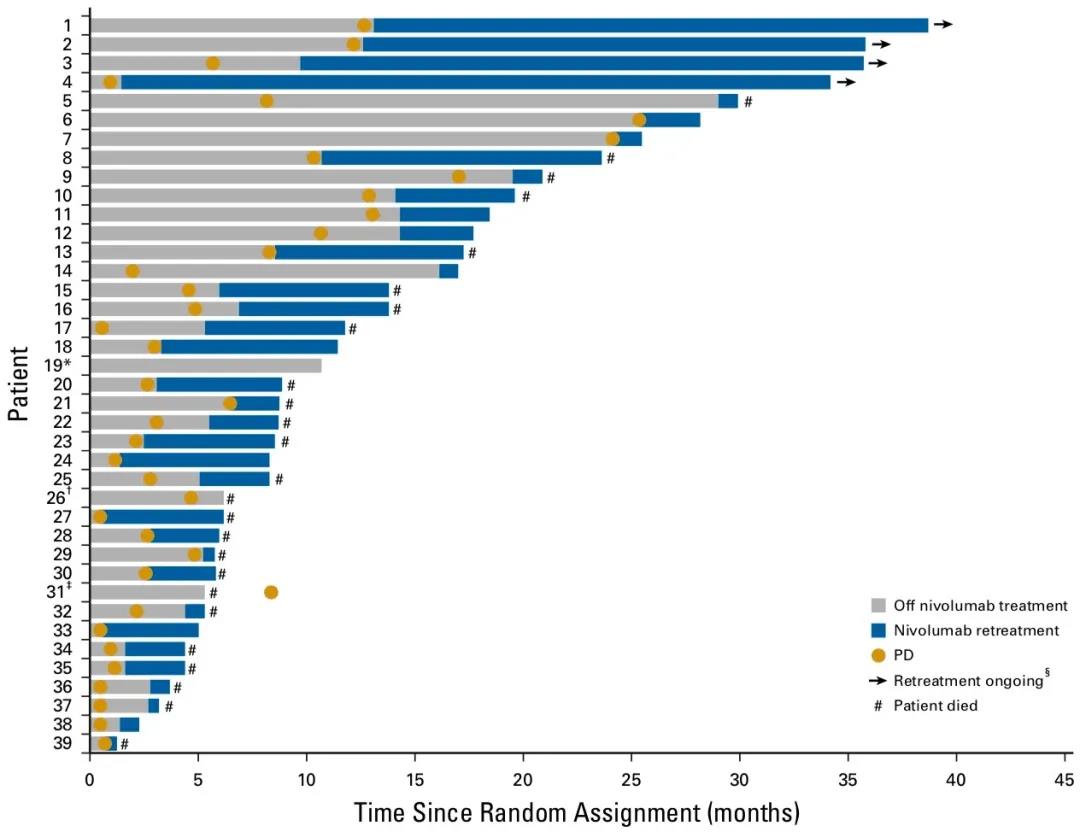
在随机分组后,1年治疗组有47例(55.3%)起初无进展的患者出现PD,其中39例(83.0%)再次接受纳武利尤单抗治疗。截至随访时间为止,4例(10.2%)患者仍在继续纳武利尤单抗治疗,14例(35.9%)患者仍然存活(图5)。
随机分组后的安全性评估显示,继续治疗组较1年治疗组在治疗相关不良反应发生率(48.0% vs. 26.4%)以及不良事件导致停药发生率(9.4% vs. 1.6%)更高,考虑和治疗时长相关。3~4级不良事件发生率,继续治疗组同样高于1年治疗组(9.4% vs. 3.2%),无其它新发不良事件报道。
讨论
CheckMate153作为首个在随机对照研究中探索免疫治疗周期的研究,显示了免疫维持治疗相比1年治疗周期更佳预后改善,但该研究也存在一定局限性,包括随机分组时未进行基线特征的采集以及未按照应答情况随机分组,同时受限于研究预设计终点,没有足够统计效能评估疗效情况。但不可否认,CheckMate153研究为免疫治疗周期提供了极具参考价值的信息,当然仍有诸多问题尚待解决,包括2年免疫治疗周期是否合适,不同联合模式或用药间隔(Q3W/Q4W)是否影响最佳治疗周期等等。
参考文献
WATERHOUSE D M, GARON E B, CHANDLER J, et al. Continuous Versus 1-Year Fixed-Duration Nivolumab in Previously Treated Advanced Non–Small-Cell Lung Cancer: CheckMate 153 [J]. 0(0): JCO.20.00131.