膀胱癌患者长生希望!中国自主研发新药ICP-192重磅登场!
关键词:膀胱癌;自主研发;抗癌新药;ICP192
膀胱癌是最常见的泌尿系统恶性肿瘤,在全球最常见的恶性肿瘤中位列第九,其中约90%~95%属于尿路上皮癌。根据统计,2018年世界范围内膀胱癌新发病例数量约55万,其中男性患者数量约为女性的四倍。
目前,针对膀胱癌,临床已有5款免疫检查点抑制剂药物及1款FGFR(成纤维细胞生长因子受体)靶点药物获批,但在国内均未有对应的适应症获批。患者治疗仍存在一定的困难,花费昂贵,疗效需要进一步的提升。
幸而,目前国内药物研发进展迅速,我国自主研发的膀胱癌新药投入试验。针对FGFR靶点的重磅新药ICP-192面世,开始免费招收患者了!
二代FGFR抑制剂ICP-192重磅登场!
ICP-192为北京诺诚健华医药科技有限公司研发的第二代泛FGFR抑制剂,对FGFR家族四个激酶均有很强的抑制效果。
与目前已获批应用于临床的同类FGFR靶向药物厄达替尼相比,ICP-192具有四大优势。
特异性强
ICP-192靶点特异性强,非靶向的毒副作用更低。通过对其进行468种激酶的高通量筛选检测, ICP-192 在1 uM浓度下仅对FGFR 1~4有显著的抑制作用,而对其他激酶并无明显抑制作用,选择性优于同类在研品种。
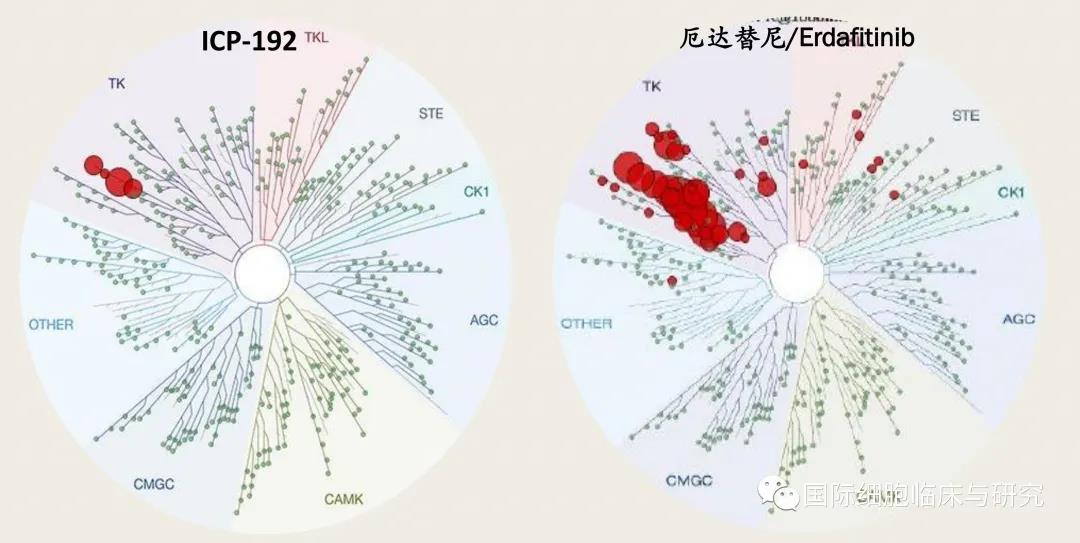
从右图中可以看出,除真正的目标靶点FGFR 1~4以外,厄达替尼还可能对许多其他位点产生抑制效果。这将导致治疗过程中对正常细胞、正常生理功能的抑制,进而导致更多不良反应的发生。
而从左图中可以看到,ICP-192的选择性更好,不会对靶点以外的其他受体造成抑制,有望获得更好的疗效与更轻微的不良反应。
二代药物,药效更持久
ICP-192为最新第二代泛FGFR抑制剂,药效更持久,ICP-192是根据靶点蛋白结构特点设计的具有完全自主知识产权(发明专利)的FGFR抑制剂。主要特点为与FGFR激酶不可逆共价结合且具有很高的特异性。这种结合方式不会因为药物代谢后浓度降低而解离,因此抑制效果更好,更不容易产生耐药,药效更持久;(参照同类二代FGFR抑制剂TAS120药效持续时间>1年),而一代FGFR抑制剂为可逆结合,药物有效持续中位时间较短, 为4.8~7.5个月不等。
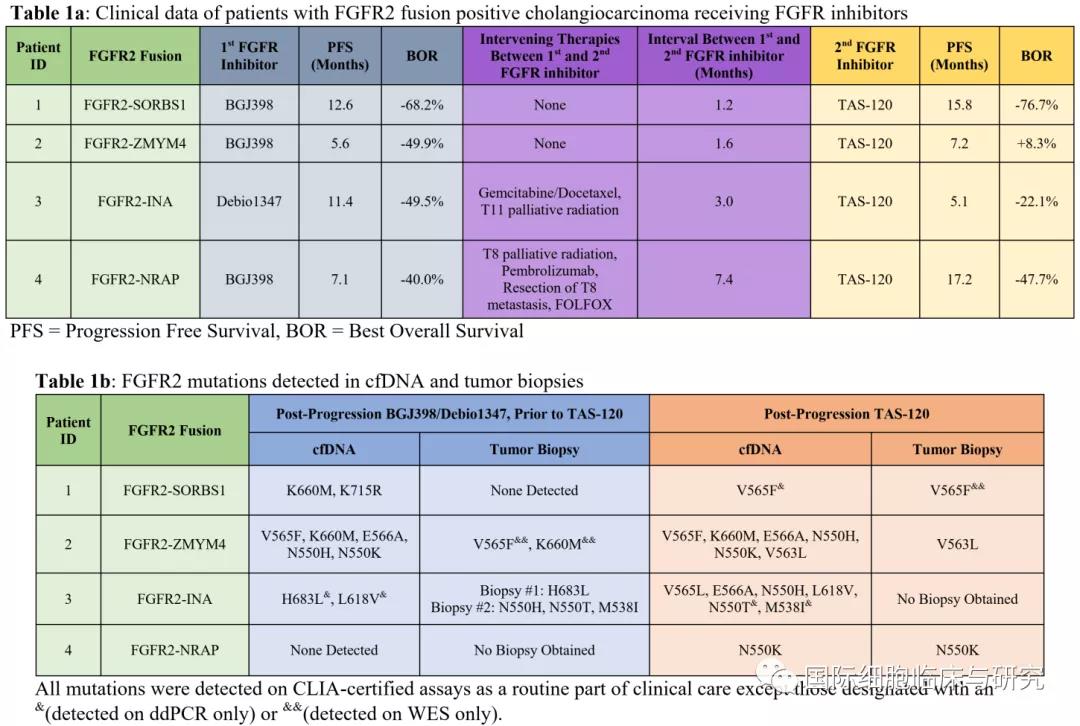
对耐药突变仍然有效
ICP-192有很强的抗肿瘤作用,且对耐药突变有效。一代GFR抑制剂容易产生耐药突变, ICP-192为最新第二代泛FGFR抑制剂,对某些特定耐药突变FGFR激酶仍具有较强的结合作用。
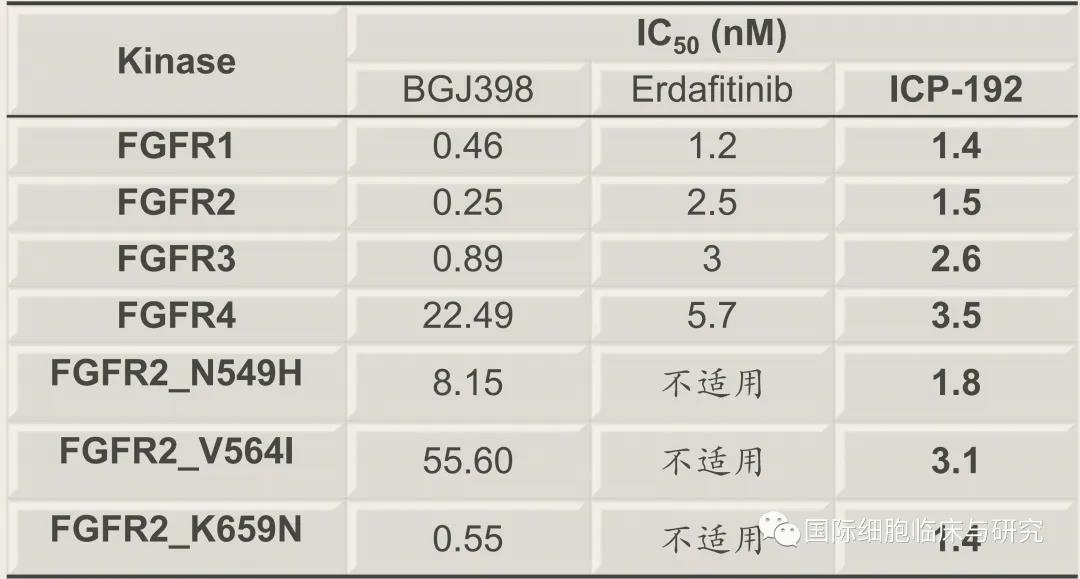
在各类肿瘤模型中,ICP-192都展现出了良好的抑制肿瘤生长效果。
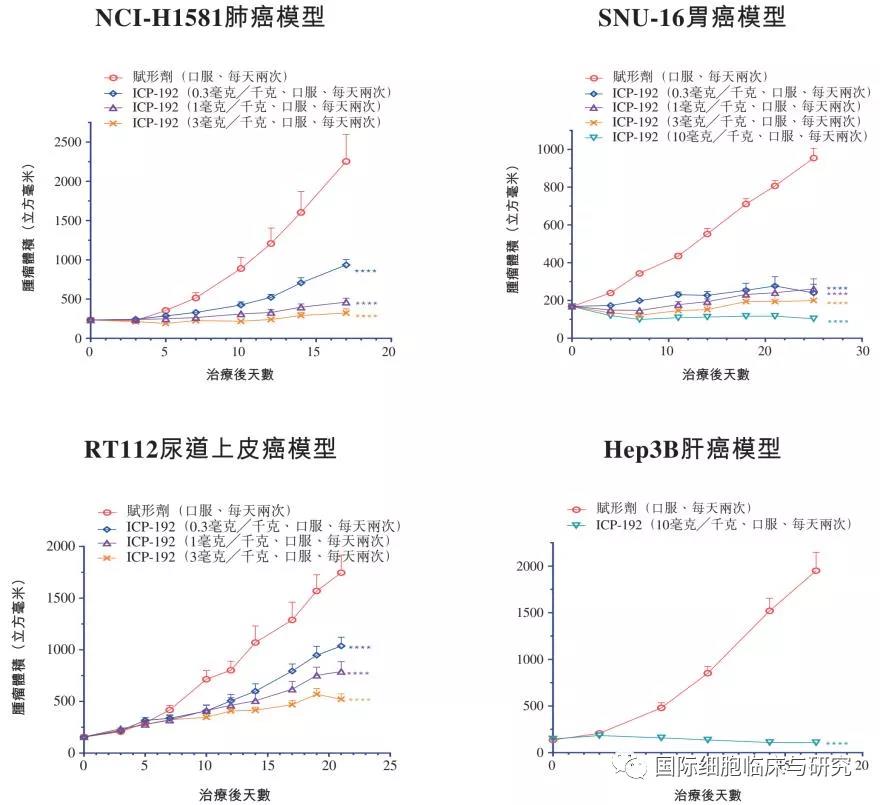
安全性更高、有效性更好
与一代FGFR抑制剂药物相比,二代药物ICP-192安全性更高、有效性更好。在已经完成的ICP-192 I期安全性临床试验中数据显示:剂量为2~12 mg时ICP-192安全状况良好,大多数不良反应为1~2级,未报告治疗相关的剂量限制性毒性(DLT);而试验证实,8 mg剂量时已达到有效药物浓度(数据截止到2019年12月)。
认识膀胱癌最重要的靶点——FGFR
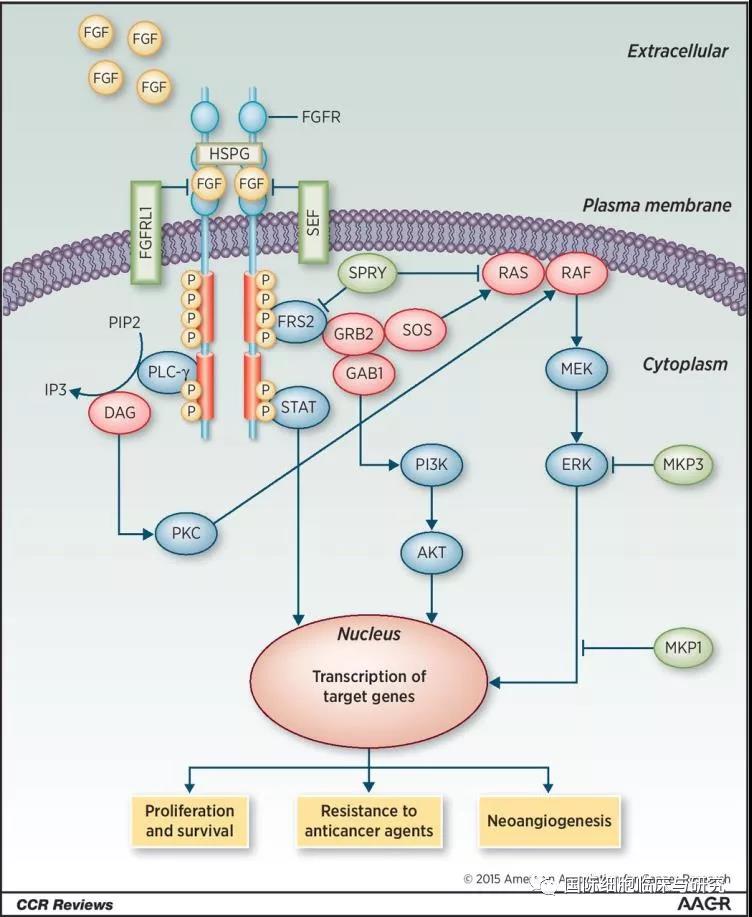
FGFR,成纤维细胞生长因子受体,顾名思义,是一类与成纤维细胞生长因子结合的靶点。FGFR受体与FGF配体结合,激活FGFR酪氨酸激酶活性,可促进细胞增殖、存活以及抗凋亡等下游信号通路。FGFR基因变异(基因突变、基因融合、基因扩增等)可导致其激酶异常激活,从而不再依赖于与其FGF配体的结合,促进肿瘤细胞的增殖和转移。
作为原癌基因,FGFR异常可能导致多种癌症,以肝内胆管癌和膀胱癌为主。肝内胆管癌患者的变异频率为10%~15%;膀胱癌患者变异频率根据肿瘤类型的不同为10%~80%不等。
多种FGFR抑制剂的临床试验数据表明,很多FGFR变异类型的患者均可在FGFR抑制剂治疗中获益:比如FGFR基因突变、基因融合、基因扩增、基因异常表达等变异情况。目前多项临床试验已经证明FGFR抑制剂可以用于治疗肝内胆管癌和膀胱癌,客观缓解率可达20%~50%,而传统的化疗方案仅为10%左右。这两个适应症均已经被美国FDA批准,国内暂无药物获批。
根据指南推荐,目前临床上治疗膀胱尿路上皮癌的常规治疗方案为:

一线化疗方案疗效较好,可以达到50%左右,但几乎所有患者都会在治疗后复发或进展,中位生存时间仅5~7个月,疗效并不理想。二线化疗及二线免疫治疗疗效不理想,缓解率仅10%~25%,且整体来说,花费高昂。
相比之下,FGFR的疗效更值得期待,目前有多种药物在研缓解率大大高于二线治疗方案,达到25%~40%,对于肿瘤体积缩小有比较明确的效果。通常来说,FGFR抑制剂药物的治疗花费为12万/月,对于国内患者来说仍显昂贵。
但幸运的是,国内自主研发的FGFR抑制剂药物ICP-192开展临床试验,国内患者免费用药的机会来了!
免费用药机会来了!ICP-192治疗膀胱尿路上皮癌临床试验重磅开启!
目前,在全国多家医院均开启了针对ICP-192治疗FGFR基因变异的肝内胆管癌以及尿路上皮癌等临床项目。患者可以联系全球肿瘤医生网,提交病例报告,由专业医疗顾问为您进行评估。
登记号:CTR20200688
适应症:膀胱尿路上皮癌
药物名称:ICP-192片
试验名称:一项评价ICP-192治疗特定FGFR基因异常的不可切除或转移性膀胱尿路上皮癌的多中心、单臂、开放性II期临床试验
试验分类:安全性和有效性
试验分期:Ⅱ期
纳入标准:
1、年龄≥18周岁,性别不限;
2、ECOG体力评分为0~1分;
3、预计生存期3个月以上;
4、经组织病理学证实的不可切除或转移性膀胱尿路上皮癌,可以接受少量成分(<50%)伴腺样分化或鳞状分化,或转化为更具侵袭性的亚型,如肉瘤样或微乳头尿路上皮癌;
5、既往一线化疗失败的不可切除或转移性膀胱尿路上皮癌或化疗不耐受的受试者;
即患者应已经接受过至少一线化疗,可为接受过多线治疗的患者。
6、根据RECIST1.1标准,筛选期至少有一个可测量病灶作为靶病灶;
即患者应具备至少一个可测量的实体病灶。
7、经中心试验室检测,必须至少具有以下一种基因异常:FGFR3基因突变:R248C、S249C、G370C、Y373C;基因易位/融合:FGFR2-BICC1、FGFR2-CASP7、FGFR3-TACC3、FGFR3-BAIAP2L1;
8、患者器官功能水平标准可咨询无癌家园位点。
排除标准:
1、既往接受过选择性FGFR抑制剂【例如:Erdafitinib、ARQ-087(Derazantinib)、AZD4547、BAY 1163877(Rogaratinib)、BGJ398(Infigratinib)、Debio 1347、HMPL-453、EOC317等】或FGFR抗体治疗;
2、已知有影像学证据的中枢神经系统转移;