ROAR研究:达拉非尼+曲美替尼治疗BRAF突变胆道癌
胆道癌是一种恶性侵袭性疾病,临床预后较差,大多数患者确诊时已处晚期,5年生存率仅18%。晚期胆道癌治疗主要是化疗(吉西他滨+顺铂),但中位PFS仅8个月,中位OS为12个月。近日,《柳叶刀·肿瘤》(The Lancet Oncology)发布ROAR篮子试验的其中一项研究,结果令人鼓舞,再次表明基于基因状态的精准治疗是胆道癌未来发展方向,有望突破化疗局限性。

研究背景
胆道癌包括肝内胆管癌(胆管癌)、肝外胆管癌和胆囊癌,三者复发率、预后和基因组情况因肿瘤位置不同而异,已鉴定的基因突变有IDH1、FGFR2、BRAF和HER2,这为该群体的靶向治疗提供可能性。BRAF突变在胆道癌占5%~7%,尤以胆管癌常见。与无BRAF V600E突变者相比,BRAF V600E突变胆管癌者在切除时具有更高的肿瘤分期、淋巴结转移,且长期OS较差。吉西他滨+顺铂治疗晚期胆道癌,进展后5-FU+顺铂治疗的回顾性研究结果令人失望,应答率较低。BRAF抑制剂(BRAFi)单药试验显示出鼓舞的抗癌活性,然而已报道的毒性(包括继发皮肤癌)和持续性低应答提示该疗法需改进。帕博利珠单抗已被FDA批准用于高微卫星不稳定(MSI-H)、错配修复缺陷胆道癌,然而免疫治疗获益人群仅占胆道癌的小部分。
既往研究表明BRAFi+MEK抑制剂(MEKi)联合与BRAFi单药比较,前者降低黑色素瘤病人皮肤不良反应,延长OS和PFS。达拉非尼(BRAFi)+曲美替尼(MEKi)组合在某些BRAF V600E突变癌种中显效,已被批准用于黑色素瘤、非小细胞肺癌和甲状腺癌的治疗。个案报道提示该联合用药耐受性好,且效果优于单药。ROAR篮子试验是一项跨癌种研究,主要评估达拉非尼+曲美替尼联合治疗BRAF V600E突变的少见癌种,如未分化甲状腺癌、胆道癌、胃肠间质瘤、小肠腺癌、非精原细胞瘤型生殖细胞肿瘤、低级别神经胶质瘤、高级别神经胶质瘤和多发性骨髓瘤的安全性和有效性。本研究发布了胆道癌的研究结果。
研究方法
这是一项正在进行的2期、开放标签、单臂、多中心研究,属于ROAR篮子试验的一部分,该试验针对BRAF V600E突变的罕见肿瘤患者。胆道癌纳入标准是年龄≥18岁、BRAF V600E突变、不可切除、转移性、局部晚期或复发、美国东部肿瘤协作组(ECOG)评分0-2以及既往已接受过全身系统性治疗。所有入组患者口服达拉非尼150mg bid+曲美替尼2mg qd,直到疾病进展或治疗不耐受。主要终点是总体缓解率(ORR),该ORR是由RECIST 1.1在意向治疗可评估人群中确定的,人群包括所有可评估的入组患者,无论接受治疗如何(如已开始进展、开始接受新的抗癌药、撤回同意、死亡、病情稳定持续6周或更长时间,或基线评估后进行两次或多次新抗癌治疗)。这些结果是根据中期分析所得。
研究结果
在2014年3月12日至2018年7月18日之间,对626例胆道癌患者进行BRAF V600E突变预筛查。根据BRAF基因检测结果,鉴定出57例BRAF V600E突变的胆道癌患者,其中43例选为研究对象,包括意向性治疗人群,18例患者处于贝叶斯分析的主要队列,25例处于扩展队列。43例受试者中胆管癌占91%(39/43),肝门部胆管癌2%(1/43),胆囊癌2%(1/43),未知2%(1/43),缺失2%(1/43)。中位随访时间10个月,四分位数间距IQR(6-15)个月,截至2019年3月29,有7例(16%)仍继续接受治疗,36例终止(34例疾病进展,1例死于不良事件,1例要求终止)。
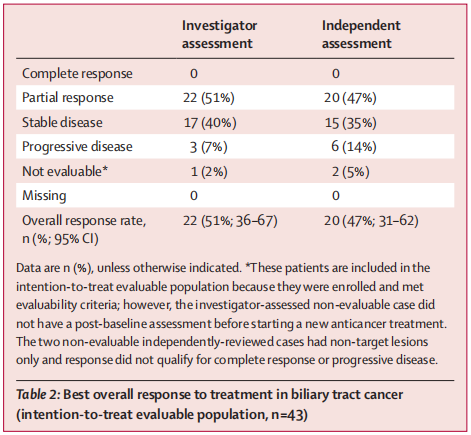
ORR:43例患者中22名(51%[95%CI: 36-67])达到研究者评估的ORR。43例患者中20名(47%[95%CI: 31–62])达到孤立审评委员会评估的ORR(表1)。
表1:胆道癌对治疗的最佳ORR(意向性治疗可评估人群,n = 43)
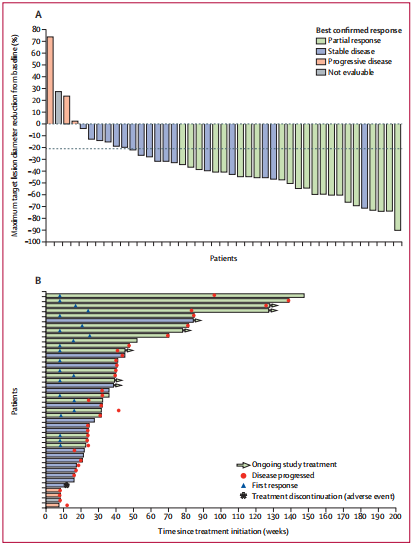
在22例接受研究者评估的总体应答者中,持续缓解的患者比例在6个月时为67%(95%CI:43-83),在12个月时为36%(95%CI:17-57),而24个月时为13%(95%CI:2-33)。经研究人员评估为总体应答的22例患者中,有13例(59%)持续应答超过6个月,7例超过12个月,2例在数据截止时仍持续应答。由研究人员评估的22例患者总体应答中位时间为9个月(95%CI: 6-14)(图1)。
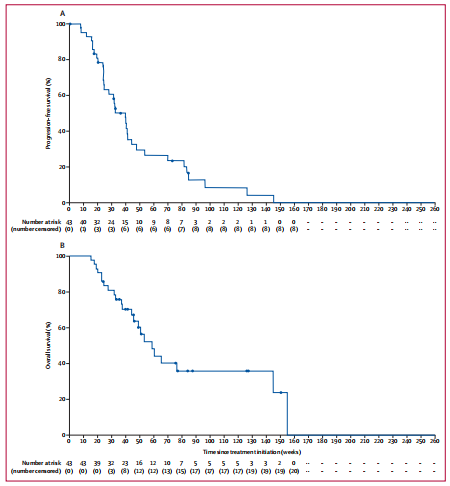
PFS和OS:研究人员评估的6个月PFS为63%(95%CI: 47-76),12个月为30%(95%CI: 16-45),而24个月为8%(95%CI: 2-22)。根据研究者评估,中位PFS为9个月(95%CI: 5-10;图2A)。6个月时OS为84%(95%CI: 69-92),12个月时OS为56%(95%CI: 38-71),24个月时OS为36%(95%CI: 19-53)。中位OS为14个月(95%CI: 10–33;图2B)。有35个无进展生存事件(29个进展和6例死亡)和23个总体生存事件。
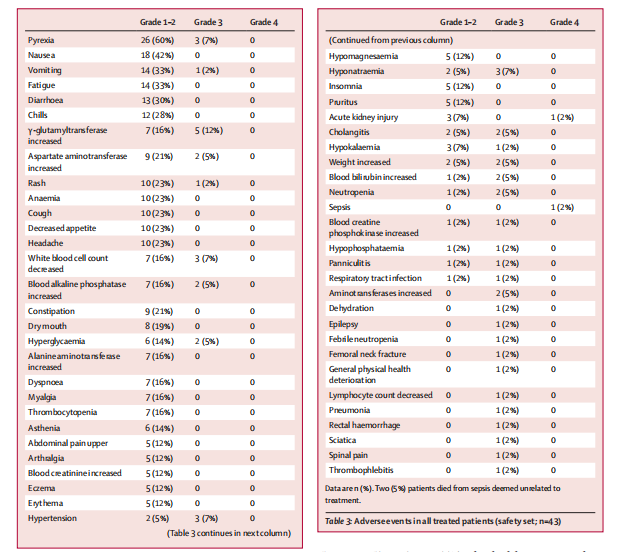
安全性:在5名(12%)患者中,最常见的全因3级或4级不良事件是γ-谷氨酰转移酶升高(表3)。15例(35%)因不良事件降低剂量,24例(56%)因不良事件导致剂量中断,而1例(2%)因败血症导致永久性停药。17(40%)例发生严重的不良事件;9例(21%)有与治疗相关的严重不良事件(最常见发热)。2名(5%)死于败血症,但被认为与研究治疗无关,无治疗相关的死亡。
表3:所有接受治疗的患者的不良事件(n = 43)
结 论
达拉非尼+曲美替尼联合治疗在BRAF V600E突变型胆道癌患者中显示出令人鼓舞的抗癌活性,且安全性可控。胆道癌患者应考虑常规检查BRAF V600E突变。
参考文献
Vivek Subbiah, Ulrik Lassen, Elena Élez, et al. Dabrafenib plus trametinib in patients with BRAFV600E-mutated biliary tract cancer(ROAR): a phase 2, open-label, single-arm, multicentre basket trial. THE LANCET Oncology , 2020. DOI:https://doi.org/10.1016/S1470-2045(20)30321-1