ORR高达70%!全新RET-TKI Pralsetinib获FDA批准用于RET融合阳性的转移性非小细胞肺癌患者
随着恶性肿瘤的治疗进入靶向时代,越来越多的肿瘤驱动基因变异被精准识别,越来越多的靶向药物获批上市。近日,一款自诞生之日就广受关注的药物——RET抑制剂Pralsetinib因其在前期临床试验中表现出来的惊艳数据,被FDA加速批准用于RET融合阳性的转移性非小细胞肺癌这一适应证。较高的客观反应率,超长的缓解持续时间,让Pralsetinib为RET融合阳性的晚期非小细胞肺癌患者带来了充满希望的新选择。

RET抑制剂新药获批,剑指RET融合阳性晚期NSCLC
2020年9月4日,美国食品和药物管理局(Food and Drug Administration,FDA)加速批准全球第二款RET抑制剂—— Pralsetinib用于RET融合阳性的转移性非小细胞肺癌(NSCLC)成人患者,并同时批准了美国生命科技公司(Life Technologies Corporation)基于二代测序法(NGS)的“Oncomine™Dx” 靶向检测体外诊断试剂框(ODxT)作为RET融合的推荐检测方案。
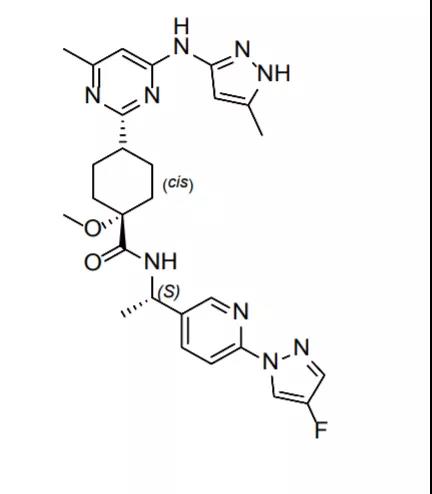
Pralsetinib(商品名Gavreto,研发代号BLU-667,化学式见图1 )是由美国蓝图医药公司(Blueprint Medicines)研发的口服强效小分子RET酪氨酸激酶抑制剂,能特异性地抑制多种类型的RET基因变异,包括RET融合突变。Pralsetinib对RET受体作用的高选择性和目前获批涵盖RET靶点的多激酶TKI相比有着质的飞跃,且不论对MET原发突变抑或RET继发(耐药性)突变均有效,药理研究显示Pralsetinib能有效抑制各种RET突变或者融合驱动的非小细胞肺癌及甲状腺癌细胞的生长。
ORR最高可达70%,铂类化疗经治患者可评估DoR最短15.2个月!
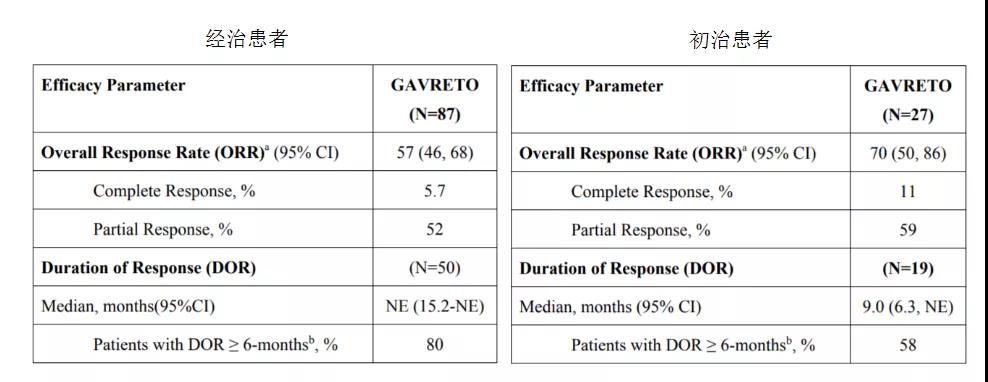
FDA批准Pralsetinib用于RET融合阳性非小细胞肺癌这一适应证基于一项名为“ARROW”的注册临床研究(注册号:NCT03037385)。这项多中心、开放标签、多队列的临床试验共纳入114例非小细胞肺癌患者,其中27例为初治患者,87例患者既往接受过含铂方案化疗,所有患者均由NGS,FISH等检测法确认为MET融合阳性,研究主要评价指标为客观缓解率(ORR)及反应持续时间(DoR)。结果揭晓让人振奋,对于初治患者,Pralsetinib的ORR高达70%,其中58%的患者缓解持续时间达6个月以上,更有11%的患者达到完全缓解,可评估患者组群的中位DoR为9个月。对于接受过含铂方案化疗的患者其ORR也可达57%,其中80%的患者缓解持续时间超过6个月,有5.7%的患者达到完全缓解,对于缓解持续时间的评估未能完成,因为可评估的经治患者目前观察到的最短缓解时间也长达15.2个月,其余患者尚处于观察之中(见图2)。
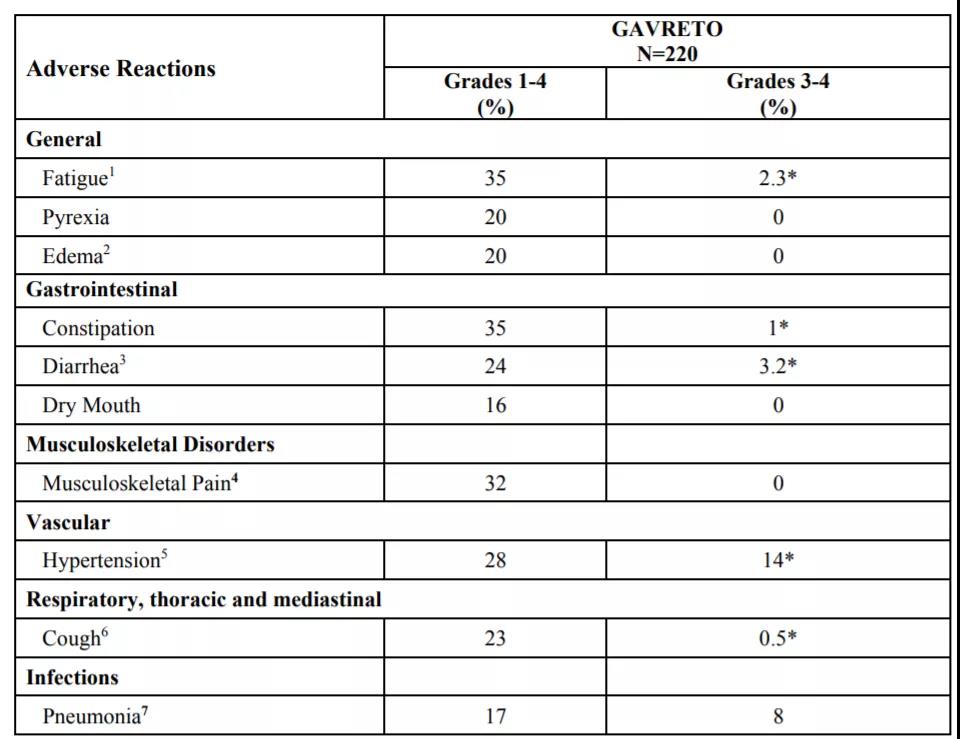
Pralsetinib推荐剂量为400mg口服,每日一次,建议空腹服用(饭前1小时或者饭后两小时)。Pralsetinib观察到的最常见的不良反应包括转氨酶(AST/ALT)升高、贫血、白细胞下降(包括中性粒细胞和淋巴细胞下降)、肌酐升高、碱性磷酸酶升高、疲劳、便秘、肌肉骨骼疼痛、高血压和血小板减少等。其中发生频率最高的不良反应依次为高血压(42%)、乏力(37.8%)和便秘(36%),但乏力和便秘3级以上的严重不良反应频率仅仅为2.3%和1%,值得引起注意的是3级以上高血压事件发生率可达14%,因此用药期间需要密切监测血压并及时进行降压药物干预。
NSLCLC强势获批,RET突变/融合阳性甲状腺癌适应证指日可待
值得一提的是作为高选择性强效RET抑制剂,在“ARROW”研究中,Pralsetinib不仅对非小细胞肺癌表现出突破性的数据,对于RET突变阳性的甲状腺癌初治患者,整客观缓解率达到了74%,86%的患者缓解持续时间达到15个月以上。对于经治患者,整体缓解率同样可以达到60%,90%以上的患者持续缓解时间超过18个月。对于RET融合阳性的甲状腺癌患者客观缓解率更是高达91%,疾病控制率达到了惊人的100%。基于如此优秀的临床试验数据,FDA目前已经授予了Pralsetinib用以治疗RET突变阳性的晚期/转移性甲状腺髓样癌及RET融合阳性的甲状腺癌新药适应证的优先审查资格。此外Pralsetinib研发母公司蓝图医药已经于今年年1月启动了名为“Accele RET Lung”的Ⅲ期临床试验。旨在评估Pralsetinib一线治疗RET融合阳性非小细胞肺癌患者的无进展生存期(PFS)这一关键终点数据,并将单药或者联合目前大热的免疫治疗药物帕博利珠单抗(K药)对比标准含铂方案化疗的疗效,其结果将有望改变目前RET融合阳性非小细胞肺癌患者的治疗推荐。虽然在非小细胞肺癌患者中RET融合阳性的比例只占1-2%,但针对这部分患者既往除了Selpertinib(首款RET TKI)外并无他药,靶向治疗依然处于较弱势的地位,Pralsetinib获批将进一步改写RET融合阳性非小细胞肺癌治疗的格局。同时我们也期待着Pralsetinib用于甲状腺癌的适应证能够早日获批。目前甲状腺癌治疗领域也迈入了分子靶向时代,从MET靶点抑制剂Cabozantinib到BRAF抑制剂达拉非尼,各种靶向药物百花齐放,不断突破着甲状腺癌治疗的新高度。Pralsetinib在ARROW研究中对于RET突变/融合阳性甲状腺癌表现的惊人数据表明又一枚重磅药物即将诞生,让我们期待这款药物能在肿瘤靶向治疗领域造福更多患者。
参考文献
1、https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-pralsetinib-lung-cancer-ret-gene-fusions?utm_medium=email&utm_source=govdelivery
2、http://www.globecancer.com/azzx/show.php?itemid