哪些转移性癌症需要检测基因突变?首部二代测序指南来啦
二代测序(NGS),又称为高通量测序,是低成本、高准确度、一次可对多个样本的几十万甚至几百万条DNA分子同时进行快速测序分析的新一代测序技术,虽然已被广泛运用于临床,但尚无科学协会对其在肿瘤学实践中的应用提出建议。
早在2018年,欧洲肿瘤内科学会(ESMO)发布了分子靶点临床可行性量表(ESCAT),根据对患者管理的影响将分子靶点分为6个等级,针对导致全球死亡最多的8种癌症中所发生的基因组改变,ESCAT量表评估了其证据等级和临床意义。
近日,ESMO在旗下期刊Annals of Oncology正式发布了转移性癌症患者NGS指南。该指南由ESMO转化研究和精准医学专家组参与,并基于ESCAT制定建议。这也是科学界关于NGS使用的第一个指南。

在这份指南中,专家组基于ESCAT评级和突变发生率,以及有效靶向药物的情况,进一步评估NGS对于每种肿瘤类型的效率和临床价值。
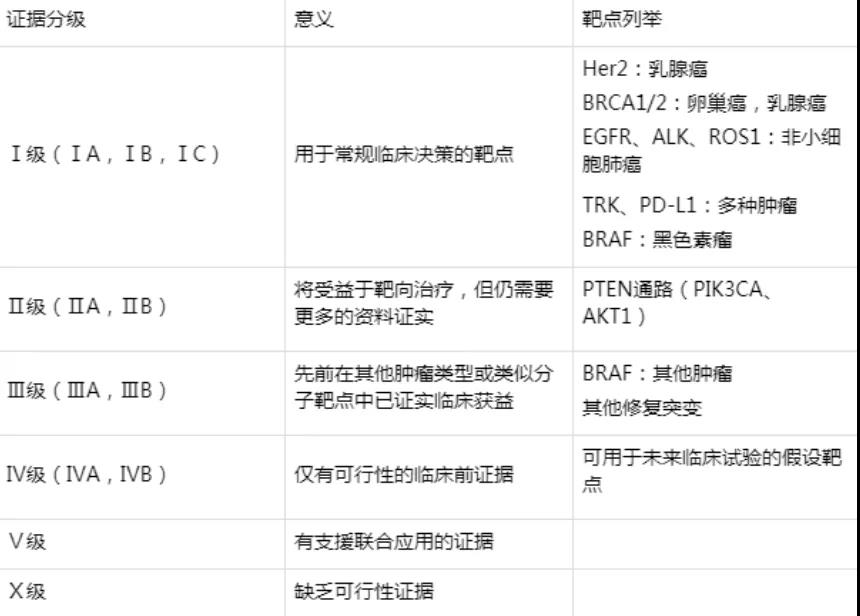
根据目前的证据,ESMO建议如下:
一、晚期非鳞状非小细胞肺癌(NSCLC)、前列腺癌、卵巢癌和胆管癌可常规使用NGS:
对于晚期非鳞状NSCLC,建议通过肿瘤(或血浆)样本来检测ESCAT I级突变。
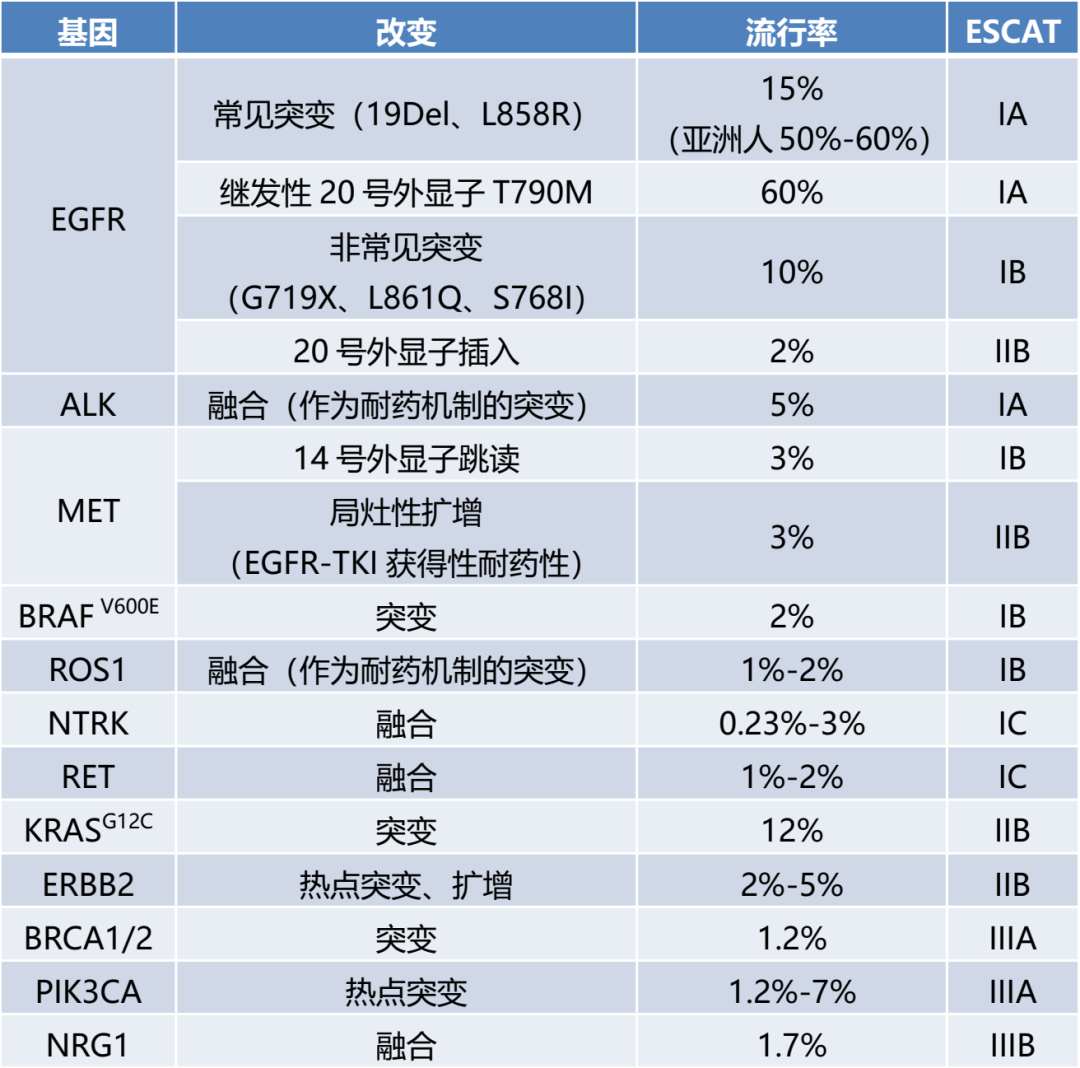
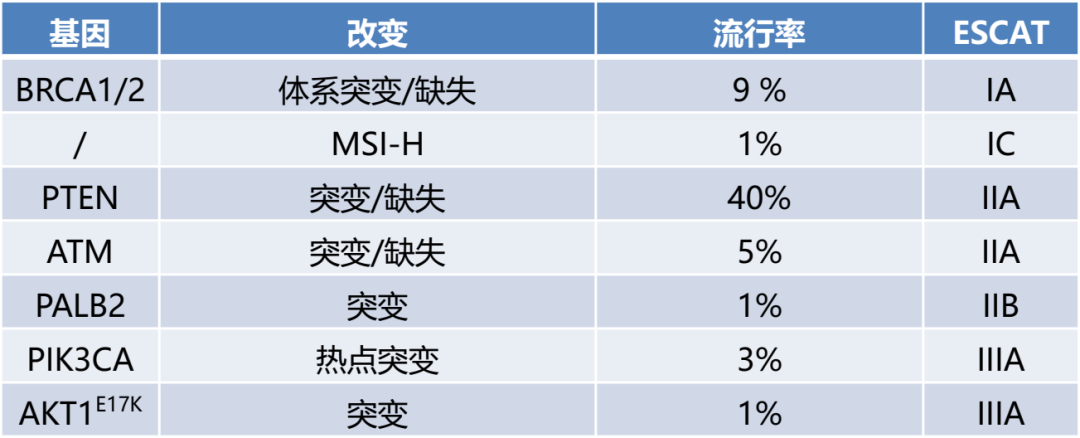
对于前列腺癌,患者所在地区如可获得PARP抑制剂,建议至少检测BRCA1/2突变,根据AKT抑制剂三期试验的初步结果,也可以考虑增加检测PTEN突变。
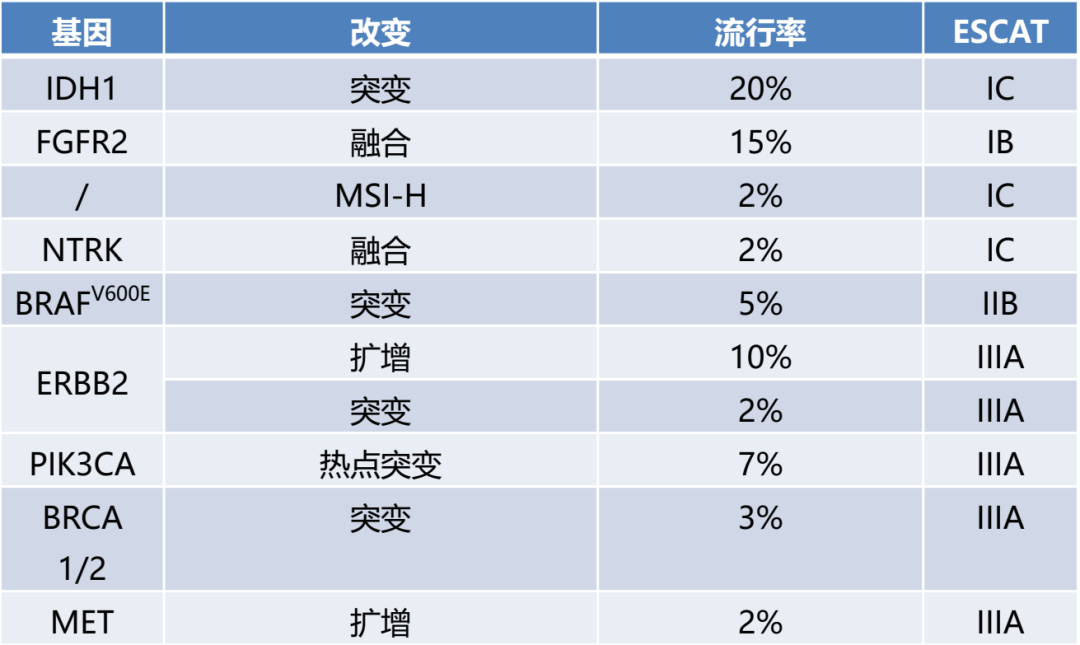
胆管癌建议检测IDH1、FGFR2、NTRK等ESCAT I级突变。
卵巢癌中的BRCA1/2体细胞突变与PARP抑制剂获益增加相关,也可常规使用NGS。
二、建议检测子宫内膜癌、小细胞肺癌、宫颈癌高分化和中分化神经内分泌肿瘤、唾液腺癌、甲状腺癌和外阴癌的肿瘤突变负荷(TMB),这些癌症中的高TMB患者对免疫疗法反应较好。
三、乳腺癌、肺鳞癌、胃癌、胰腺癌和肝细胞癌不推荐使用NGS。
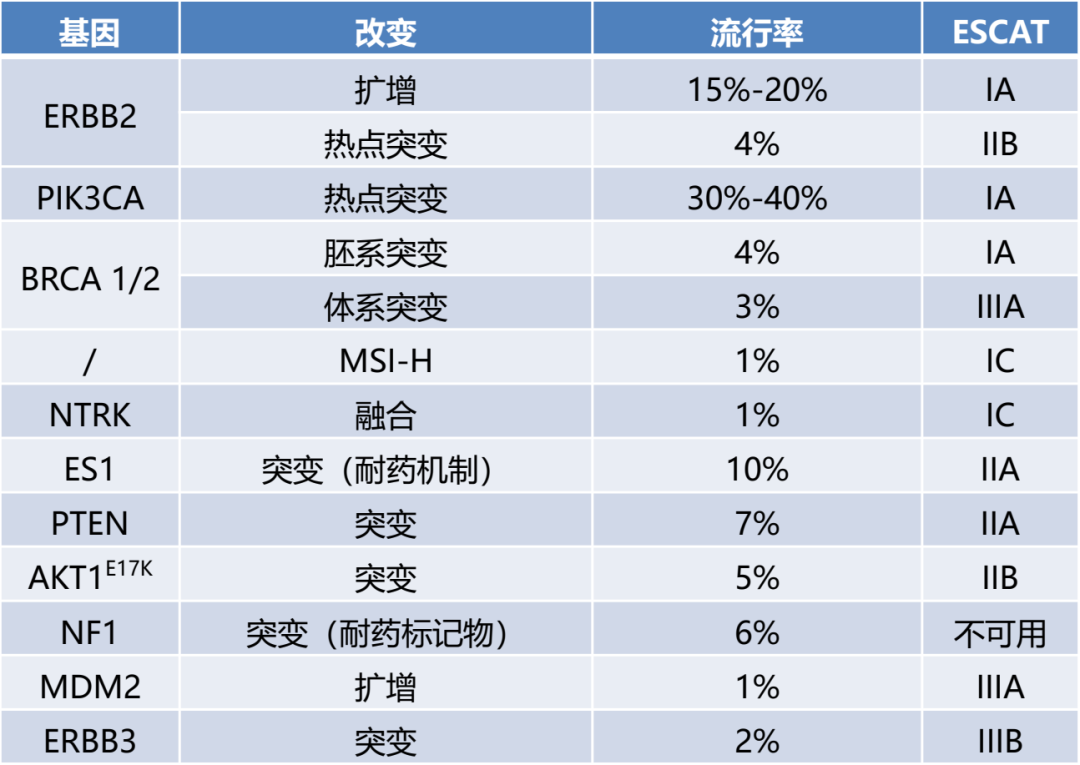
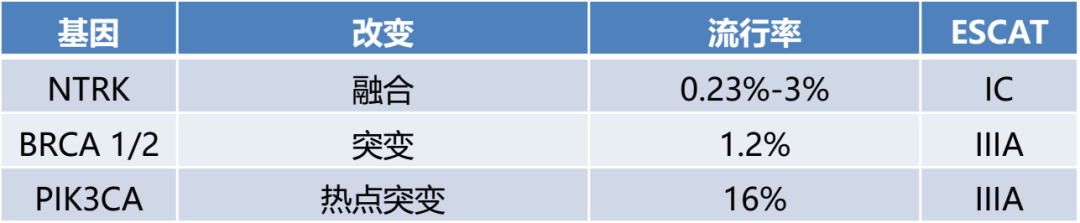
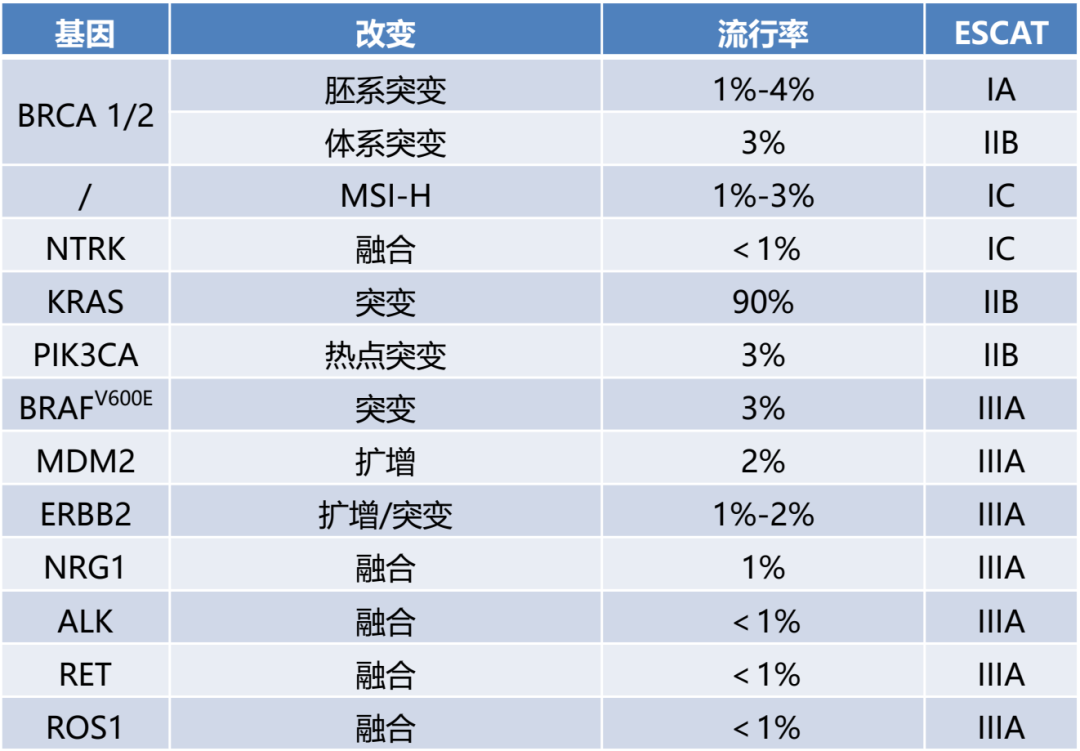
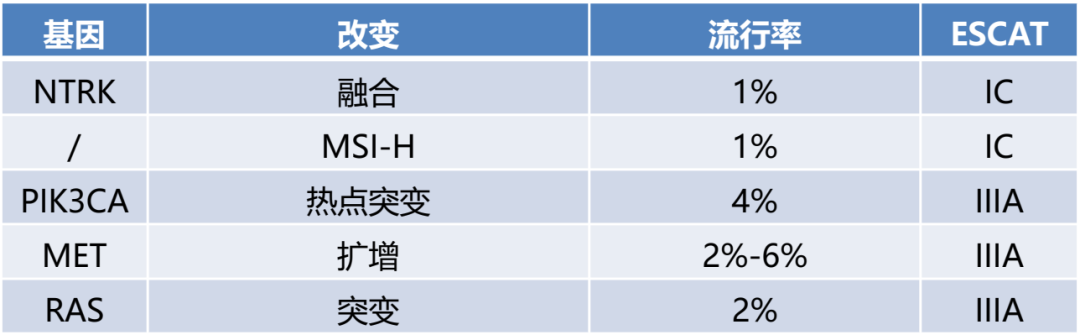
四、结直肠癌中,大多ESCAT I级突变是KRAS、NRAS和BRAF基因中的突变热点,且微卫星不稳定(MSI)状态需由IHC测试或PCR测试检测。但成本可控情况下,NGS可以替代PCR检测,以检测ERBB2扩增、NTRK融合并高精度检测MSI状态。
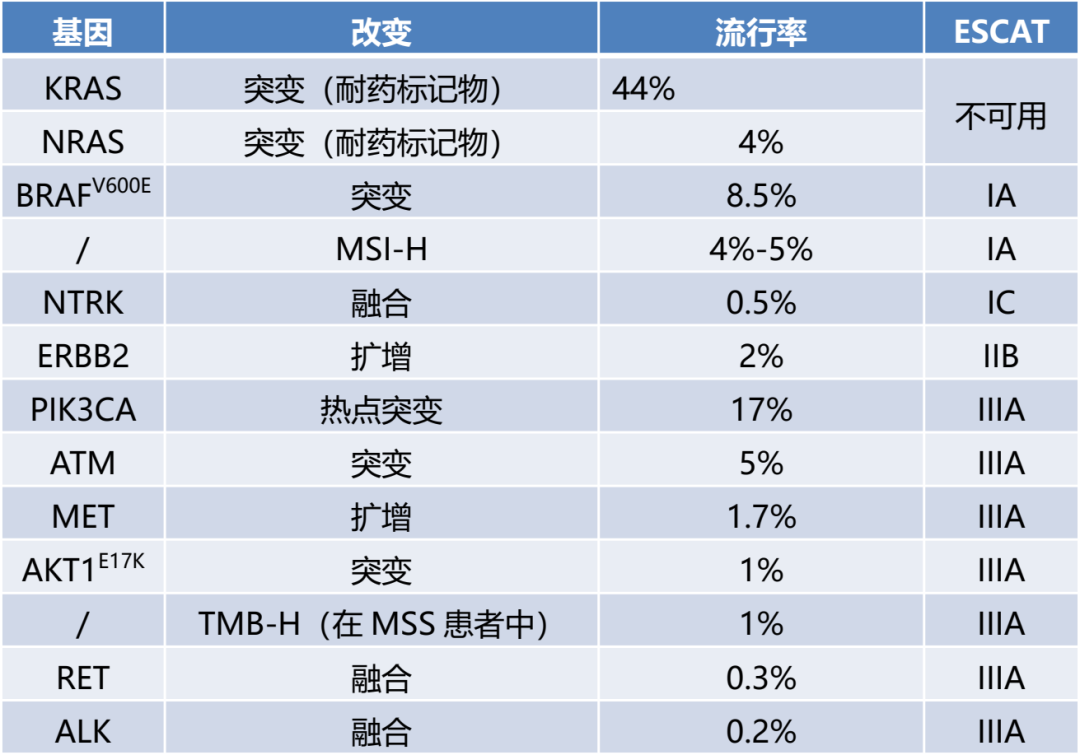
除了以上转移性癌症的基因组改变ESCAT分级表,ESMO强烈建议临床研究中心通过将多基因测序作为其任务的一部分,加速癌症研究和药物的研发,为病人提供获得创新性治疗的途径并收集相关数据,此外,还应当在临床试验的同时进行经济评价,以提供促进这一领域的证据。
同时ESMO认为,在不需要额外费用的情况下,患者和医生可以共同决定是否选择大批量基因的测序套餐以获得潜在的收益。
参考文献:
[1] Mosele F, et al. Recommendations for the use of next-generation sequencing(NGS) for patients with metastatic cancers: A report from the ESMO Precision Medicine Working Group. Ann Oncol, DOI:https://doi.org/10.1016/j.annonc.2020.07.014
[2] Marino P, Touzani R, Perrier L, et al. Cost of cancer diagnosis using next-generation sequencing targeted gene panels in routine practice:a nationwide French study. Eur J Hum Genet. 2018;26(3):314e323.
[3] Pagès A, Foulon S, Zou Z, et al. The cost of molecular-guided therapy in oncology: a prospective cost study alongside the MOSCATO trial.Genet Med. 2017;19(6):683e690
[4] Van Nimwegen KJM, van Soest RA, Veltman JA, et al. Is the $1000 genome as near as we think? A cost analysis of next-generation sequencing. Clin Chem. 2016;62(11):1458e1464
[5] J Mateo, D Chakravarty, R Dienstmann, et al. A framework to rank genomic alterations as targets for cancer precision medicine: the ESMO Scale for Clinical Actionability of molecular Targets(ESCAT). Annals of Oncology. mdy263, https://doi.org/10.1093/annonc/mdy263