免疫检查点抑制剂相关肺炎的研究进展
免疫检查点抑制剂相关肺炎(checkpoint inhihitor-related pneumonitis,CIP)临床发生率偏低,但却是一种严重的并发症,通常伴有咳嗽、呼吸困难和缺氧等表现以及肺部浸润的影像学特征,通常对皮质类固醇治疗有效,严重的CIP可导致死亡。因此,CIP需要及早诊断和治疗,了解CIP的发病情况和临床特征可能有助于其早期诊断和治疗。
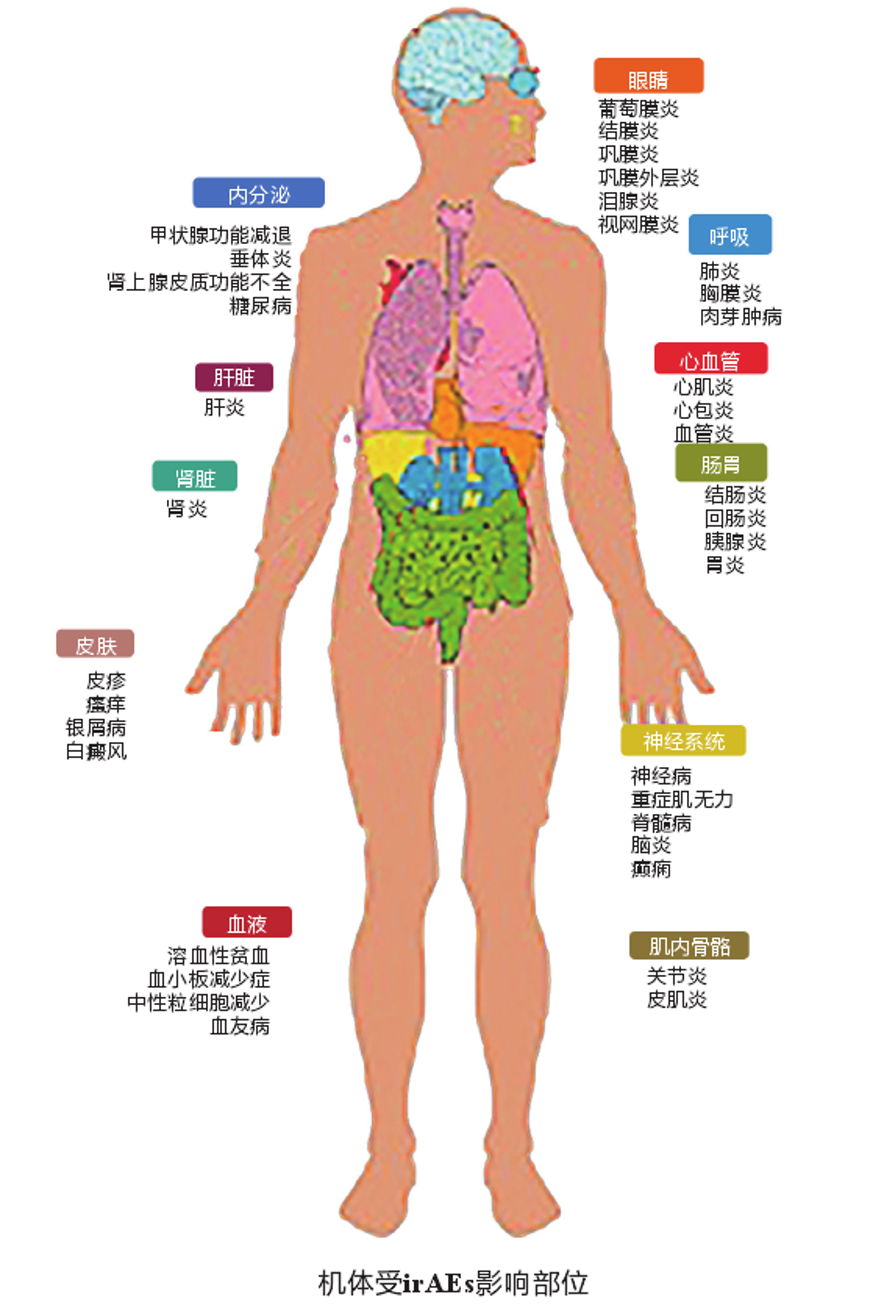
发生率及发作时间
肺癌CIP发生率在3%-5%,严重不良反应发生率约为1.8%。一项Meta分析发现:PD-L1抑制剂和PD-1抑制剂导致的肺炎总发生率分别为3.6%、1.3%, 3-4级严重肺炎的发生率为1.1%、0.4%。回顾性研究表明,CTLA-4抑制剂较PD-1/PD-L1抑制剂治疗引起的肺炎少,发生率低于1%。但当与前两者联用时发生率增加。
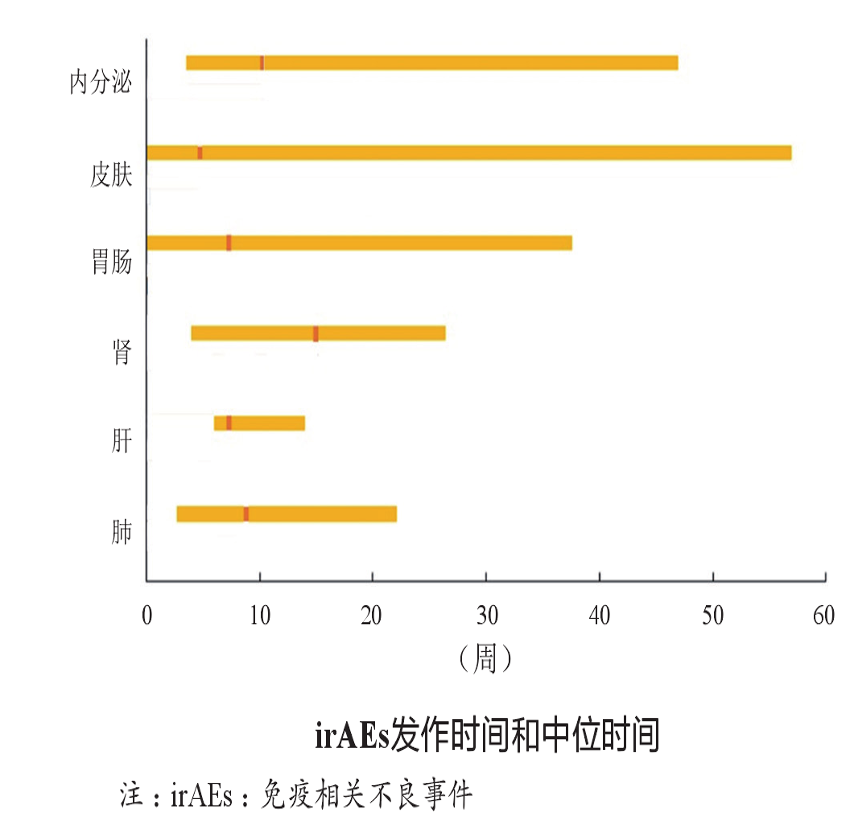
CIP的发作时间不同,基本集中在2.5个月,相对其他irAEs而言,ICIs相关性肺炎发作时间较晚。
临床表现
CIP临床上主要表现为非感染性肺部炎症,症状和体征均缺乏特征性。20%-33%CIP患者无明显的不适,仅在随访的胸部CT扫描时发现影像学上的肺部炎症表现。
CIP的临床表现主要是呼吸困难(53%)和咳嗽(35%),而发热(12%)和胸痛(7%)等症状发生较少见。在其他研究中亦可见心动过速、发组、疲劳、寒战等表现。也有部分缺氧严重的CIP患者发展至呼吸衰竭,危及生命。因此,当患者在接受ICIs治疗过程中出现新发或加重的呼吸系统症状,需高度警惕CIP的可能。
肺部毒性管理
依据分级原则,肺部毒性管理策略为:无症状的1级患者停药,密切监测患者状况,若症状无进展则继续治疗;2级症状患者停药,使用皮质类固醇药物缓解;3级以上症状患者视情况采用呼吸支持,使用激素类药物治疗30 d,利用辅助设备监测患者情况。
病例分享
一位64岁男性,曾是重度吸烟者,被诊断为左肺腺癌,并伴有多发性肺转移及股骨骨转移。这名患者接受抗PD-1 nivolumab(3mg/kg q2w)治疗——作为二线治疗。这项治疗是在意大利奥斯塔地区医院肿瘤和血液科进行的。
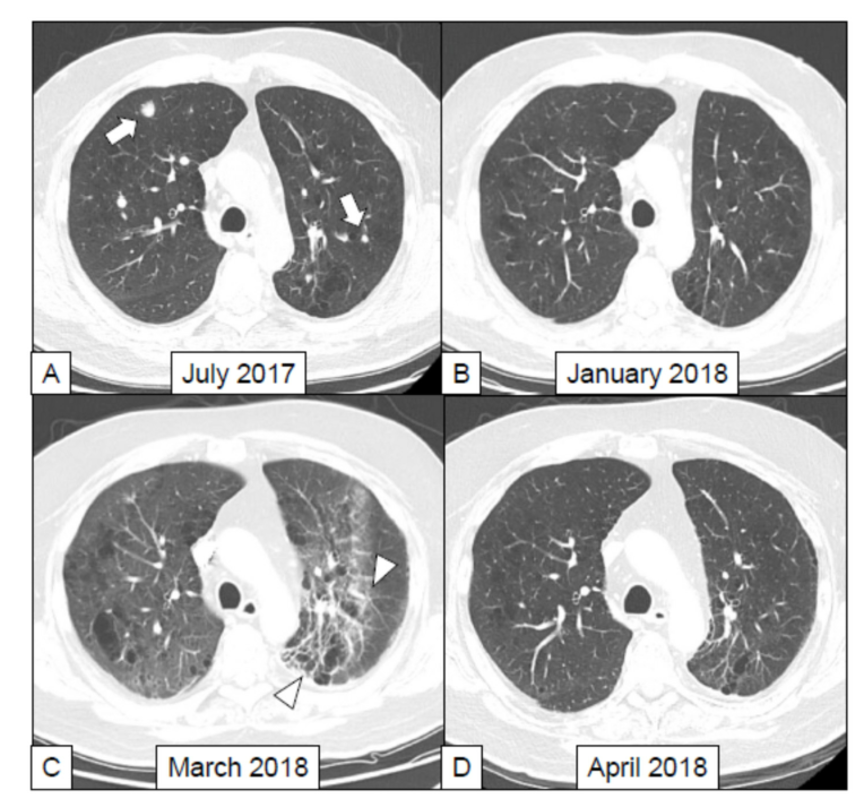
(A)2017年7月免疫治疗开始前进行的肺部CT扫描显示双肺均存在肺转移(B)在6个月后的CT扫描中,这两个转移灶不再明显。根据iResist 1.1标准被归类为部分应答(iPR)(C)在最后一次CT扫描后一个月,患者突然出现疲劳和呼吸困难,周围血氧饱和度达到80%,没有发烧,全身炎症标志物循环水平正常。2018年3月(免疫治疗开始后8个月)进行了肺部CT检查,显示弥漫性间质增厚与毛玻璃样改变相关,在后叶区域更为明显。怀疑免疫相关肺炎肺炎(D)患者接受了大剂量甲泼尼龙(1毫克/公斤)治疗,2018年4月进行的随访CT扫描显示,患者的呼吸道症状有所改善,肺部病理结果也有所缓解。
文献参考:
1.李小雪,任军,王鑫, 等.免疫检查点抑制剂相关毒性管理研究综述[J].中国医学前沿杂志(电子版),2019,11(12):27-31.
2.谭嘉蓉,胡成平.免疫检查点抑制剂相关致命性不良反应及管理策略[J].中国实用内科杂志,2020,40(4):340-344.
3.张思燚,谢长生.免疫检查点抑制剂相关肺炎的研究进展及管理策略[J].肿瘤学杂志,2020,26(5):391-395.
4.薛鹏,徐芃芃,毛昀, 等.非小细胞肺癌免疫检查点抑制剂相关性肺炎研究进展[J].中国肿瘤,2019,28(5):367-372.
5.Cancers(Basel). 2019 Mar 5;11(3):305. doi: 10.3390/cancers11030305.