靶向局部双剑合璧有望为超“upto7”BCLC-B期肝癌患者提供联合新获益
我国是全球肝癌发病率最高和病死数最多的国家,原发病例占全球病例的半数以上,因此我国的肿瘤防治仍面临严峻形势。阿帕替尼作为我国最早一批自主研发的小分子抗血管生成靶向药物,上市已有7年余。2020年,由南京金陵医院秦叔逵教授牵头的AHELP研究成果在ASCO口头报告专场重磅发布。同年7月18日,基于AHELP研究取得的突出成果,阿帕替尼获2020版《CSCO原发性肝癌诊疗指南》Ⅰ级专家1A类证据推荐,用于晚期肝癌二线治疗。
为了让临床医生更好地掌握靶向药物阿帕替尼的特性,从而将其更好地应用于临床,本报特邀AHELP研究的主要参与者之一,广东省人民医院陈晓明教授,为我们解读AHELP研究成果并分享局部治疗与靶向药物联合应用策略。以下内容为采访整理精粹,以飨读者。

广东省人民医院主任医师
广东省医学科学院教授
广东省人民医院肿瘤中心副主任
综合(介入)肿瘤一区主任
中国抗癌协会介入医学临床研究专业委员会主任委员
世界华人肿瘤医师协会肿瘤微创与介入专业委员会副主任委员
广东省医学会肝癌分会副主委及介入治疗学组组长
广东省医学会介入医学分会副主委
广东省临床医学会肿瘤微创诊疗专业委员会第一届副主任委员
广东省医学教育协会介入专业委员会第一届副主任委员
阿帕替尼AHELP研究利剑出鞘直指肝癌二线适应证
“
Q、您如何评价AHELP研究的安全性和有效性?是否能请您分享下相关病例?
陈晓明教授:AHELP研究是一项大型的随机、双盲、安慰剂对照RCT研究,循证医学证据已达最高级别Ⅰa级,结果可信度极高。从疗效数据来看,与安慰剂相比,阿帕替尼可显著延长肝癌患者的中位OS(8.7个月对6.8个月)和中位PFS(4.5个月对1.9个月),另外其ORR达10.7%,显著高于对照组的1.5%。众所周知,ORR可有效反映治疗的实际效果,并最终转化为PFS或OS获益,因此对方案疗效的评估极有参考意义。从安全性数据来看,目前阿帕替尼已获批胃癌治疗适应证,而其应用于晚期HCC二线治疗的安全数据与胃癌中的应用情况类似,即无新的不良反应发生,且安全性整体可控。
相关病例
患者情况
患者男性,48,主诉“肝癌切除后半年余,复发1月”就诊。
诊疗经过
2016年9月5日口服1周期(4 w)阿帕替尼(750 mg)后出现3度手足综合征,停用10天后改为阿帕替尼500 mg。
2019年9月22日,因足底皮肤破损,疼痛导致无法行走,改为阿帕替尼250 mg维持治疗。
患者自第2周期起,每两个周期(8 W)进行影像学评价,均评价为PR。
2020年1月15日,患者因出现尿蛋白升高、肾病综合征,停药退出研究组,直至退出研究组仍评价为PR(图1)。
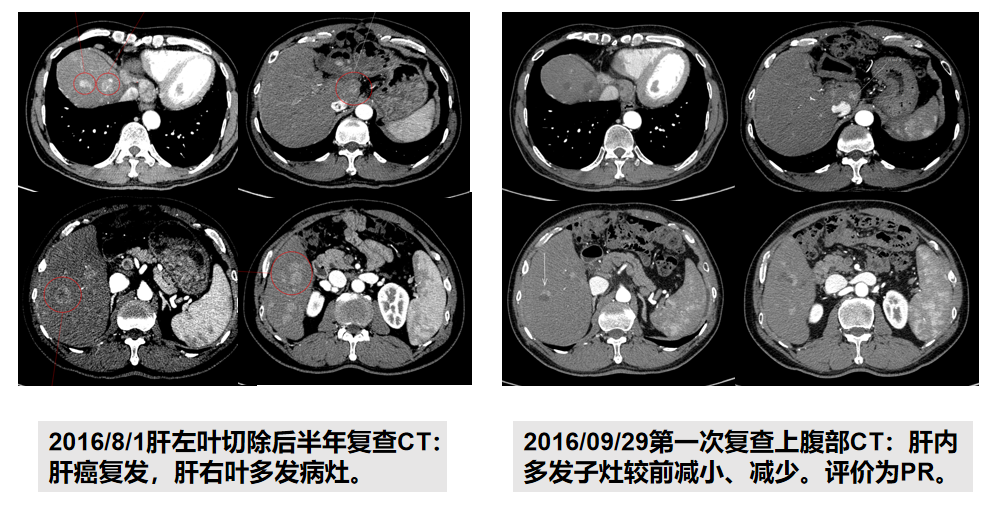
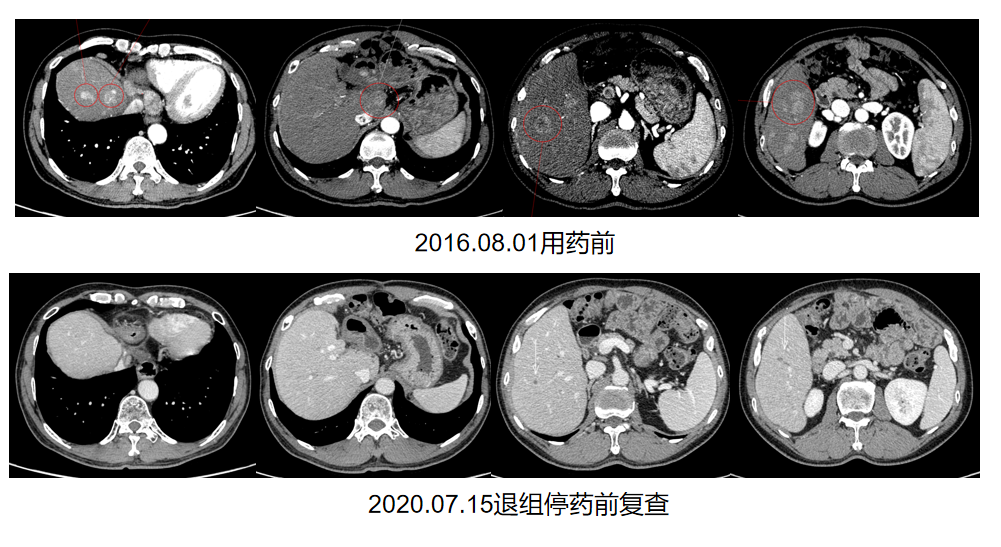
治疗总结
Child-Pugh A级肝细胞癌切除术后复发患者,口服阿帕替尼单药治疗后,首次疗效评价即为PR,并持续缓解近4年;在安全性方面,患者出现手足综合症、AST/ALT升高、蛋白尿等副反应,安全性整体可控。
“
Q、作为AHELP研究的主要参与者之一,您如何看待阿帕替尼获2020版《CSCO原发性肝癌诊疗指南》Ⅰ级专家1A类证据推荐用于晚期HCC二线治疗这一成果?
陈晓明教授:不论是ASCO年会还是CSCO会议,均注重临床实践。2020年5月,AHELP研究成果在ASCO口头报告专场首次公布。同年7月,阿帕替尼即获2020版《CSCO原发性肝癌诊疗指南》Ⅰ级专家1A类证据推荐,用于晚期肝癌二线治疗。能够在如此短的时间内获高级别证据推荐,首先证明了领域内专家对研究成果的高度肯定。其次对于患者来说,此举意味着应用方案较为有限的肝癌二线治疗中,多了一种新选择。最后对于我国肝癌治疗领域来说,自主创新靶向药物阿帕替尼的研究成果能够亮相国际顶级学术会议舞台,代表了我国肝癌诊疗水平的飞速进展,这是国家强大综合实力的体现,也是国家的荣誉。
基于以上三方面原因,相信阿帕替尼获批我国甚至国际肝癌二线治疗适应证值得期待。而其后续在联合治疗的应用探索,如联合局部或免疫治疗等,同样值得关注。
TACE联合靶向应用需趁早,超“upto7”标准肝癌患者联合方案或可带来更佳获益
“
Q、您认为介入如TACE联合靶向药物治疗肝癌的重要意义何在?在您看来,介入联合靶向治疗是否具有疗效“1+1>2”的效果?是否能请您分享下相关病例?
陈晓明教授:对于BCLC-C期肝癌患者,国外指南多推荐以系统治疗为主,而国内指南在此基础上还联合了局部治疗应用推荐。对于BCLC-B期肝癌患者,国内外指南均推荐应用TACE作为标准治疗方案。已有研究证明,经TACE联合靶向药物治疗的患者,与单独应用TACE相比,PFS获益明显。另一项小样本探索性研究也证明,对于超过“upto7”标准的肝癌患者,靶向治疗较TACE可能提供更佳的获益。提示了TACE联合靶向药物治疗肝癌的可观应用前景,然而不同方案的具体应用时机还需要研究者的进一步探索。
结合既往文献及个人研究经验来看,我认为介入联合靶向或免疫治疗等,可以达到1+1>2的效果。一项由我牵头开展的抗血管生成药物联合肝动脉灌注化疗(HAIC)一线治疗晚期肝癌的回顾性研究成功入选2020年ASCO壁报展示,结果表明,联合治疗的ORR为58.3%(RECIST标准)和66.7%(mRECIST),DCR达到79.2%。众所周知,单独应用HAIC或抗血管生成药物治疗肝癌的ORR分别约为30%和20%,而联合方案明显发挥出了1+1>2的治疗效果。我相信,阿帕替尼肝癌适应症获批以后,同样可以联合局部治疗进行肝癌领域的相关探索。
相关病例
患者情况
患者男性,68,主诉“肝癌切除后3年,再发1月”入院。
诊疗经过
2015年10月至2016年5月行TACE联合MWA治疗(图2)。
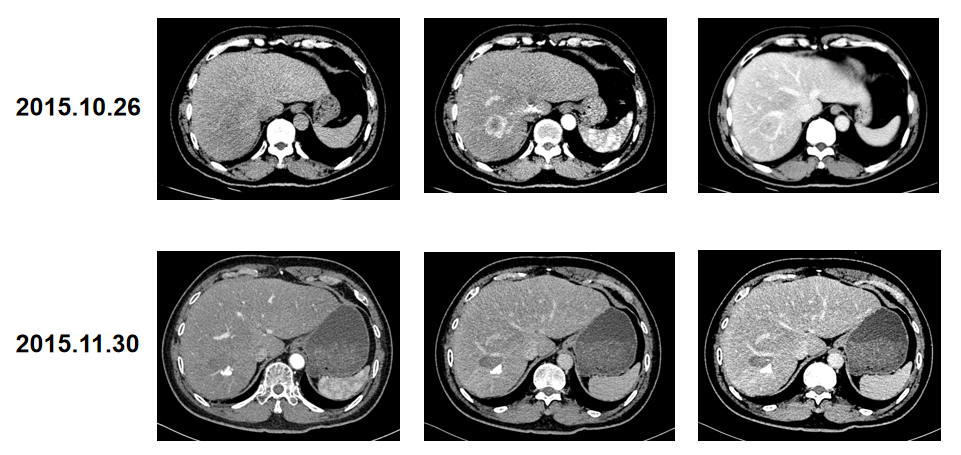
2017年5月15日复查MR,未见明确异常强化(图3)。
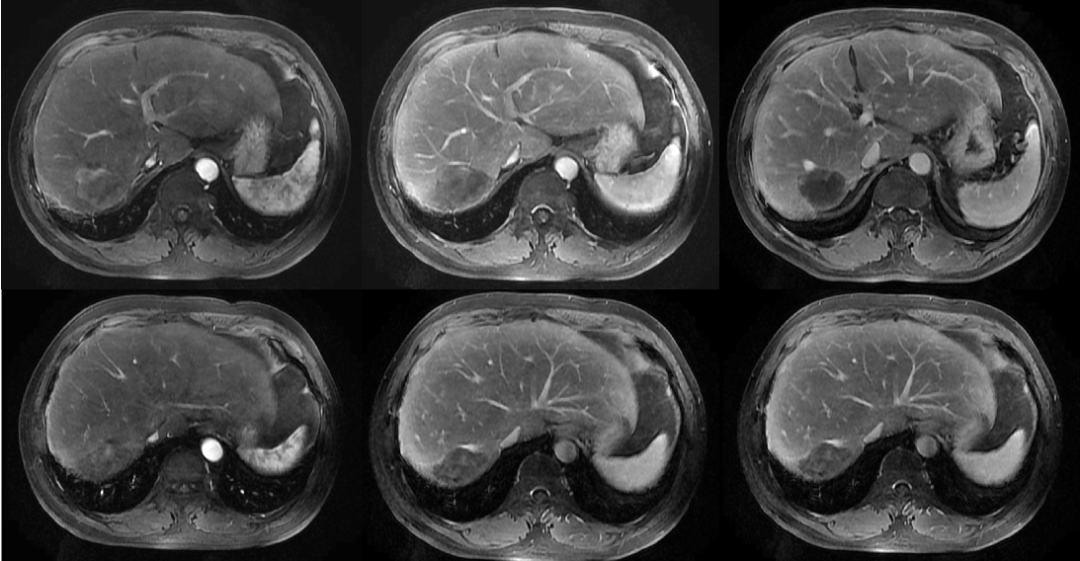
2018年4月8日复查CT示,肝S7病灶未见强化,病灶周边肝实质较明显强化,病灶周围见片状低密度影,增强扫描见不均匀明显强化。肿块侵犯肝静脉、下腔静脉、右心房(图4)。
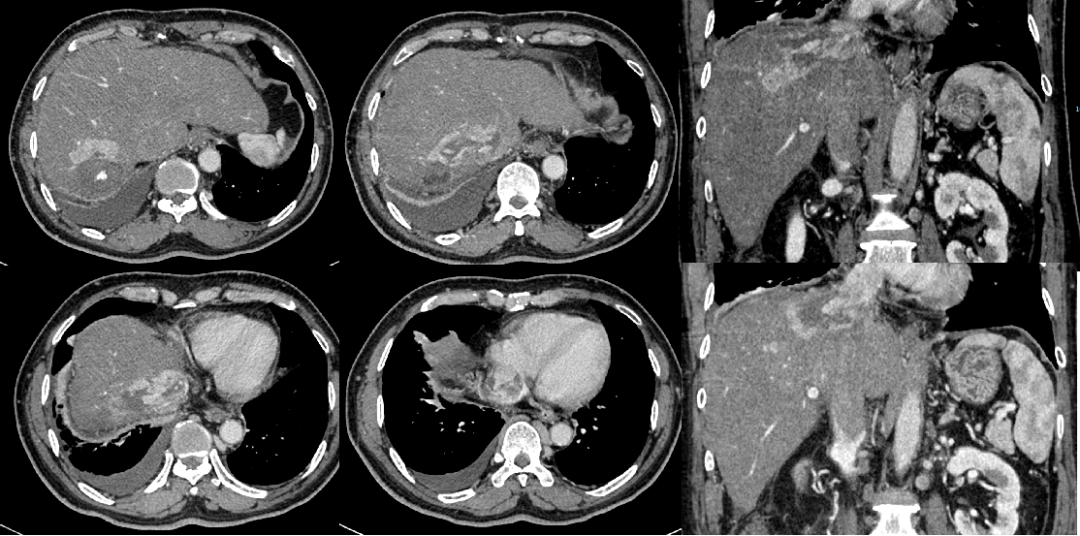
2018年4月10日行TACE治疗,出院后口服阿帕替尼500 mg治疗。
2018年5月23日复查CT,提示肝脏S7段病灶内见少量碘油沉积,未见明显强化;肝右静脉、下腔静脉及右心房内病变较前缩小,见少量碘油沉积,增强扫描大部分无明显强化。评价为PR(图5)。
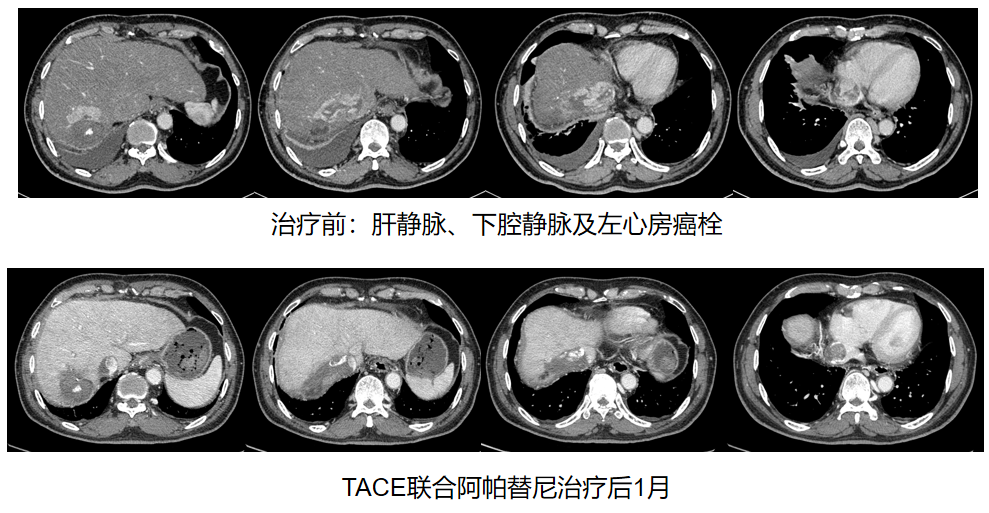
继续口服阿帕替尼500mg,规律复查,癌栓稳定,未见强化(图6)。
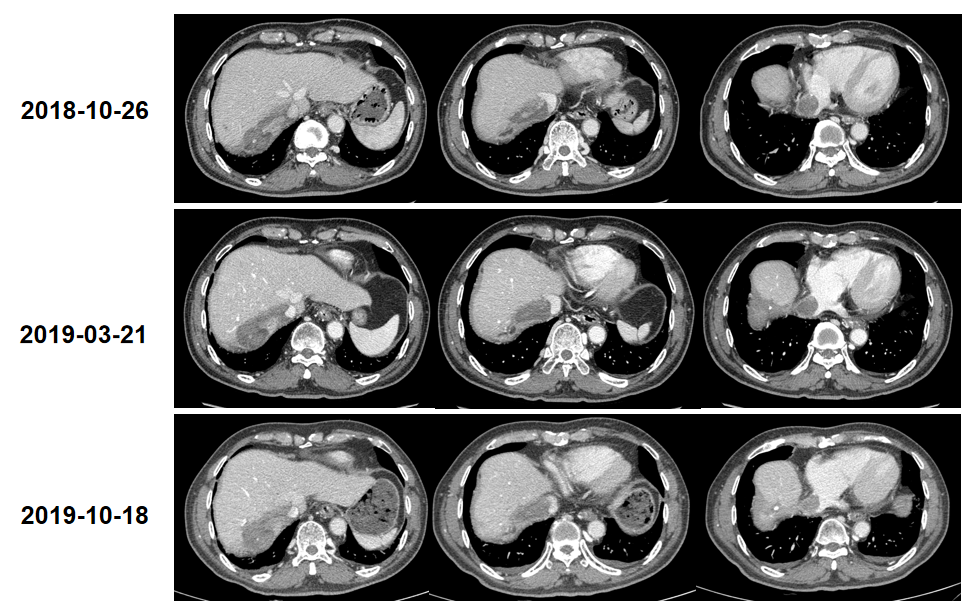
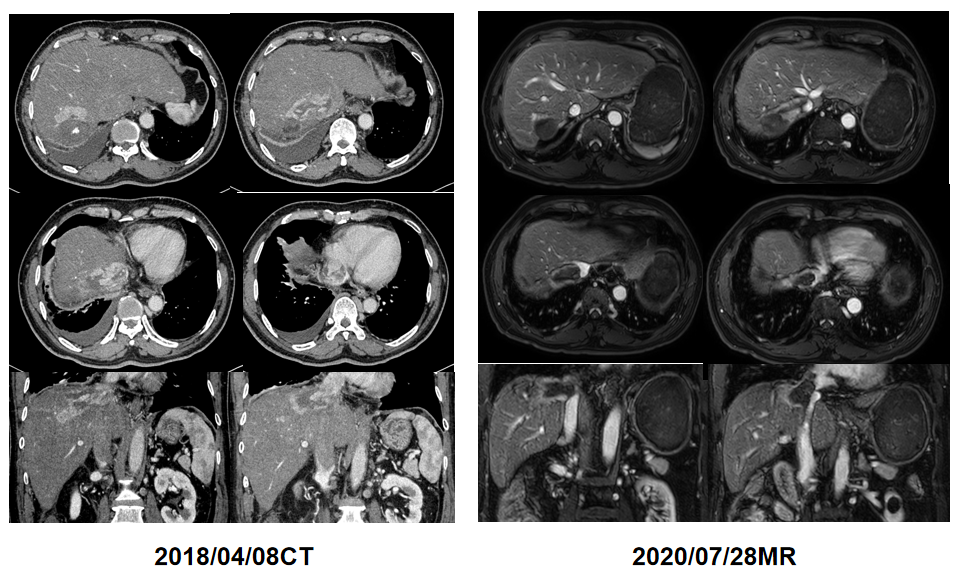
治疗总结
Child-Pugh A级肝癌切除术后复发患者,行TACE联合MWA治疗后PFS达22.3个月。后患者病灶周围复发,同时合并肝静脉、下腔静脉及右心房癌栓,行TACE联合阿帕替尼治疗后,病灶、癌栓坏死退缩;患者继续口服阿帕替尼维持治疗,癌栓达稳定状态。值得一提的是,患者下腔静脉栓塞(血供减少,但并未坏死),予阿帕替尼治疗后,癌栓完全没有强化,这在临床中极为少见。目前患者生活质量佳,阿帕替尼可观ORR带来的整体疗效值得肯定。
“
Q、您认为在TACE与阿帕替尼的联合方案中,应如何确定二者的应用时间?
陈晓明教授:一旦确定适用人群便应尽早联合。目前国内相关指南均推荐对BCLC-C期肝癌患者应用系统联合局部治疗,而对于BCLC-B期肝癌患者,尚无统一的联合治疗标准。但众多领域内专家认为,超过“upto7”标准的患者应考虑联合治疗策略。而我们团队也于近日递交了研究伦理申请,以期通过改变局部治疗方式,探讨灌注联合靶向是否能为超过“upto7”标准的肝癌患者带来生存获益。
“
Q、最后能否请您分享一下团队目前正在进行的研究项目和下一步的研究计划呢?
陈晓明教授:首先是关于申办方的研究。本科室是国内少有的临床试验基地,拥有非常专业的诊疗团队,并参与了多项药物上市前临床研究。目前团队正在进行的临床研究主要涉及两个方向,即根治性治疗后的辅助治疗和TACE联合靶向治疗。相信随着后续研究的进展,会有更多的证据可以解答关于肝癌联合方案的应用时机及优选人群的问题。
第二是关于团队自行开展的研究。如对TACE获益不显著的超过“upto7”标准的BCLC-B期肝癌患者,开展免疫联合靶向或HAIC联合免疫及靶向的疗效及安全性探索,以期为患者带来生存获益,当然研究者也需在过程中避免过度治疗。另外由于HAIC在晚期肝癌患者的诊疗中展现出了可期的应用前景,团队也在尝试开展HAIC联合靶向对比TACE联合靶向治疗BCLC-B期肝癌患者的疗效及安全性评估,希望让更多的患者从中获益。