多发性骨髓瘤患者的福音 D-RVd疗法再传捷报!
D-RVd联合治疗有望成为适合移植的NDMM的标准诱导治疗手段。
适合移植的初诊多发性骨髓瘤(NDMM)的一线治疗原则包括诱导治疗、巩固治疗(自体造血干细胞移植(ASCT)和维持治疗。
蛋白酶体抑制剂硼替佐米+免疫调节剂来那度胺+地塞米松的三联治疗(RVd)是NDMM的标准诱导治疗方案。该方案改善了未接受ASCT的NDMM患者的无进展生存期(PFS)和总生存期(OS),用于诱导缓解和巩固治疗时,中位PFS为50个月,4年OS率为81%。
达雷妥尤单抗是一种靶向CD38的IgGκ单克隆抗体。在NDMM和复发性/难治性MM的Ⅲ期临床试验中,基于达雷妥尤单抗的治疗方案改善了缓解深度,包括微小残留病变(MRD)转阴,延长中位PFS。
先前CASSIOPEIA研究已证实达雷妥尤单抗联合硼替佐米、沙利度胺、地塞米松(D-VTd)方案对于适合移植的NDMM患者来说,无论是移植前诱导治疗还是移植后巩固治疗,都可以提高其缓解深度及PFS,为诱导治疗。
因此,GRIFFIN研究旨在考察D-RVd方案联合ASCT是否可以改善NDMM的治疗效果,研究成果于近日发表在Blood上。

这项多中心Ⅱ期临床研究将207位符合条件的NDMM患者1:1随机分配至D-RVd组或RVd组,按国际分期系统(ISS)疾病分期(Ⅰ、Ⅱ或Ⅲ期)和肌酐清除率(30-50mL/min或>50 mL/min)分层;患者的中位随访时间为22.1个月;主要结局指标是严格意义的完全缓解(sCR)和MRD阴性(以<10-5计)的患者百分比。
患者的治疗反应分为五个等级:
• 严格意义上的完全缓解(sCR)
• 完全缓解(CR)
• 非常好的部分缓解(VGPR)
• 部分缓解(PR)
• 疾病稳定/疾病进展/未评估(SD/PD/NE)
在ASCT后巩固治疗结束时,疗效如下:
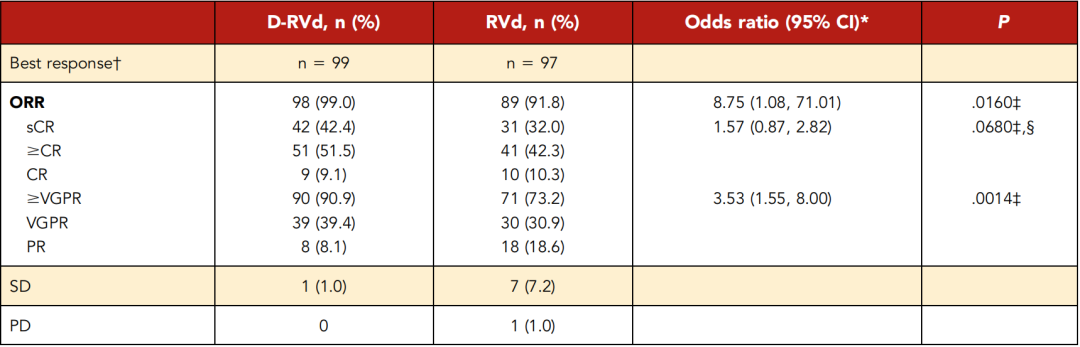
• D-RVd组和RVd组分别有42例(42.4%)和31例(32.0%)患者达到sCR(OR,1.57;95%CI,0.87-2.82;单侧P = 0.068),在预设的单侧&α;= 0.10时具有统计学显著性;
• D-RVd组在次要终点事件总体缓解率(ORR;99.0% vs 91.8%;P =0.016)和达到及优于VGFR的百分比(90.9% vs 73.2%;P=0.0014)均优于RVd组(表1);
表1 初步分析:巩固治疗结束时两组患者缓解情况汇总
随着治疗时间延长,更多患者达到临床缓解
• 末次随访时(图1),D-RVd组和RVd组实现sCR的比例分别为62.6%和45.4%(OR,1.98;95%CI,1.12-3.49;P =0.0177);
• 此外,D-RVd组的CR+sCR率为79.8%;RVd组为60.8%(OR,2.53;95%CI,1.33-4.81;P =0.0045);
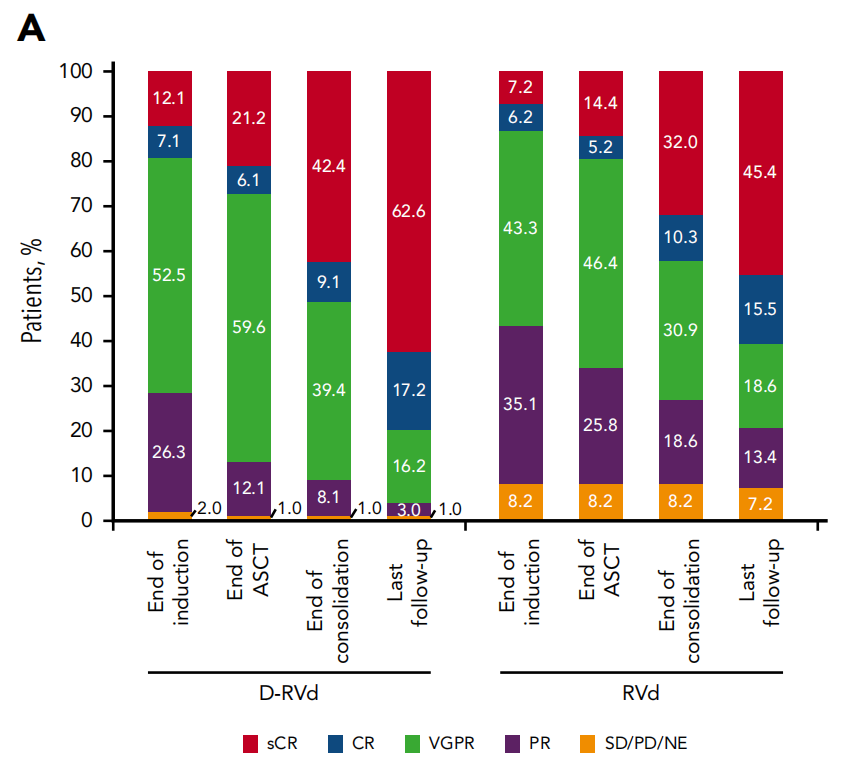
图1. 两组患者在治疗不同阶段的缓解率汇总 [诱导缓解、ASCT和巩固治疗结束时的数据来自。初步分析,还显示了末次随访的缓解数据(中位随访时间为22.1个月)]
MRD阴性率
对所有受试者中位随访22.1个月后发现与RVd相比,D-RVd组的MRD阴性率较高(表2):
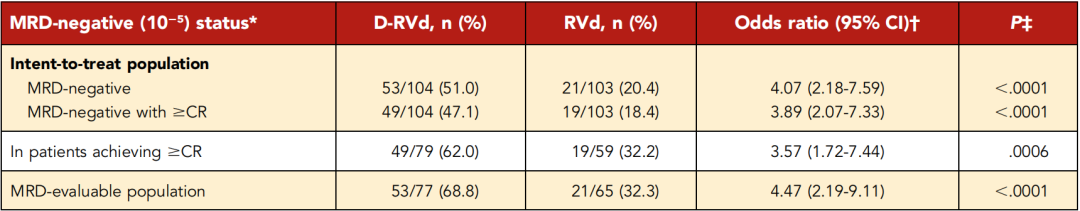
• 意向性治疗(ITT)人群中:51.0%[53/104] vs 20.4%[21/103](P=0.0001);
• 达到CR+sCR的患者中:62.0%[49/69]vs 32.2%[19/59](P=0.0006);
• 可评估MRD的患者中:68.8% [53/77] vs 32.3%[21/65](P<0.0001);
• 意向治疗人群中MRD阴性且≥CR的患者比例也比D-RVd组更高(47.1%[49/104] vs 18.4%[19/103];P=0.0001)。
表2 两组受试者在末次随访时的MRD阴性率
此外,在意向性治疗分析中,在诱导缓解阶段观察到D-RVd方案的MRD阴性率更高(21.2%[22/104]vs 5.8%[6/103];P =0.0019;图2)和诱导结束时患者达到更好的CR或缓解(47.4%[9/19]vs 7.7%[1/13];P =0.0237)。
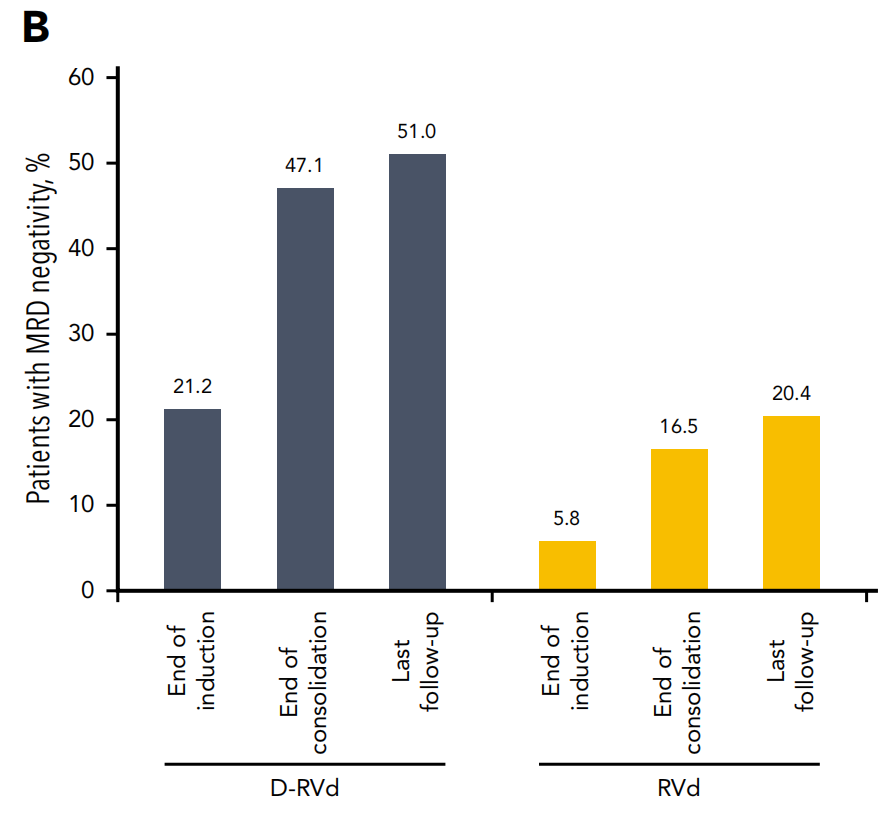
图2. 诱导缓解、巩固治疗和末次随访时,ITT人群中的MRD阴性率(所有MRD数据均来自随访期间的结果。在基线、首次出现疑似CR或sCR证据、诱导和巩固治疗结束时以及维持治疗12个月和24个月后分别评估MRD,不考虑缓解情况)
将MRD阴性的阈值提高至10-6,随访结束时,D-RVd组的MRD阴性率依然更高:18.3%(19/104)vs 6.8%(7/103);P =0.0197;在(CR+sCR)的患者中为24.1%[19/79] vs 10.2%[6/59];P=0.0447。
疾病进展
在随访结束时,D-RVd组和RVd组分别有4位(3.8%)和7位(6.8%)患者出现PD。两组患者均未达到中位PFS,D-RVd组和RVd组的24个月PFS率的Kaplan-Meier估计值分别为95.8%(95% CI,89.2-98.4)和89.8%(95% CI,77.1-95.7)(图3)。
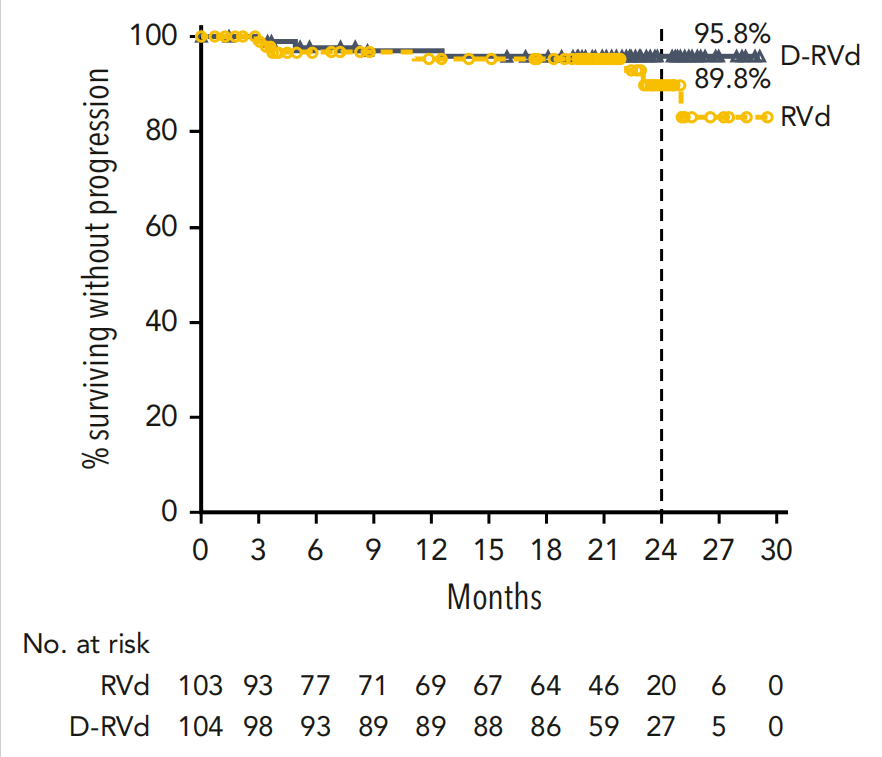
图3. ITT人群患者的PFS Kaplan-Meier估计值(两组均未达到中位PFS,此图展示24个月时PFS百分比的Kaplan-Meier估值)
安全性
根据不良事件评价标准(CTCAE)将不良反应分为1-5级,表3汇总了试验期间的常见血液系统/非血液系统不良反应。最常见的(≥10%)严重不良反应(3/4级)为中性粒细胞减少、淋巴细胞减少、血小板减少、白细胞减少和感染性肺炎。
表3 在治疗期间报告的最常见不良事件
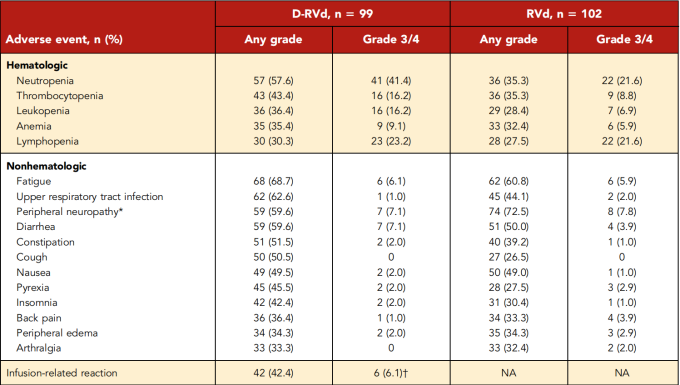
D-RVd组和RVd组分别有39例(39.4%)和52例(51.0%)患者报告了严重不良反应。最常见的(任一组发生率≥5%)是发热(D-RVd组10.1%;RVd组7.8%)和感染性肺炎(9.1%;10.8%)。D-RVd组和RVd组分别有15.2%和20.6%的患者因AE导致终止治疗,外周感觉神经病变(D-RVd组5.1%;RVd组3.9%)居首位。
D-RVd组的感染发生率高于RVd组(90.9% vs 61.8%),主要体现在是前者1-2级上呼吸道感染的发生率更高。两组间3/4级感染的发生率相似(23.2% vs 21.6%),需要终止治疗的严重感染患者的比例相似(2.0% vs 2.9%)。
42例患者(42.4%)发生达雷妥尤单抗输液相关反应,多为轻度,仅6例患者(6.1%)发生3级不良反应。没有患者因IRR中止治疗。
对干细胞动员和植入的影响
D-RVd组和RVd组的中位CD34+细胞采量分别为8.2×106/kg(2.6×106-33.0×106)和9.4×106/kg(4.1×106 - 28.7×106)。D-RVd组和RVd组植入的CD34+细胞中位数量分别为4.2×106和4.8×106。
两组的造血重建指标相当;D-RVd组中性粒细胞和血小板植入的中位天数分别为12天和13天,RVd组分别为12天和12天,表明达雷妥尤单抗的引入并未影响造血功能的恢复。
小结
总之,在适合移植的NDMM患者中,诱导缓解方案在RVd基础上加用达雷妥尤单抗可提高sCR率和MRD阴性率,与常规治疗相比未增加不良反应的发生率,且对造血干细胞动员和植入无显著影响。本研究结果表明,D-RVd联合治疗有望成为适合移植的NDMM的标准诱导治疗手段。

D-RVd疗法流程图
参考文献
[1] Voorhees PM, Kaufman JL, Laubach J, et al. Daratumumab, lenalidomide, bortezomib, and dexamethasone for transplant-eligible newly diagnosed multiple myeloma: the GRIFFIN trial. Blood. 2020;136(8):936-945.
[2] Moreau P, Attal M, Hulin C, et al. Bortezomib, thalidomide, and dexamethasone with or without daratumumab before and after autologous stem-cell transplantation for newly diagnosed multiple myeloma(CASSIOPEIA): a randomised, open-label, phase 3 study [published correction appears in Lancet. 2019 Jun 14;:]. Lancet. 2019;394(10192):29-38.
本文作者:蓝鲸晓虎