腺苷 CD39-CD73-腺苷三部曲之结局
CD39分解ATP,ADP,CD73分解AMP,最后生成腺苷(ADO),腺苷结合其受体发挥作用,执行功能(健康情况下,eATP和eADO在nM水平,但是在缺氧,营养缺乏,炎症情况下,细胞死亡,可以上升至mM水平。)
腺苷受体
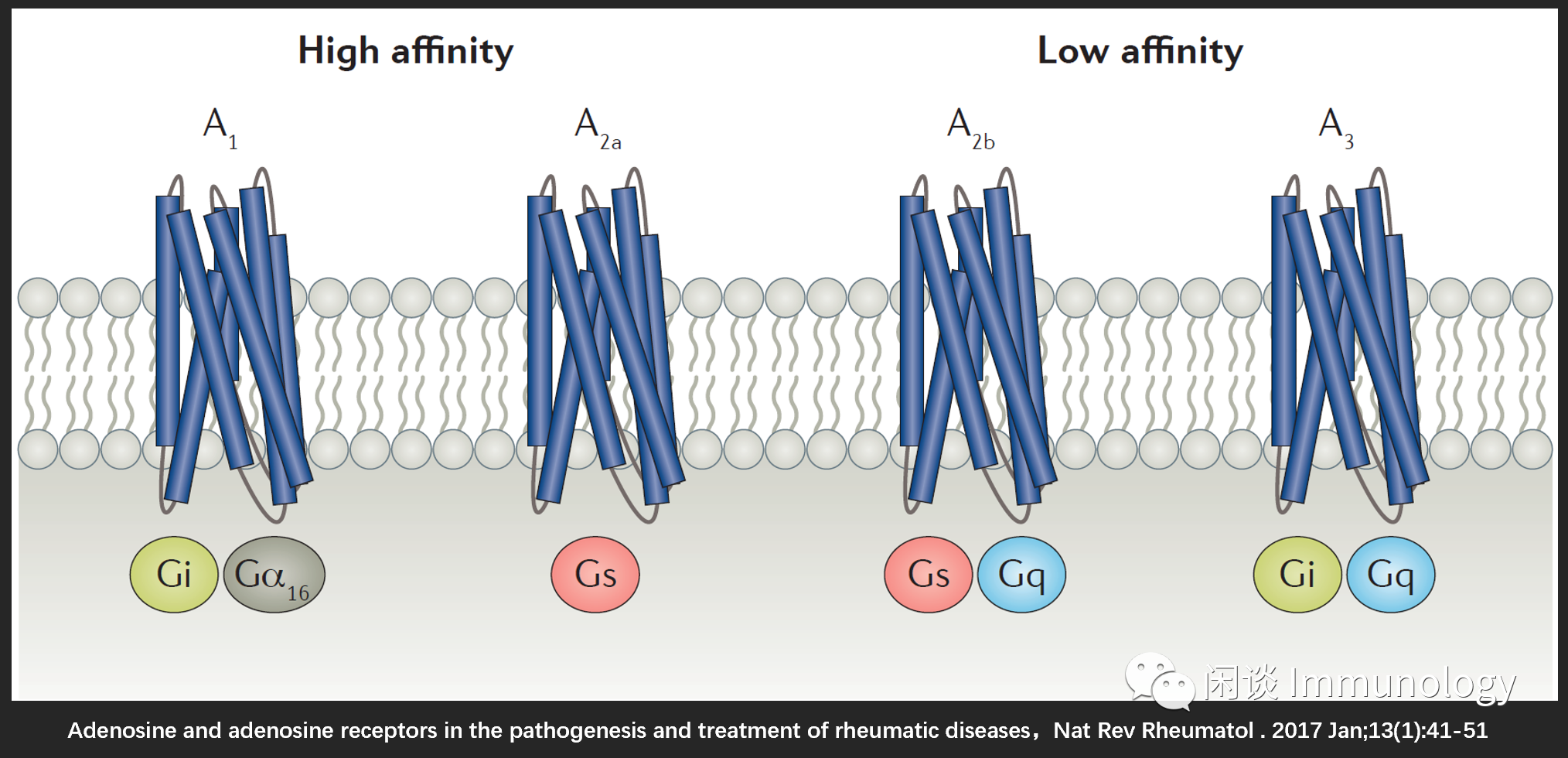
腺苷受体属于G蛋白偶联受体,A1亲和力最高,pM腺苷即可激活,A2a次之,需要nM,而A2b和A3属于低亲和力受体,需要mM的腺苷才能激活。
肿瘤微环境腺苷免疫抑制功能
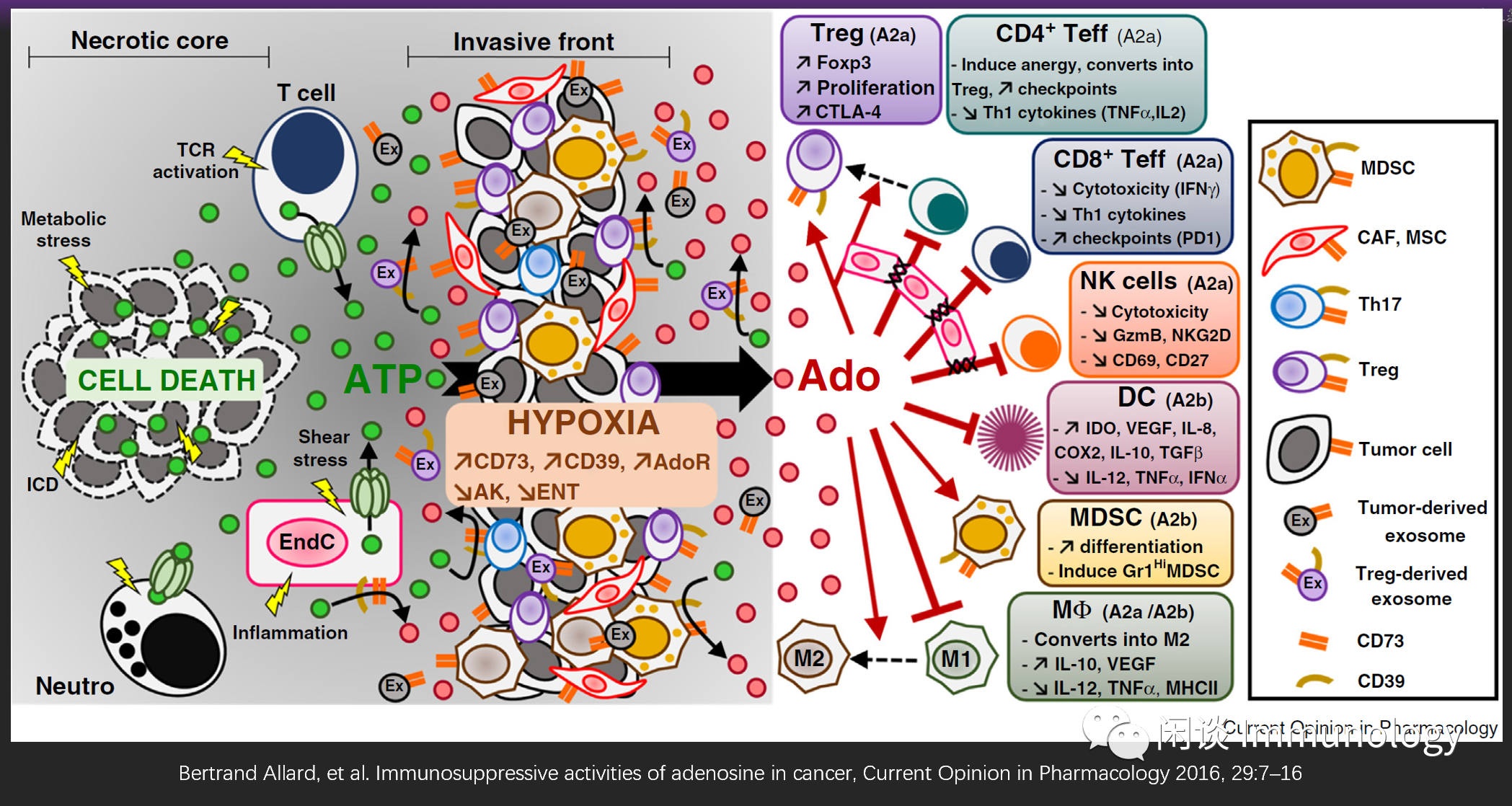
引起腺苷增加的因素
化疗,放疗等引起的细胞死亡
肿瘤微环境缺氧等
免疫抑制的具体表现
调节性T细胞(A2a)
Foxp3表达上调
增殖上调
免疫检查点CTLA-4上调
CD4+效应T细胞(A2a)
向Treg分化
免疫检查点分子上调
Th1细胞因子(TNF-&α;,IL-2)表达减少
CD8+效应T细胞(A2a)
细胞毒性下降(IFN-&γ;下降)
Th1细胞因子下降
免疫检查点分子上调
NK细胞(A2a)
细胞毒性下降
颗粒酶,NKG2D,CD69,CD27下降
树突状细胞(A2b)
IDO,VEGF,IL-8,COX2,IL-10,TGF-&β;上调
IL-12,TNF-&α;,IFN-&γ;下调
髓源性抑制细胞MDSC
向MDSC分化
Gr1Hi MDSC增加
巨噬细胞(A2a,A2b)
向M2极化
IL-10,VEGF上调
IL-12,TNF-&α;,MHCII下调
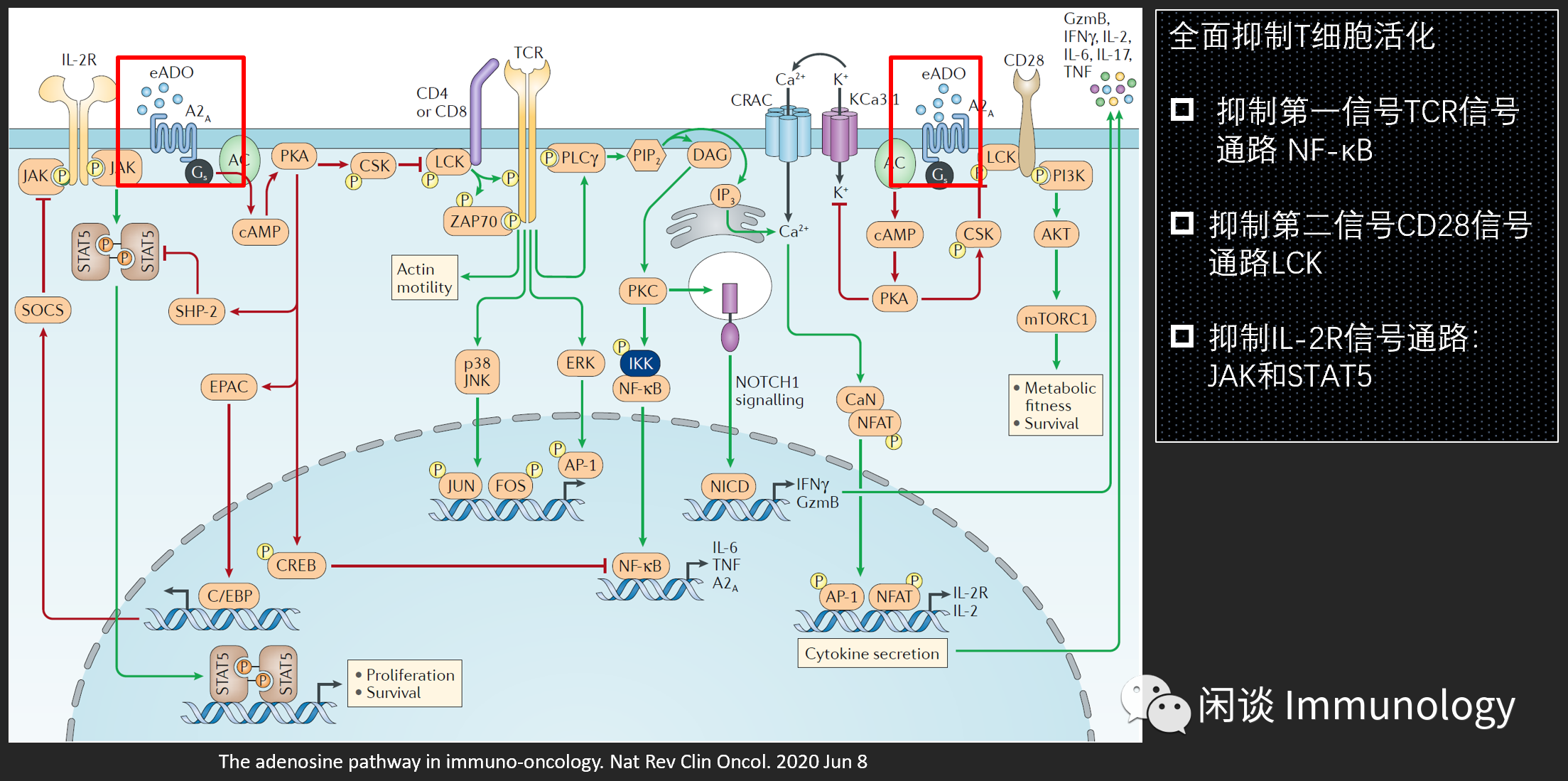
T细胞是肿瘤免疫主力军,eADO-腺苷信号通路,基本上抑制了T细胞激活的所有通路。
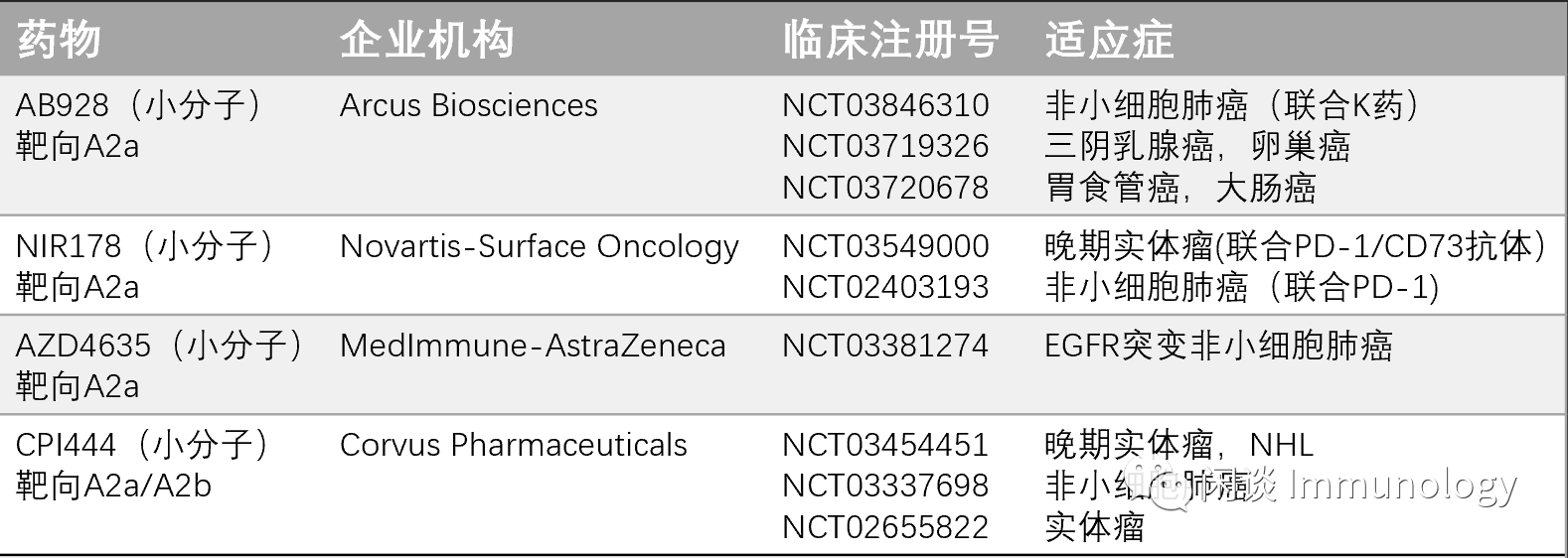
药物开发
已经有多家企业开始开发小分子抑制剂,联合PD-1抑制剂,CD73抑制剂等,治疗肿瘤。
部分药物如下:
主要参考文献
Bruce N Cronstein , Michail Sitkovsky,Adenosine and adenosine receptors in the pathogenesis and treatment of rheumatic diseases,Nat Rev Rheumatol . 2017 Jan;13(1):41-51
Allard B, Allard D, Buisseret L, Stagg J.,The adenosine pathway in immuno-oncology.Nat Rev Clin Oncol. 2020 Jun 8
Dipti Vijayan et al,Targeting immunosuppressive adenosine in cancer,Nat Rev Cancer . 2017 Nov 22;17(12):765.
Akil Hammami,et al.Targeting the adenosine pathway for cancer immunotherapy,Seminars in Immunology 42(2019) 101304
Bertrand Allard, et al.Immunosuppressive activities of adenosine in cancer,Current Opinion in Pharmacology 2016, 29:7–16
来源:闲谈 Immunology 2020-08-27