复发性卵巢癌“Chemo-free”--我们准备好了吗?
上皮性卵巢癌通常诊断时已是晚期,尽管大部分患者在完成肿瘤细胞减灭术及化疗后可以达到缓解,但是约70%的患者会出现复发。基于美国国立综合癌症网络(NCCN)指南[1],对于铂敏感复发(PSR)卵巢癌患者,标准方案是铂类为基础的联合化疗±贝伐珠单抗,随着治疗线数的增加,后续治疗的缓解率逐渐下降,无进展生存期(PFS)和总生存期(OS)逐渐缩短,大部分患者最终会转变为铂耐药复发(PRR),这类患者治疗方案以非铂类药物为主。细胞毒药物均有一定的不良反应,如骨髓抑制、恶心呕吐、周围神经毒性等,这些是患者继续使用化疗的限制因素。因此,如果能用其他方案来减少这些毒副反应,并且能达到相近甚至更好的疗效,对于复发性卵巢癌患者来说是一种很好的选择。在过去的10-15年,并没有出现能够改变临床实践的重要数据。幸运的是,随着研究的进展,这一治疗领域也有了一些喜人的数据报道。“Chemo-free”--去化疗,我们已经准备好了吗?今天我们特邀请天津市肿瘤医院王珂教授,为大家深入解读复发性卵巢癌“Chemo-free”治疗策略。

天津市医科大学肿瘤医院妇瘤科科主任
中国抗癌协会妇科肿瘤专业委员会常委
中国抗癌协会家族遗传性肿瘤协会委员
中国抗癌协会腹膜肿瘤专业委员会委员
中国临床肿瘤协会妇科肿瘤专家委员会委员
中国临床肿瘤协会热疗专业委员会委员
中国医师协会妇产科医师分会委员会委员
中华医学会妇科肿瘤分会委员
中国奖励医学会妇科肿瘤分会常委
世界华人肿瘤医师协会委员
天津市医学会妇科肿瘤分会副主委
天津市医师协会妇产科医师分会常委
天津医学会妇科内镜分会委员
天津市血管靶向学会委员
天津市肿瘤医院妇科肿瘤MDT首席专家
“Chemo-free”单药治疗数据
2014年,基于Study42研究,美国食品药物管理局(FDA)加速批准了奥拉帕利用于既往≥3线化疗的BRCA突变(BRCAm)上皮性卵巢癌。SOLO3[2](NCT00628251)是一项验证性的Ⅲ期研究,旨在既往接受过≥2线含铂化疗的胚系突变(gBRCAm)的PSR卵巢癌患者中,评估奥拉帕利对比医生选择的非铂类化疗的疗效。奥拉帕利组客观缓解率(ORR)显著高于化疗组(图1)。与化疗组相比,奥拉帕利组BICR评估的PFS显著延长,两组mPFS分别为13.4个月和9.2 个月(HR 0.62,P=0.013)。SOLO3研究,为既往至少接受过2线含铂化疗BRCAm的PSR卵巢癌患者提供了一种“Chemo-free”的治疗选择。
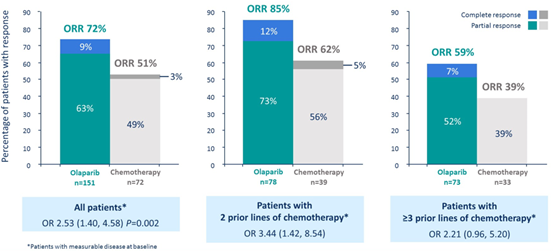
CLIO[3](NCT02822157) 是一项随机Ⅲ期研究,旨在评估奥拉帕利与医生选择的化疗方案治疗复发性卵巢癌患者的疗效,分为铂敏感卵巢癌(PSOC)队列和铂耐药卵巢癌(PROC)队列(图2)。PSOC队列入组的是BRCA野生型(BRCAwt)患者,PROC队列包括BRCAm和BRCAwt患者。
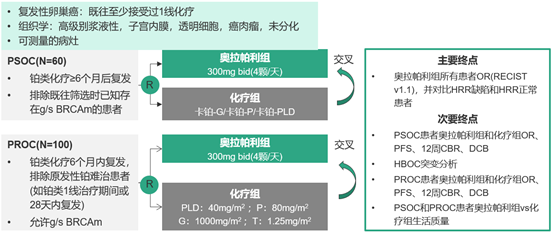
图2. CLIO研究设计。g/s BRCAm :胚系或体系BRCA突变;bid:一天两次;PLD:聚乙二醇的脂质体阿霉素;P:紫杉醇;G:吉西他滨;T:拓扑替康;OR:客观缓解;HRR:同源重组修复;PFS:无进展生存;CBR:临床获益率;DCB:临床获益持续时间;RECIST:实体瘤疗效评估标准;HBOC,遗传性乳腺癌和卵巢癌综合征
2019年美国临床肿瘤学会(ASCO)会议上公布了PROC队列结果[4],奥拉帕利组(OLA)和化疗组(CT)的ORR分别为18%和6%,BRCAm患者两组的ORR分别为36%和0%, BRCAwt患者两组的ORR分别为13%和6% 。OLA组和CT组PFS无显著差异,mPFS分别为2.9个月和3.4个月,HR=1.18(95%CI 0.75-1.87;P=0.48)。2020年美国妇科肿瘤学会(SGO)年会上公布了PSOC队列的结果[3],OLA组与CT组ORR分别为40%和60%(P=0.12)。疾病控制率(DCR)分别为80%和85%。两组PFS相似(OLA和CT组的mPFS分别为6.4个月和8.5个月;HR=1.11,95% CI 0.60-2.04;P=0.7)。OS相似(mOS分别为23.9和27.7个月;HR=1.01,95% CI 0.40-2.51)。对于BRCAwt的PSR患者的治疗,奥拉帕利单药组与医生选择的标准化疗组的PFS和OS均无统计学差异,两组疗效相似。两组不良事件(AE)与既往研究相似。
QUADRA[5](NCT02354586)是一项单臂Ⅱ期研究,旨在评估尼拉帕利用于复发性卵巢癌后线治疗的疗效和安全性,无论患者的铂类敏感状态和生物标志物状态。研究达到主要终点,47例既往接受过3或4线抗肿瘤治疗、同源重组缺陷(HRD)阳性、对最近一次含铂方案敏感、既往未接受过PARP抑制剂(PARPi)治疗的患者中(主要疗效人群),ORR为28%,mPFS为5.5个月,中位缓解持续时间(mDoR)为9.2个月,DCR为68%。387例疗效可评估人群和456例符合方案人群的ORR分别为10%和8%。既定的探索性分析,根据患者的生物标志物状态和铂类敏感状态评估的治疗结局,总结见表1:
表1. 根据生物标志物状态和铂类敏感状态评估的治疗结局
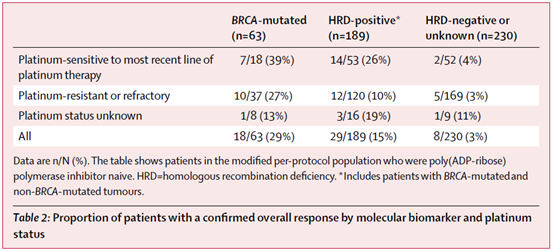
QUADRA 研究在各个临床亚组和生物标志物亚组中均观察到临床获益,基于这一研究结果,FDA于2019年批准尼拉帕利用于既往≥3线化疗后复发的HRD阳性的晚期卵巢癌治疗[6]。
“Chemo-free”联合治疗数据
PARPi+抗血管生成药物:抗血管生成药物引起的缺氧可能会增加DNA损伤和遗传不稳定,导致同源重组缺陷,从而增加PARPi的敏感性。
AVANOVA2[7](NCT02354131) 是一项随机Ⅱ期研究,入组的是PSR卵巢癌患者,随机分为两组,一组接受尼拉帕利单药,另一组接受尼拉帕利联合贝伐珠单抗治疗。主要研究终点为研究者评估的PFS,相比于尼拉帕利单药,联合方案的PFS显著延长,mPFS分别为11.9个月和5.5个月,矫正分层因素后的HR为0.35(95%CI 0.21–0.57, P<0.0001)。在BRCAm患者(n=33)中,两组mPFS分别为14.4个月和9.0个月(HR 0.49,95% CI 0.21-1.15);在非BRCAm患者(n=64)中,两组的mPFS分别为11.3个月和4.2个月(HR 0.32,95% CI 0.17-0.58])。联合治疗并未影响患者的生活质量,患者报告的治疗结局两组相似。该研究中,在既往使用过贝伐珠单抗的人群中,相比于单药组,联合方案的PFS并没有延长,在这种情况下,换用其他抗血管生成药物(如西地尼布)是否能延长PFS还需要进一步探索。AVANONA2研究没有与标准含铂化疗方案对比,因此,这项研究还有待于进一步验证。
GY004[8](NCT02446600) 是奥拉帕利单药或联合西地尼布对比标准含铂化疗治疗PSR卵巢癌的Ⅲ期研究(图3)。与标准化疗组(SOC)相比,西地尼布+奥拉帕利组(C+O)的PFS风险比为0.856(95% CI 0.66-1.11,P=0.08);与SOC组相比,单药奥拉帕利组(O)的PFS风险比为1.20(95% CI 0.93-1.54)。三组mPFS分别为10.3个月(SOC), 8.2个月(O)和10.4个月(C+O)。ORR分别为71.3%(SOC), 52.4%(O)和 69.4%(C+O)。BRCA1/2突变者PARPi占优[三组mPFS分别为10.5个月(SOC),12.7个月(O)和18.0个月(C+O)],非BRCA1/2突变者化疗占优[三组mPFS分别为9.7个月(SOC),6.6个月(O)和8.9个月(C+O)]。血液学AE在SOC组发生率较高,非血液学AE在C+O组发生率较高。这是第一个比较非铂类治疗方案与标准含铂化疗用于PSR卵巢癌的Ⅲ期试验。在PSR卵巢癌患者中,西地尼布+奥拉帕利显示出与标准含铂化疗相似的活性。

PARPi+免疫检查点抑制剂:免疫检查点抑制剂单药用于卵巢癌疗效有限,临床前研究表明,DNA损伤会促进新抗原的表达,而PARPi可以导致DNA损伤的增加,可能会产生更大的突变负荷并扩大新抗原的表达,从而增加肿瘤的免疫识别。因此,免疫检查点抑制剂联合PARPi是一种有希望的治疗方案。
MEDIOLA[9](NCT02734004)是一项单臂Ⅱ期研究,在卵巢癌队列中,研究者探讨了奥拉帕利联合度伐利尤单抗治疗gBRCA1/2突变PSR卵巢癌(既往至少接受过一线含铂化疗)的疗效。28周的DCR为65.6%,ORR为71.9%,其中有7例达到完全缓解(CR)。总人群的mPFS为11.1个月,mDoR为10.2个月。最常见的≥3级AE是贫血(17.6%),脂肪酶升高(11.8%),中性粒细胞减少(8.8%)和淋巴细胞减少(8.8%)。
TOPACIO/KEYNOTE-162[10]( NCT 02657889)是一项单臂Ⅰ/Ⅱ期研究,旨在评估尼拉帕利联合帕博利珠单抗用于PRR卵巢癌的疗效和安全性。在60例可以进行疗效评价的患者中,ORR为18%,DCR为65%,其中3例(5%)CR, 8 例(13%)部分缓解(PR), 28例(47%)疾病稳定(SD)。最常见的治疗相关AE为疲劳(53%),恶心(42%),贫血(36%)和便秘(36%)。
最近发布的《PARP抑制剂在卵巢癌中的应用:ASCO指南》[11],推荐PARPi(奥拉帕利、尼拉帕利、卢卡帕利)可用于治疗既往未使用过PARPi、胚系或体系BRCA1/2突变的复发性卵巢癌;PARPi单药可用于治疗既往未使用PARPi、Myriad myChoice CDx检测提示基因组不稳定、含铂化疗6个月以上复发的上皮性卵巢癌。由于目前报道的很多是Ⅱ期研究,在现有数据情况下,ASCO指南不推荐PARPi用于治疗BRCAwt或PRR卵巢癌患者,也不推荐PARPi与化疗、其他靶向药物或免疫治疗药物联合使用。鼓励患者参加临床试验。
对于复发性卵巢癌,治疗方法已开始从传统的细胞毒化疗转向新型的,对患者更友好,副作用更少的药物。临床医生都想为患者选择一种疗效好、不良反应少的双赢方案。随着chemo-free相关研究的陆续报道,这些结果会如何影响医生的治疗决策?去化疗,但不是放弃化疗,对于既往化疗副反应重,药物过敏、出现交叉耐药,依从性差的复发性卵巢癌患者,PARPi单药,以及联合方案为我们提供了更多的治疗选择。基于目前的研究数据,临床上,我们还面临着许多问题,如:PSR卵巢癌最佳的治疗顺序是什么?PARPi是应该用于化疗之后还是相反?我们可以用非化疗方案来防止化疗的不良事件,又不影响患者的OS吗?这些问题,还有待于未来的临床研究和临床实践来回答。期待未来我们能为卵巢癌患者做出更好的治疗选择,带给她们更多的生存获益。
参考文献
[1] NCCN Guidelines Version 1.2019 Epithelial Ovarian Cancer/Fallopian Tube Cancer/Primary Peritoneal Cancer.
[2] Penson R T, Valencia R V, Cibula D, et al. Olaparib versus nonplatinum chemotherapy in patients with platinum-sensitive relapsed ovarian cancer and a germline BRCA1/2 mutation(SOLO3): a randomized phase III trial[J]. Journal of Clinical Oncology, 2020, 38(11): 1164.
[3] Loverix L, Vanderstichele A, Olbrecht S, et al. Randomized phase II CLIO study on olaparib monotherapy versus chemotherapy in platinum-sensitive recurrent ovarian cancer[C]//SGO 2020 Annual Meeting on Women's Cancer. SGO, 2020.
[4] Vanderstichele A, Van Nieuwenhuysen E, Han S, et al. Randomized phase II CLIO study on olaparib monotherapy versus chemotherapy in platinum-resistant ovarian cancer[J]. 2019.
[5] Moore K N, Secord A A, Geller M A, et al. Niraparib monotherapy for late-line treatment of ovarian cancer(QUADRA): a multicentre, open-label, single-arm, phase 2 trial[J]. The Lancet Oncology, 2019, 20(5): 636-648.
[6] https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-niraparib-hrd-positive-advanced-ovarian-cancer.
[7] Mirza M R, Lundqvist E Å, Birrer M J, et al. Niraparib plus bevacizumab versus niraparib alone for platinum-sensitive recurrent ovarian cancer(NSGO-AVANOVA2/ENGOT-ov24): a randomised, phase 2, superiority trial[J]. The Lancet Oncology, 2019, 20(10): 1409-1419.
[8]https://www.clinicaltrials.gov/ct2/show/NCT02446600?cond=NCT02446600&draw=2&rank=1
[9] Drew Y, Kaufman B, Banerjee S, et al. Phase II study of olaparib + durvalumab(MEDIOLA): Updated results in germline BRCA-mutated platinum-sensitive relapsed(PSR) ovarian cancer(OC)[J]. Annals of Oncology, 2019, 30: v485-v486.
[10] Konstantinopoulos P A, Waggoner S, Vidal G A, et al. Single-arm phases 1 and 2 trial of niraparib in combination with pembrolizumab in patients with recurrent platinum-resistant ovarian carcinoma[J]. JAMA oncology, 2019, 5(8): 1141-1149.
[11] Tew W P, Lacchetti C, Ellis A, et al. PARP Inhibitors in the Management of Ovarian Cancer: ASCO Guideline[J]. Journal of Clinical Oncology, 2020: JCO. 20.01924.