【卡瑞利珠单抗·CameL研究者说】董晓荣教授:卡瑞利珠单抗联合化疗安全有效,必将改变我国肺癌临床实践

Q:首先请您介绍一下,目前在我国,驱动基因阴性晚期非鳞NSCLC的治疗现状如何?
董晓荣教授:肺癌是我国乃至全球发病率及相关死亡率居于首位的恶性肿瘤,主要分为小细胞肺癌(SCLC)和非小细胞肺癌(NSCLC),其中NSCLC比例高达85%,涉及人群众多。
NSCLC的治疗需要基于基因检测结果选择治疗方案。以Ⅳ期NSCLC为例,若驱动基因突变阳性,则予以相应的靶向药物,例如EGFR、TKI、ALK-TKI及ROS-1等相应靶点的靶向药物等,若驱动基因突变阴性,首选治疗方式可考虑传统的化疗联合抗血管生成治疗以及现目前正在探索且疗效前景较好的免疫治疗。
依据KEYNOTE-024研究结果,对于晚期NSCLC驱动基因阴性且PD-L1表达大于等于50%的高表达人群,一线治疗可予以抗PD-1/PD-L1抗体的单药治疗。对于肿瘤负荷较大、患者体力状态评分较好以及非高表达人群可考虑免疫联合化疗的模式。选用免疫联合化疗模式,首先要注意区分NSCLC的组织学类型,包括鳞癌及非鳞癌。对于非鳞癌NSCLC的治疗,目前证据级别较高的是抗PD-1抗体联合培美曲塞及铂类的联合治疗4个周期后,序贯免疫检查点抑制剂联合培美曲塞的维持治疗,直至疾病进展或用药时间达2年。此种治疗模式与以往的单纯化疗、化疗联合抗血管生成等治疗模式相比,显现出很好的应用前景。对于非鳞NSCLC的治疗,IMpower150研究中采取的免疫+抗血管生成+化疗的四药联合模式亦值得关注。
总之,无论是抗PD-1/PD-L1抗体的单药治疗,还是免疫联合化疗或是免疫联合抗血管生成治疗,免疫治疗的引入都给肿瘤患者带来了长期生存的希望及治愈的可能。
Q:作为CameL研究的PI之一,请您介绍下本中心研究开展的具体情况?结果如何?
董晓荣教授:CameL研究是一项开放标签、随机、多中心Ⅲ期研究,评估了自主创新免疫检查点抑制剂卡瑞利珠单抗联合或不联合化疗方案对比单纯化疗,治疗驱动基因阴性的晚期非鳞NSCLC患者的疗效和安全性。华中科技大学同济医学院附属协和医院作为CameL研究的分中心之一,于2018年1月完成首例患者入组。观察入组患者可知,卡瑞利珠单抗疗效及安全性均良好。印象最为深刻的病例是首例入组患者,其为伴有肝转移的Ⅳ期男性患者,驱动基因突变阴性且PD-L1表达阳性(PD-L1表达≧1),入组CameL研究后予以卡瑞利珠单抗联合培美曲塞及卡铂治疗,病情稳定后序贯卡瑞利珠单抗联合培美曲塞的维持治疗。随访至今(2020年5月),获益时间2年余且仍病情稳定,同时毒副作用可控。据此来看,卡瑞利珠单抗联合化疗的治疗模式给患者带来了长期的生存获益。
Q:对于卡瑞利珠单抗在该研究中的安全性和有效性表现,您有何评价?该研究结果对于临床实践有何影响?
董晓荣教授:从CameL研究结果来看,卡瑞利珠单抗的安全性较为良好,主要不良反应包括血液学毒性,考虑与联合化疗相关。此外可观察到卡瑞利珠单抗常见的反应性皮肤毛细血管增生症(RCCEP),但安全性总体而言良好,3级、4级以上的毒副反应小于3%,在安全和可控范围内。
有效性方面,卡瑞利珠单抗联合化疗组的ORR达60%,对比化疗组的39%,有显著提升。联合治疗组的中位PFS达到11.3个月,疾病进展风险下降39%。其次,卡瑞利珠单抗联合化疗组与单纯化疗组的缓解持续时间(DoR)分别为17.9个月与9.9个月,前者明显延长。OS数据目前尚未成熟,但两条曲线分开提示OS亦有获益的趋势。
从研究结果来看,无论是ORR、PFS还是DoR,卡瑞利珠单抗联合治疗组均优于单纯化疗组,提示晚期非鳞NSCLC患者予以卡瑞利珠单抗联合培美曲塞及铂类治疗优于传统标准培美曲赛联合铂类治疗,获益更多且安全性良好。以上便是CameL研究所得到的结论,相信该研究会在未来的治疗中改变临床实践,免疫联合化疗将会成为晚期非鳞NSCLC的一种新治疗模式。
Q:请您谈谈,未来晚期非鳞NSCLC治疗的发展趋势如何?您觉得卡瑞利珠单抗在肺癌领域的探索方向有哪些?
董晓荣教授:CameL研究证实了免疫联合化疗方案对晚期非鳞NSCLC患者的优势,其中,免疫联合抗血管生成药物、联合放疗均在机制上有协同作用,未来在NSCLC领域还有更多免疫联合治疗模式值得探索与期待。既往研究还显示,对于晚期NSCLC患者在经过免疫联合化疗治疗达到DCR后,再对原发灶或转移灶予以放疗,可进一步延长患者的OS,此类联合方案均值得未来进一步探索。除了联合治疗这一趋势外,未来免疫治疗还将逐步前移,甚至应用至辅助及新辅助等NSCLC治疗。卡瑞利珠单抗一线治疗驱动基因阴性晚期转移性NSCLC的CameL研究是免疫联合治疗的一次成功探索,未来,卡瑞利珠单抗在治疗更前线、更多联合治疗模式领域都还有很长的路要走,相信免疫治疗必将能使更多患者得到更多生存获益。
病例分享
华中科技大学同济医学院附属协和医院 童凡

病史概述
胡xx,男性,59,长期吸烟史,>600年支。
咳嗽1月,发现肺占位6天,于2017年12月12日首次入我院。
现病史:患者2017年11月无明显诱因出现阵发性咳嗽,就诊于外院胸部CT示:1.右肺下叶占位,考虑肿瘤性病变;2.两肺散在小结节;纵隔及右肺门淋巴结肿大。遂入我院。发病来体力体重未下降。
既往史:有高血压史,口服苯磺酸氨氯地平,血压控制可。
入院检查
【体格检查】
T:36.4℃,P:82bpm,
R:20次/分,BP:120/73mmHg。
神志清,精神可,心率:82bpm,律齐,未闻及杂音。两肺呼吸音略粗,未闻及明显干湿罗音,腹软,无压痛,肝脾肋下未触及。双下肢不肿。
【辅助检查】
血常规:正常;
肝肾功能:正常;
肿瘤标记物:癌胚抗原 10.05↑ng/mL
心脏彩超:超声心动图检查未见明显异常;
肺功能:轻度阻塞性通气功能障碍;
影像学基线检查:胸部CT,2018年1月3日(图1)。
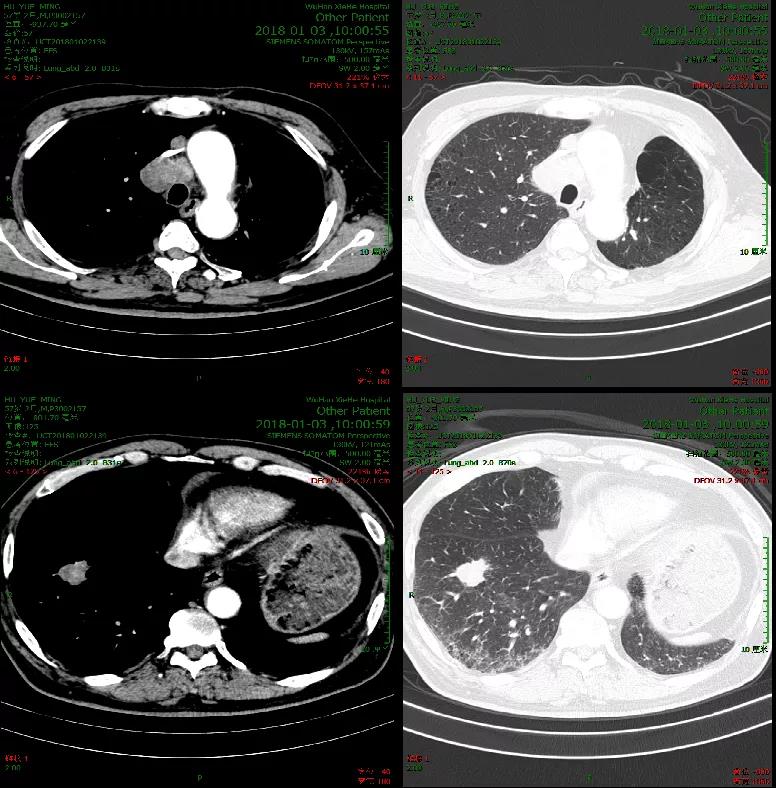
【病理检查】
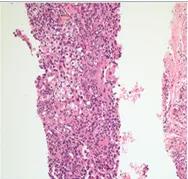
CT导向性经皮右下方肿块穿刺活检:浸润性腺癌(图2)。
免疫组化:
PCK(+),EMA(+),CK7(+),Vim(-),Ki67(+,70%),CK5/6I(-),P40(-),P(-),NapsinA(-),TTF-1(-),CD56(-),Syn(-),EGFR(+),ALK(D5F3)(-)。
基因检查:
分子检测结果:
EGFR基因未检测到L858R、19外显子缺失突变;ALK未见融合。
PD-L1蛋白表达≥1%。
诊断
右下肺低分化腺癌。
分期:cT1N3M1b,肝Ⅶ段转移。
分子诊断:EGFR基因(-),ALK(D5F3)(-),PD-L1≥1%。
ECOG PS评分:1分。
一线治疗方案
卡瑞利珠单抗200 mg+培美曲塞500 mg/m2+卡铂(AUC=5),3周1次,化疗4周期。
结束后给予卡瑞利珠单抗 200mg+培美曲塞 500mg/m2维持治疗,3周1次,于2020年1月维持治疗结束。
疗效评价
2018年3月第一次疗效评估即达到PR,2018年6月开始行维持治疗,至2020年1月维持治疗结束。2020年5月随访结果显示患者仍然保持病情稳定,PFS已达28个月(图3)。
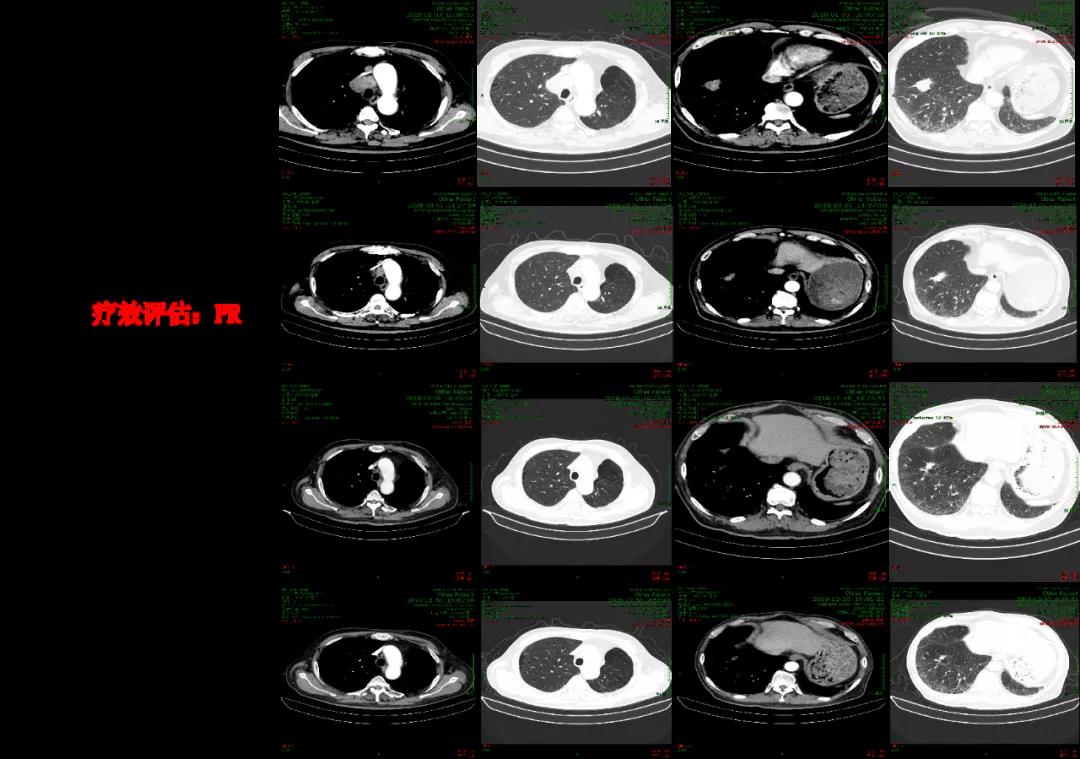
不良反应
治疗过程中发生的主要不良反应有贫血、中性粒细胞计数降低、肝功能损伤,严重程度为1/2级,采取对症治疗后即可有效控制。
诊治体会与思考
本例患者为59岁男性,诊断为右下肺低分化腺癌(EGFR和ALK基因阴性,PD-L1阳性)。患者自愿入组CameL研究后,进入治疗组接受“卡瑞利珠单抗+培美曲塞+卡铂”一线治疗,治疗仅1周期即达到PR,此后接受“卡瑞利珠单抗+培美曲塞”维持治疗,PFS达28个月,目前仍保持病情稳定,持续随访中。总的来说,卡瑞利珠单抗一线联合化疗治疗野生型晚期肺腺癌疗效显著,可实现生存期显著延长,且安全耐受性好,患者生活质量显著提高。
最新消息:
2020年6月19日,卡瑞利珠单抗正式获得国家药品监督管理局(NMPA)批准用于肺癌治疗,成为中国首个获批肺癌适应证的国产PD-1抑制剂!获批的具体适应证为“卡瑞利珠单抗联合培美曲塞和卡铂用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的、不可手术切除的局部晚期或转移性非鳞状非小细胞肺癌(NSCLC)的一线治疗”,该获批正是基于CameL研究的结果。
此前,基于CameL研究结果,卡瑞利珠单抗联合培美曲塞和铂类方案已被写入《2020 CSCO非小细胞肺癌诊疗指南》,作为IV期无驱动基因、非鳞NSCLC一线治疗方案,1A类证据,II级推荐。
卡瑞利珠单抗二线治疗晚期NSCLC的Ⅱ期伞形研究(ORR达18.5%,OS达19.4个月)以及卡瑞利珠单抗联合阿帕替尼二线治疗晚期NSCLC的Ⅱ期研究(ORR达30.8%,PFS达5.9个月)也写入本次指南二线治疗的注释部分。