TACE联合索拉非尼序贯瑞戈非尼,晚期肝癌患者持久获益
肝癌手术后的高复发率和转移率是影响肝癌患者长期生存的主要问题。因此,复发转移后的全程管理尤为重要。系统治疗贯穿肝癌治疗全程,必不可少,靶向药物目前仍是中晚期肝癌治疗的基石。本例肝癌患者手术后短期出现复发转移,肿瘤分化差,恶性程度高。后续治疗中针对肝脏局部采用经导管动脉栓塞化疗(TACE)减轻肿瘤负荷,靶向药物一线索拉非尼序贯二线瑞戈非尼控制全身病情,取得了很好的效果。
病例介绍
基本信息
患者男性,51,主因“肝癌术后17个月,复发1年余”入院。既往慢性乙型病毒性肝炎病史10年,其母患有乙肝,父亲逝于胃癌,其弟乙肝病史10年,淋巴瘤6年已治愈。17个月前体检时发现AFP 40u/L,肝右叶占位。就诊外院检查提示肝右叶肝癌可能,肝硬化,脾大,侧枝循环形成。于2018年12月4日行腹腔镜探查+肝癌切除+门静脉化疗泵置入术,术中所见:肝脏呈弥漫性结节性肝硬化改变,肝右前叶(第Ⅵ段)有直径约4cm和1cm两个圆形质硬肿块,腹腔内少量淡黄色腹水,腹腔未发现肿大淋巴结及癌转移结节。术后病理示:肝细胞性肝癌Edmonson-Steiner分级Ⅲ~Ⅳ级:未见明确的脉管内癌栓及神经侵犯。免疫组化:A.AFP(-),Arginase-1(-),CD10(+),CD34(血窦+)、CK19(-):CK7(-)、Glypicn3(-)、HBcAg(-),HBsAg(-),Hepatocyte(-),Ki67(约55%+)。术后恢复好,该院行门静脉化疗2次。
入院后诊断:原发性肝癌术后,pT2N0M0,Ⅱa期,乙型病毒性肝炎,肝硬化。
肝癌术后2个月余复发转移,局部治疗联合索拉非尼一线治疗
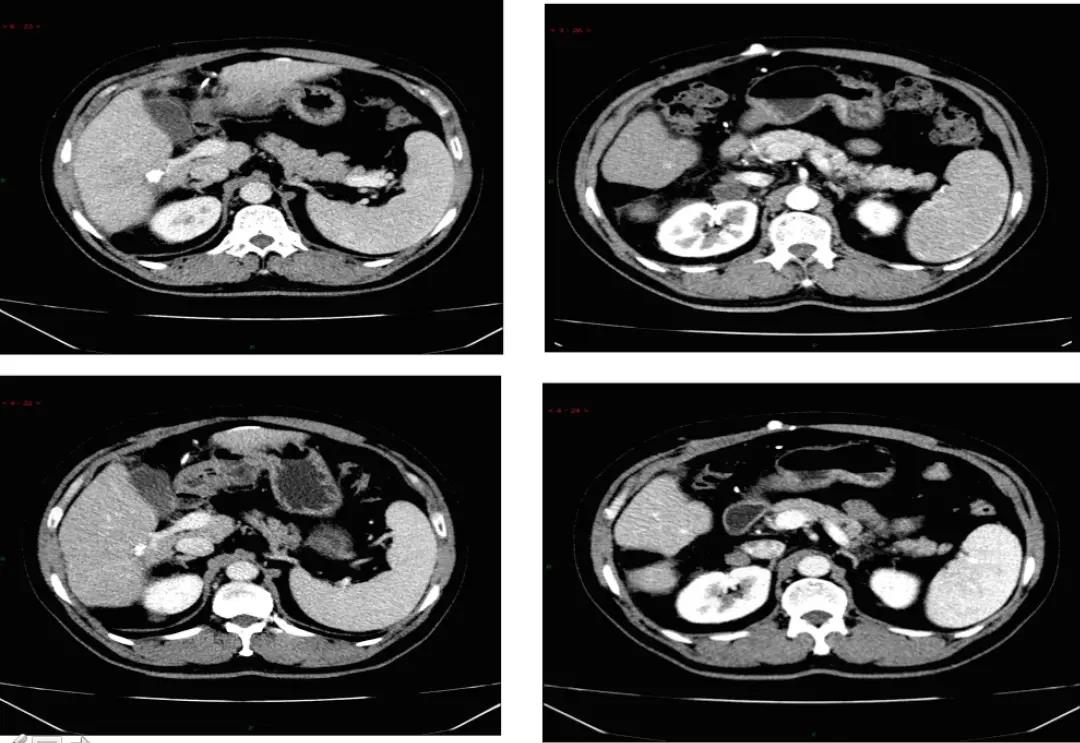
2019年2月25日随访发现肝内多发病灶复发,右上腹腹膜后淋巴结转移。MDT讨论后认为没有手术指征,分别于2019年2月27日及3月24日给予“TACE+经导管动脉内药物灌注术(TAI)”2次,术中造影提示肝肿块多发,血供丰富,行动脉灌注栓塞治疗,碘油10ml沉积好,同时动脉灌注奥沙利铂+氟尿嘧啶,为防止乙肝病毒复燃给予抗恩替卡韦规律抗病毒治疗,2程治疗后复查肝内病灶碘油沉积好,明显缩小好转,部分病灶消失,但监测到右上腹腹膜后淋巴结进展(图1)。因此于2019年3月28日患者开始口服索拉非尼片400mg BID。不良反应包括皮肤反应2级,伴疼痛、红肿,轻度乏力,纳差,对症处理可缓解,索拉非尼未减量。复诊评估疗效:疾病稳定(SD)。ECOG评分:0~1分。

6个月后疾病进展,二线治疗更换瑞戈非尼
2019年9月21日患者出现乏力,纳差加重,体力下降。复查CT发现肝内病灶稳定,但右侧腹膜后淋巴结增大。疗效评价:疾病进展(PD;图2)。ECOG评分:1分。肝功能良好。2019年9月24日更换为口服瑞戈非尼片160mg QD,服3周停1周,4周为1周期。不良反应包括:胃肠道刺激,恶心,纳差,偶有呕吐,肌肉疼痛,乏力,皮肤粘膜反应,高血压轻到中度,给予硝苯地平缓释片控制血压,吗丁啉促进胃动力,奥美拉唑口服保护胃黏膜,间断使用芬必得控制肌肉疼痛等对症处理措施。耐受不好时偶有自行减量为120mg,但非连续发生。2019年11月19日,复查肝内病灶稳定,腹膜后淋巴结稳定。2020年2月5日,复查肝病灶稳定,腹膜后淋巴结缩小,疗效评价为部分缓解(PR;图3)。
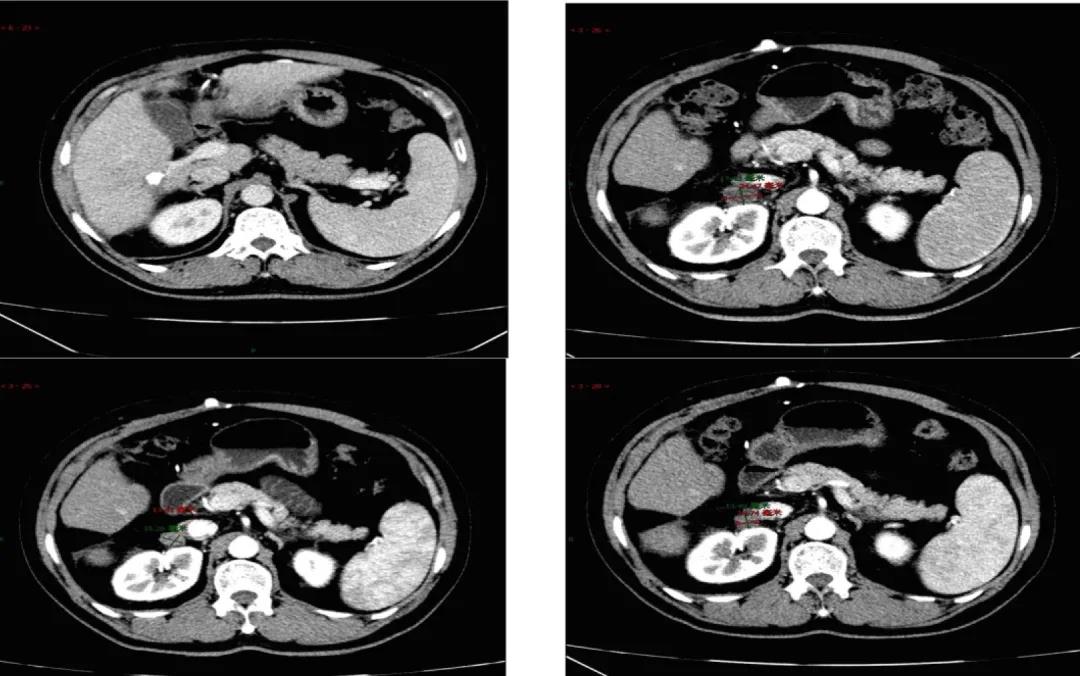
局部新发病灶,予局部处理
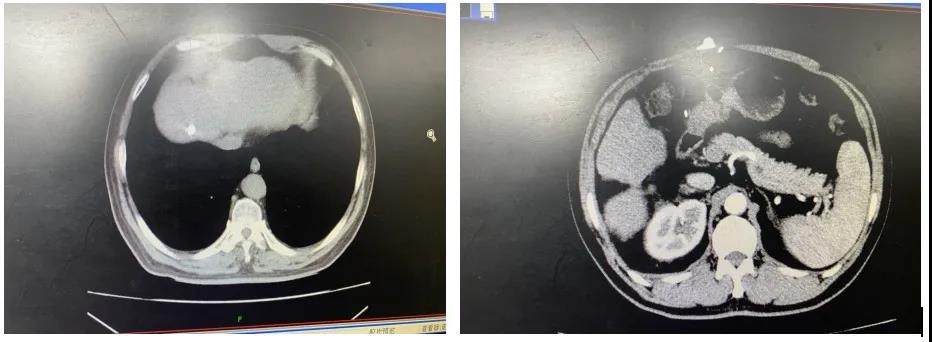
2020年5月11日患者出现乏力,纳差。复查CT发现:右下肺微结节;肝硬化、脾大;右肾高密度囊肿表现;肝右叶异常强化灶,新发转移病灶(图4),提示局部进展。局部采取TACE治疗,继续口服瑞戈非尼。2020年6月6日复查CT(图5):右下肺微结节未见明显改变;肝硬化、脾大;右肾高密度囊肿表现;肝右叶顶部新增病灶治疗后碘油栓塞良好,病灶控制,余复查稳定。继续口服瑞戈非尼控制病情。八月份复查MRI,病灶稳定,体力良好。继续口服瑞戈非尼治疗。


惠双
主任医师、医学硕士
南阳市中心医院肿瘤科主任医师、医学硕士
南阳市中心医院内科支部书记
中国抗癌协会肿瘤微创专业委员会青年委员
中华医学会会员
河南省医学会放疗专业委员会青年委员
河南省抗癌协会化疗专业委员会委员
河南省生物免疫治疗委员会青年委员
河南省老年学会肿瘤治疗委员会委员
河南省抗癌协会食管癌专委会常委
河南省抗癌协会肿瘤姑息治疗委员会委员
南阳市抗癌协会肿瘤治疗委员会常务理事
南阳市医学会肿瘤专业委员会常委兼秘书
南阳市医学会肿瘤质控中心秘书
病例点评

李捷
医学博士、硕士生导师
郑州大学第一附属医院 郑东院区肝胆胰外二科/肝脏移植科 主任
中华医学会器官移植分会青年委员、基础研究学组委员
河南省医学会普通外科委员会秘书
河南省医学会肿瘤委员会委员
中国医师协会器官移植医师分会第一届活体器官移植专业委员会委员
中国医师协会微无创医学专业委员会胰腺学组委员
担任《中华细胞与干细胞杂志》第二届编辑委员会委员
专家点评
患者乙肝、肝硬化,查体发现肝占位性病变,手术切除2枚结节。术后病理提示肝细胞癌Edmonson-Steiner分级Ⅲ~Ⅳ级。癌细胞分化程度差,恶性程度高。术后不足3个月时间即出现肝脏多发病灶同时右腹膜后淋巴结增大。此时根据《原发性肝癌诊疗规范(2019年版)》[1],对于Ⅲb期患者建议系统治疗(索拉非尼、仑伐替尼)、TACE、放疗。TACE治疗肝癌主要是基于肝癌和正常肝组织血供的差异,即95%~99%的肝癌血供来自肝动脉,而正常肝组织血供的70%~75%来自门静脉,肝动脉血供仅占20%~25%。与放疗相比,TACE能有效阻断肝癌的动脉供血,同时持续释放高浓度的化疗药物打击肿瘤,使其缺血坏死并缩小,在减少肝脏局部肿瘤负荷的同时可以尽量减少对正常肝组织的损伤。循证医学证据业已表明TACE能有效控制肝癌生长,明显延长患者生存期,使肝癌患者获益,已成为不能手术切除的中晚期或术后复发肝癌患者有效的治疗方法。TACE治疗后会导致肿瘤细胞及周围组织缺氧,进而促进新生血管形成,使得肿瘤易于复发、转移。而抗血管生成靶向药物可能会降低TACE术后VEGFR的水平,从而在治疗上达到与TACE互补的作用。
患者在6个月索拉非尼治疗后出现了疾病进展。肿瘤细胞在药物治疗压力应激下,可以通过重建血运、增强侵袭性及转移性等生物学特性的改变导致疾病进展。NCCN指南[2]及CSCO指南[3]均以Ⅰ类推荐瑞戈非尼为晚期肝癌二线治疗。推荐的循证学依据是国际、多中心、随机、双盲,Ⅲ期RESORCE研究[4]。在RESORCE研究中,瑞戈非尼二线治疗为患者带来显著的总生存(OS)获益,总体人群中,瑞戈非尼组与安慰剂组的中位OS分别为10.6月vs 7.8月,风险比为0.63,这意味着与安慰剂组相比,瑞戈非尼组死亡风险降低了37%。后续探索性分析显示[5],一线索拉非尼序贯二线瑞戈非尼全程治疗模式下患者中位OS长达26.0个月,而对照组仅为19.2个月。该研究中156例来自中国(包括大陆及台湾地区),而我国患者亚组分析数据与总体结果保持一致。一线索拉非尼序贯二线瑞戈非尼的超长OS已在韩国、日本、西班牙等的多项真实世界研究中得到过验证。此外,针对肝癌二线药物的研究还包括 REACH-2研究[6],对比了二线雷莫芦单抗+最佳支持治疗 vs安慰剂+最佳支持治疗,中位OS分别为8.5个月和7.3个月;CELESTIAL研究[7]对比了卡博替尼 vs安慰剂,中位OS分别为10.2个月和8.0个月。RESORCE研究中瑞戈非尼组的OS数值是3项研究中最长的。
免疫治疗近年来不断取得突破,但免疫单药对于肝癌二线治疗的数据并不令人满意,帕博利珠单抗的Ⅲ期研究KEYNOTE-240也未达到研究终点。结合我国的药物可及性及医保等情况,瑞戈非尼目前仍是晚期肝癌二线治疗的优选。
本例患者术后短期复发,局部治疗联合索拉非尼PFS 6个月,右侧腹膜后淋巴结增大致疾病进展后更换瑞戈非尼,最佳疗效达到PR。不良反应可控,生活质量良好,PFS达11个月。局部治疗联合靶向药物序贯治疗为患者带来了生存获益,值得临床推广。
参考文献
[1] 原发性肝癌诊疗规范, 2019年版.
[2] NCCN肝胆肿瘤临床实践指南, 2019.V2.
[3] 中国临床肿瘤学会.中国临床肿瘤学会(CSCO)原发性肝癌诊疗指南, 2018.V1.
[4] Bruix J, Qin S K, Merle P, et al, et al. Regorafenib for patients with hepatocellular carcinoma who progressed on sorafenib treatment(RESORCE): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 389(10064):56-66.
[5] Finn R S, Merle P, Granito A, et al. Outcomes of sequential treatment with sorafenib followed by regorafenib for HCC: Additional analyses from the phase III RESORCE trial[J]. J Hepatol, 2018,69(2):353-358.
[6] ZHU A X, KANG Y K, YEN C J, et al. Ramucirumab after sorafenib in patients with advanced hepatocellular carcinoma and increased α-fetoprotein concentrations(REACH-2): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet Oncol, 2019,20(2):282-296.
[7] Abou-Alfa GK, et al. Cabozantinib in Patients with Advanced and Progressing Hepatocellular Carcinoma[J]. N Engl J Med, 2018 Jul 5;379(1):54-63.