慢性淋巴细胞白血病的规范化诊疗策略,看这篇就够了!

徐卫教授精彩讲解慢性淋巴细胞白血病的规范化诊疗。
慢性淋巴细胞白血病(CLL)是一种淋巴增殖性疾病,来源于成熟的单克隆B淋巴细胞。其主要发生在中老年人群中,以淋巴细胞在外周血、骨髓、脾脏和淋巴结聚集为特征。小淋巴细胞淋巴瘤(SLL)与CLL是同一种疾病,是CLL的非白血病表现,统称为CLL/SLL。
近日,来自南京医科大学第一附属医院血液科的徐卫教授做客医生站直播间,为我们分享了CLL的规范化诊断和一些经典研究,精彩内容整理如下。
CLL如何诊断?前驱病变是怎么发现的?
CLL该如何诊断呢?徐卫教授介绍了CLL诊断三项标准:
外周血单克隆B淋巴细胞计数≥5×109/L。[在2017版的世界卫生组织(WHO)肿瘤分类中,外周血单克隆B淋巴细胞计数<5×109/L时,如无髓外病变,即使出现血细胞少或疾病相关症状,也不能诊断为CLL。但2018年更新的国际CLL工作组标准仍将此种情况诊断为CLL。]
外周血涂片中特征性表现为小的、形态成熟的淋巴细胞显著增多,其细胞质少、核致密、核仁不明显和染色质部分聚集,并易见涂抹细胞。外周血淋巴细胞中不典型淋巴细胞及幼稚淋巴细胞≤55%。
典型流式细胞学免疫表型:CD19+、CD5+、CD23+、CD200+、CD10-、FMC7-、CD43+;表面免疫球蛋白、CD20及CD79b弱表达。
单克隆B淋巴细胞增多症(MBL)是所有CLL/ SLL的前驱病变,目前已知MBL是所有CLL/SLL的前兆,那么MBL如何诊断呢?
记住以下5个诊断标准:
B细胞克隆性异常;
单克隆B淋巴细胞<5×109/L;
无肝、脾和淋巴结肿大(淋巴结长径<1.5cm);
无贫血及血小板减少;
无慢性淋巴增殖性疾病(CLPD)的其他临床症状。
MBL有多种免疫表型,如CLL表型、不典型CLL表型以及非CLL表型。徐卫教授强调,当患者出现不典型CLL表型或非CLL表型,需要进行全面检查,以排除白血病期的非霍奇金淋巴瘤。如果是CLL表型,计数检查为高计数MBL的患者需要进行定期随访。
哪些患者需要治疗
只有具备以下至少1项时方可开始治疗:
1. 进行性骨髓衰竭的证据:表现为血红蛋白和/或血小板进行性减少。
2. 巨脾(如左肋缘下>6cm)、进行性或有症状的脾肿大。
3. 巨块型淋巴结肿大(如最长直径>10cm)、进行性或有症状的淋巴结肿大。
4. 进行性淋巴细胞增多,如2个月内淋巴细胞增多>50%。或淋巴细胞倍增时间(LDT)<6个月。当初始淋巴细胞<30×109/L,不能单凭LDT作为治疗指征。
5. 淋巴细胞计数>200×109/L,或存在白细胞瘀滞症状。
6. 自身免疫性溶血性贫血(AIHA)和/或免疫性血小板减少症(ITP)对皮质类固醇或其他标准治疗反应不佳。
7. 至少存在下列一种疾病相关症状:在以前6个月内无明显原因的体重下降≥10%;严重疲乏;无感染证据,体温>38.0℃,≥2周;无感染证据,夜间盗汗>1个月。
8. 临床试验:符合所有参加临床试验的入组条件。
不符合上述治疗指征的患者,建议每2-6个月随访1次。
治疗前要评估哪些内容?
如果患者有了治疗指征,我们就要在治疗前(包括复发患者治疗前)对患者进行评估。
评估的内容包括:
病史和体格检查:特别是淋巴结(包括咽淋巴环和肝脾大小);
体能状态:美国东部肿瘤协作组(ECOG)和/或疾病累积评分表(CIRS)评分;
B症状:盗汗、发热和体重减轻;
血常规检测:包括白细胞计数及分类、血小板计数和血红蛋白等;
血清生化检测:包括肝肾功能、电解质、乳酸脱氢酶(LDH)、血清β2微球蛋白(β2-MG)等;
骨髓活检±涂片:在治疗前、疗效评估及鉴别血细胞减少原因时进行。典型病例诊断和常规随访无需骨髓检查;
常规染色体核型分析(CpG刺激);
乙型肝炎病毒(HBV)检测;
FISH检测del(13q)、+12、del(11q)、del(17p),检测TP53、IGHV等基因突变。
特殊情况下检测:免疫球蛋白定量;网织红细胞计数和直接抗人球蛋白试验(怀疑有溶血时必做);超声心动图检测;妊娠筛查(育龄期妇女,拟采用放化疗时);颈、胸、腹和盆腔增强CT检查等。
对于早期无症状患者,
抢先治疗能改变患者预后吗?
到目前为止,没有任何研究证实对无症状早期CLL患者进行治疗是有益的。伊布替尼是一种BTK抑制剂,对晚期或复发性CLL具有很好的临床疗效,其在未经治疗的早期无症状CLL患者中的效果如何呢?
CLL12研究是一项随机、双盲、安慰剂对照的临床试验,目的是评估伊布替尼是否能够延长早期进展风险增加的CLL患者的无事件生存期(EFS)。
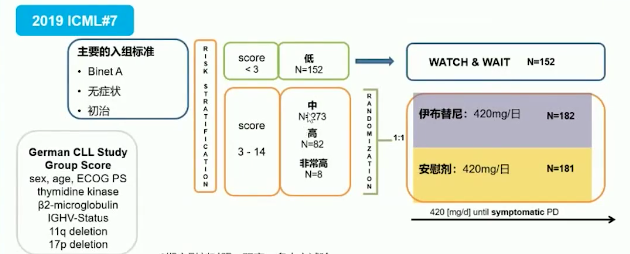
研究纳入了具有中危、高危或超高危进展风险的未经治疗无症状CLL患者,随机接受伊布替尼或安慰剂治疗。研究主要终点是EFS,次要终点是无进展生存(PFS)和下一次治疗时间(TTNT)。低风险患者(n=152)被分配到观察组,不包括在主要终点分析中。
在中位随访31个月时,伊布替尼组EFS未达到,安慰剂组EFS为47.8个月;伊布替尼组PFS未达到,安慰剂组为14.8个月(HR=0.18)。伊布替尼组的TTNT比安慰剂组长(HR=0.21)。
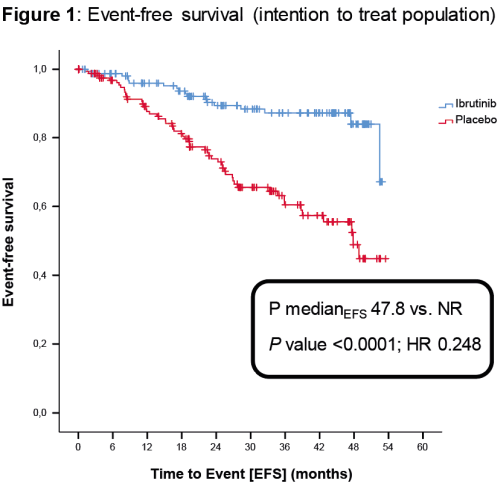
对于伊布替尼组和安慰剂组的患者,最常见的严重不良事件包括感染(11.4% vs 11.8%)和心脏疾病(8.6% vs 6.7%)等。临床特别关注的不良事件主要是常见不良反应事件评价标准(CTCAE)1-2级,在伊布替尼治疗的患者中出现得更频繁。
与安慰剂相比,伊布替尼显著改善了未经治疗的早期CLL患者的EFS、PFS和TTNT。但是总生存(OS)是否获益未知,因此目前这类患者仍可进行观察等待。
有治疗指征的患者如何选择治疗方案?
既往一些研究显示,在CLL的一线治疗上,靶向治疗相比免疫化疗有明显优势,可延长PFS和OS,获得较高缓解率。徐卫教授通过多个研究进行了阐述。
RESONATE-2研究旨在比较伊布替尼和苯丁酸氮芥在CLL中疗效及安全性。该研究共入组了269例不包括17p-的、老年初治(≥65岁)CLL/SLL患者,按1:1比例随机分配至伊布替尼组(n=136)及苯丁酸氮芥组(n=133)进行治疗。经过中位5年随访,伊布替尼组中位PFS未达到,苯丁酸氮芥组为15个月。两组5年PFS率为70% vs 12%;5年OS率分别为83% vs 68%,伊布替尼组占优。
在安全性方面,伊布替尼组不良事件发生率在治疗1年后呈现出不断降低的态势,总体上≥3级不良事件越来越少。
E1912研究是一项评估伊布替尼联合利妥昔单抗(IR)和氟达拉滨、环磷酰胺联合利妥昔单抗(FCR)治疗≤70岁初治CLL患者的Ⅲ期临床研究。研究结果显示,IR组的PFS和OS均显著优于FCR组:两组3年PFS率分别为89%和71%,3年OS率分别为99%和93%。
安全性方面,IR组治疗患者≥3级治疗相关不良事件发生率低于FCR组,分别为70%和80%。在治疗43个月时,仍有73%的患者继续使用伊布替尼治疗,说明药物的安全性和耐受性均较好。
A041202研究是一项多中心随机Ⅲ期研究,纳入547例≥65岁初治CLL/SLL患者,随机接受伊布替尼单药、伊布替尼+利妥昔单抗(IR)或苯达莫司汀+利妥昔单抗(BR)治疗,中位随访32个月。结果显示,伊布替尼单药比BR治疗的疾病进展或死亡风险降低61%。
在III期研究iLLUMINATE中,与苯丁酸氮芥+Obinutuzumab相比,伊布替尼+Obinutuzumab组的PFS获得显著改善(中位PFS不可评估 vs 19个月),疾病进展或死亡的风险降低77%。孤立评审委员会评估的伊布替尼+Obinutuzumab的ORR为89%,而苯丁酸氮芥+Obinutuzumab的ORR为73%,体现了新药的优势。
III期ELEVATE-TN研究中,研究者评估了Acalabrutinib+Obinutuzumab、Acalabrutinib单药和Obinutuzumab+苯丁酸氮芥治疗初治CLL患者的疗效和安全性,患者中位年龄70岁(41-91岁)。中位随访28个月时,Acalabrutinib+Obinutuzumab较Obinutuzumab+苯丁酸氮芥显著延长PFS(未达到 vs 22.6个月),降低了90%疾病进展或死亡风险。
Acalabrutinib+Obinutuzumab、Acalabrutinib和Obinutuzumab+苯丁酸氮芥各组预估30个月的PFS率分别为90%、82%和34%。结果显示,Acalabrutinib+Obinutuzumab和Acalabrutinib单药治疗初治CLL较Obinutuzumab+苯丁酸氮芥能明显改善PFS。
CLL一线治疗推荐:
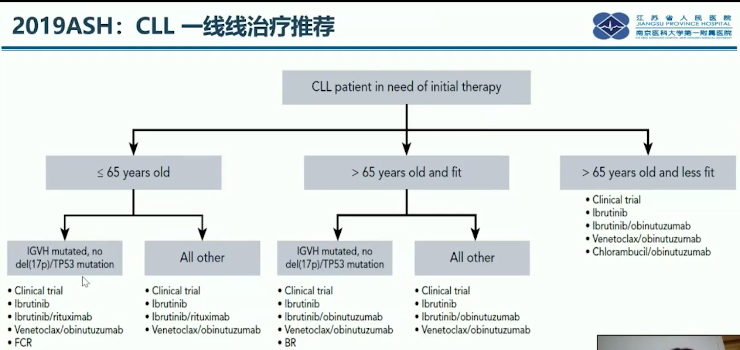
最后,徐卫教授为大家介绍了两个具有临床价值的新药,
泽布替尼:2019年11月,中国自主研发的抗癌新药泽布替尼(zanubrutinib)被美国食品药品监督管理局(FDA)批准用于复发/难治性套细胞淋巴瘤(R/R MCL)的治疗。目前,泽布替尼正在进行CLL/SLL和华氏巨球蛋白血症(WM)患者的一线治疗临床研究。
Acalabrutinib:是一种选择性BTK抑制剂,具有良好的耐受性,可作为单药治疗或与Obinutuzumab联合使用,既往发现Acalabrutinib可使CLL细胞对Venetoclax敏感。