一文读透结直肠癌PD1免疫治疗神预测指标-微卫星不稳定(MSI)!
结直肠癌作为全球发生率排名第二,死亡率排名第三的恶性肿瘤严重威胁人类生命健康,而且肿瘤的异质性很强,可谓是癌症家族中的“豪门”。近些年,结直肠癌跟化疗、放疗、靶向治疗的纠葛已经不吸引大家眼球了,免疫治疗后来居上,特别是“微卫星不稳定”的介入,让其中的爱恨情仇掀起了层层波浪,想知其中缘由,请听本文娓娓道来。
卫星不稳定的家族大起底
江湖恩怨,总是跟家族脱不了干系。微卫星不稳定有一个酷炫的简称MSI,它能入癌症家族“豪门”的法眼,自有它的过人之处。
说起微卫星不稳定的家族,怎么能少的了它大家长“微卫星”呢,它虽然只是简单重复的DNA序列,由1-6个核苷酸组成,一旦出现异常,使错配修复基因(MMR,Mismatch Repair)缺失,失去功能,发生突变,而且没法修复,微卫星不稳定性(MSI)就出现了,大大的增加了结直肠癌变的几率,有研究报道说有15%的结直肠癌跟它相关呢,更多见于右半结肠,跟发病相关就算了,还关系到结直肠癌的遗传疾病筛查、治疗及预后。能不引起我们的”豪门“的注意吗?
微卫星不稳定是怎么被发现的?
说道微卫星不稳定怎么发现的,就不得不提到家族遗传性疾病“林奇综合征(Lynch Syndrome)”,也叫遗传性非息肉病性结直肠癌(HNPCC),科学家们在研究这类疾病中发现超过90%的林奇综合征是由于错配修复基因(MMR)突变引起微卫星不稳定(MSI)而发生的。因此MSI/dMMR检测目前已经成为国际上筛选林奇综合征患者的重要诊断指标。
MLH1缺失的MMR缺陷型肿瘤应行BRAF V600E突变分子和(或)MLH1甲基化检测,以评估发生林奇综合征的风险。听说子宫内膜癌、卵巢癌、胃癌、肺癌等对微卫星不稳定也有意思,但是还是不能竞争过结直肠癌。
为了彻底的了解微卫星不稳定,科学家研究了可以检测它的不同方法:
免疫组化(IHC)
该方法是通过使用相应抗体检测四种常见错配修复基因(MLH1、MSH2、MSH6和PMS2)在细胞核内表达的情况,明确是否存在错配修复功能缺陷。存在1种或以上蛋白表达缺失的,即为dMMR,相当于MSI-H;否则为错配修复蛋白完整(pMMR),相当于MSI-L/MSS。但是IHC检测容易受到抗体质量、检测过程(固定、染色)等因素影响。
聚合酶链式反应(PCR)
该方法是MSI检测的金标准,灵敏度高,特异性强。目前最常用的Bethesda标准检测5个位点,BAT-25、BAT-26、D5S346、D2S123和D17S250。结果出现2个或以上的不稳定为微卫星高度不稳定MSI-H,存在1个位点为微卫星低度不稳定(MSI-L),而无不稳定位点则为微卫星稳定(MSS)。但是PCR不能提供准确的突变基因,且实验周期较长。
高通量测序技术(NGS)
主要有两种方式,其一是通过全外显子测序检测TMB估测MSI状态,TMB高与MSI-H显著相关。另一种方式是通过选择一组位点的reads数目分布直接评估微卫星不稳定的程度(MSIsensor、mSINGS)。但目前NGS检测MSI尚缺乏统一的标准,且价格昂贵。
结直肠癌中有15%的发病率跟微卫星不稳定相关,研究表明,MSI-H早期结肠癌(II/III期)具有独特的临床病理学和分子生物学特征,临床进展缓慢,淋巴结转移和远处转移较少,与非MSI-H型结肠癌相比预后相对较好。特别是在II期的MSI/dMMR结直肠癌术后患者中,单纯手术的5年生存率高达80%,化疗药物单药5-FU并未带来明显效益,我们2020年的CSCO指南就写的很清楚了。
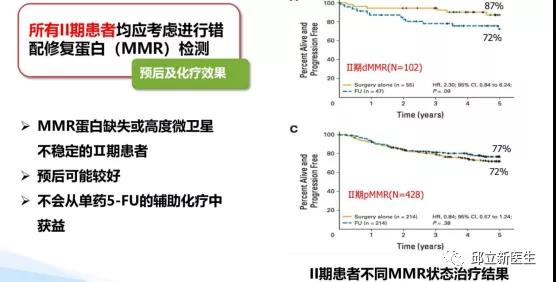
再来看看我们2020年NCCN指南怎么说的,II期MSI/dMMR结直肠癌术后,观察就可以,连化疗都省了,对这部分患者是不是不幸中的大幸呢。

在Ⅲ期结直肠癌中,接受了术后辅助化疗的MSI-H/dMMR患者,预后是优于MSS患者的。
免疫治疗时代的MSI
本以为他们的故事就仅限于此了,哪知,免疫治疗时代的到来再次激起了他们之间的火花。
早期的一些抗PD-1免疫治疗临床试验在转移性结直肠癌的治疗中并没有发现显著获益,后有研究将患者进一步细化,于2015年正式开启“豪门”与MSI的对抗时代。
结直肠癌的后线免疫治疗
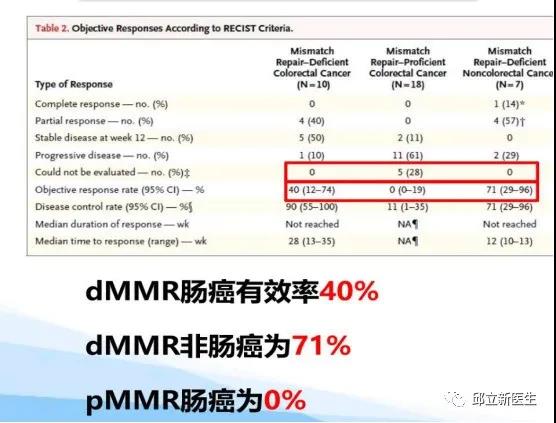
KEYNOTE-016中,研究者发现dMMR的多种肿瘤均可从帕博利珠单抗免疫治疗中获益,其中dMMR非肠癌患者的客观缓解率(ORR)为71%,而在晚期结直肠癌病例中,帕博利珠单抗单药治疗在标准治疗失败的dMMR/MSI-H患者的ORR为40%,在pMMR患者的ORR为0。dMMR/MSI-H组所有患者均未达到中位无进展生存(PFS)期和总生存(OS)期,而pMMR组中位PFS和OS仅为2.2和5.0个月。因此,该研究确定了dMMR/MSI-H是免疫治疗疗效的分子标志。
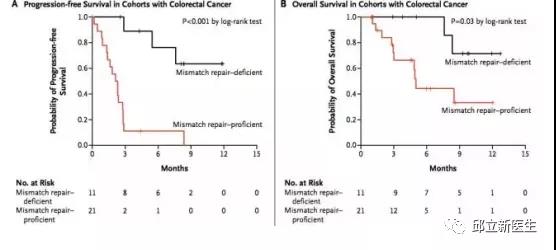
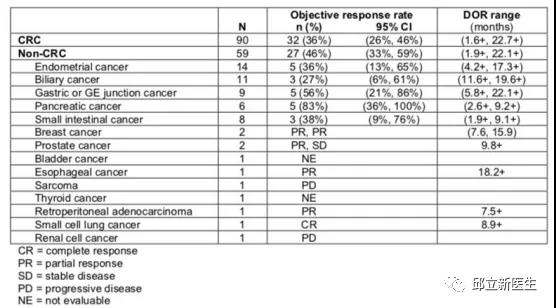
KEYNOTE-164和158研究证实,Pembrolizumab用于经治晚期MSI-H 结直肠癌患者带来33%的ORR, 且有长期生存获益。基于KEYNOTE-016、164及158等五项研究的卓越成果,2017年5月,FDA批准帕博利珠单抗用于包含结直肠癌在内的所有具有MSI-H/dMMR的实体瘤患者的治疗。
结直肠癌一线、二线免疫治疗
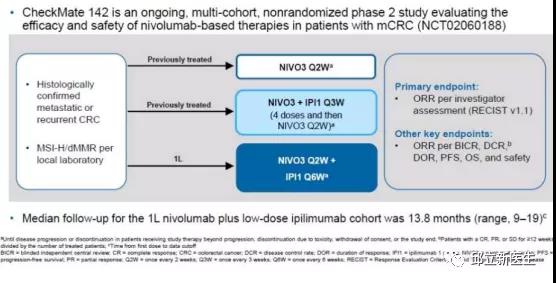
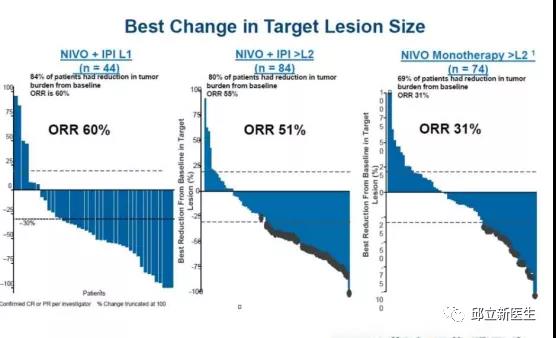
CheckMate 142研究,主要对纳武利尤单抗为基础的治疗在转移性结直肠癌患者中的疗效与安全性进行了评估。结果显示,在一线治疗中,纳武利尤单抗+伊匹木单抗双免疫治疗的ORR为60%,BRAF突变患者的ORR比整体更高,为71%,当然该亚组的病例数较少,仅17例。二线以上治疗中,纳武利尤单抗+伊匹木单抗双免疫治疗在经治dMMR患者中的ORR为55%, 纳武利尤单抗单药用于经治MSI-H/dMMR 转移性结直肠癌患者,ORR为31%,1年生存率为73%,结果与帕博利珠单抗类似。PFS和OS结果显示,一线治疗优于后线治疗,双免疫治疗优于免疫单药治疗。目前NCCN与CSCO指南均推荐免疫治疗用于dMMR/MSI-H肠癌患者。
基于CheckMate 142研究,2017年8月1日,FDA加速批准 纳武利尤单抗用于治疗12岁及以上,经氟尿嘧啶,奥沙利铂和伊立替康治疗后进展的dMMR/MSI-H转移性结直肠癌患者。
KEYNOTE-177研究,对270例dMMR的局部晚期结直肠癌或不可切除的转移性结直肠癌患者接受一线帕博利珠单抗单药或化疗的效果进行了对比。这项国际、随机、开放标签的Ⅲ期临床研究以PFS和OS作为双重主要终点。目前该研究称PFS终点已达到,且PFS的改善兼具统计学意义和临床意义,另一终点OS数据尚未成熟,我们期待后续数据的更新。
另一项正在进行的COMMIT研究,主要对靶向+化疗、免疫单药、免疫+靶向+化疗的疗效进行对比,能否取得阳性结果仍有待观察。
新辅助免疫治疗
2018年ESMO年会上报道的荷兰的NICHE研究,入组Ⅰ~Ⅲ 期结肠癌患者,dMMR和pMMR各7例,对纳武利尤单抗+伊匹木单抗用于术前新辅助治疗的效果进行了评估。结果发现,仅仅经过1个月的治疗[1次伊匹木单抗治疗(d1),2次纳武利尤单抗治疗(d1+15)],100%的dMMR肿瘤(7例)得到了明显缓解,4例患者达到了完全缓解,而pMMR患者则几乎没有出现缓解。该小样本研究提示在dMMR患者,新辅助免疫治疗带来的良好病理退缩,但是能否转化为生存获益,那就得看后续的进一步研究了,同时能否替代传统的手术治疗非常值得探索。
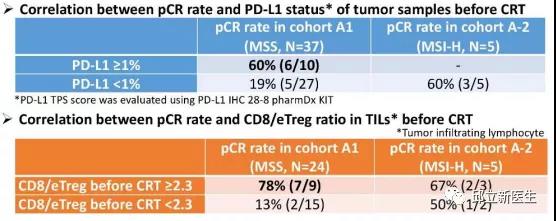
2020年ASCO更新了一项来自日本的VOLTAGE-A研究结果:研究纳入了MSS患者37人为队列A1和MSI-H患者5人为队列A2。结果显示,队列A1的37人中,11人达到了pCR(30%)。另外3人为TRG1级,即14例(38%)取得了重大病理缓解(TRG0-1)。另有1例患者达到cCR,进行等待观察,未行手术。队列A2的5人中,3人达到了pCR(60%)。 截至2020年1月,A1和A2队列中位随访时间分别为22.5个月和6.6个月,MSS患者中2例出现局部复发,2例发生远处转移;MSI-H患者无复发。
想要全程对抗微卫星不稳定,怎么能放过术后辅助治疗呢?
术后辅助免疫治疗
ATOMIC研究,为了对结直肠癌术后辅助免疫治疗进行探索,将接受过手术与1个周期mFOLFOX6化疗后的Ⅲ期结肠癌患者进行微卫星状态的检测,并将其中的dMMR/MSI-H患者分为两组,分别接受后续的标准化疗或标准化疗基础上加用阿替利珠单抗。该研究尚在进行中,结果值得期待。
总之,微卫星不稳定与结直肠癌之间的故事还在上演,而且随着医学的不断进步以及临床研究的探索,它们之间的爱恨情仇会在癌症江湖中一直流传。
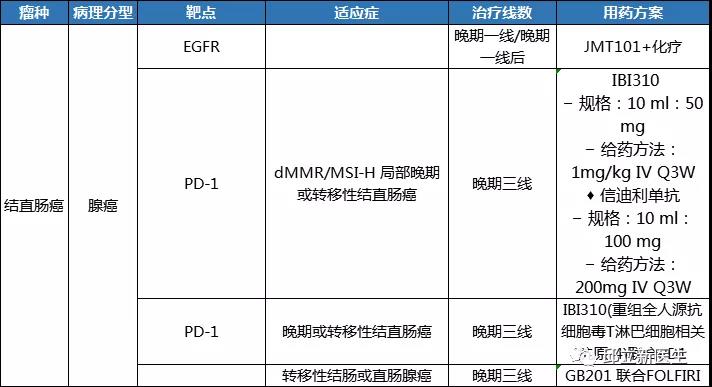
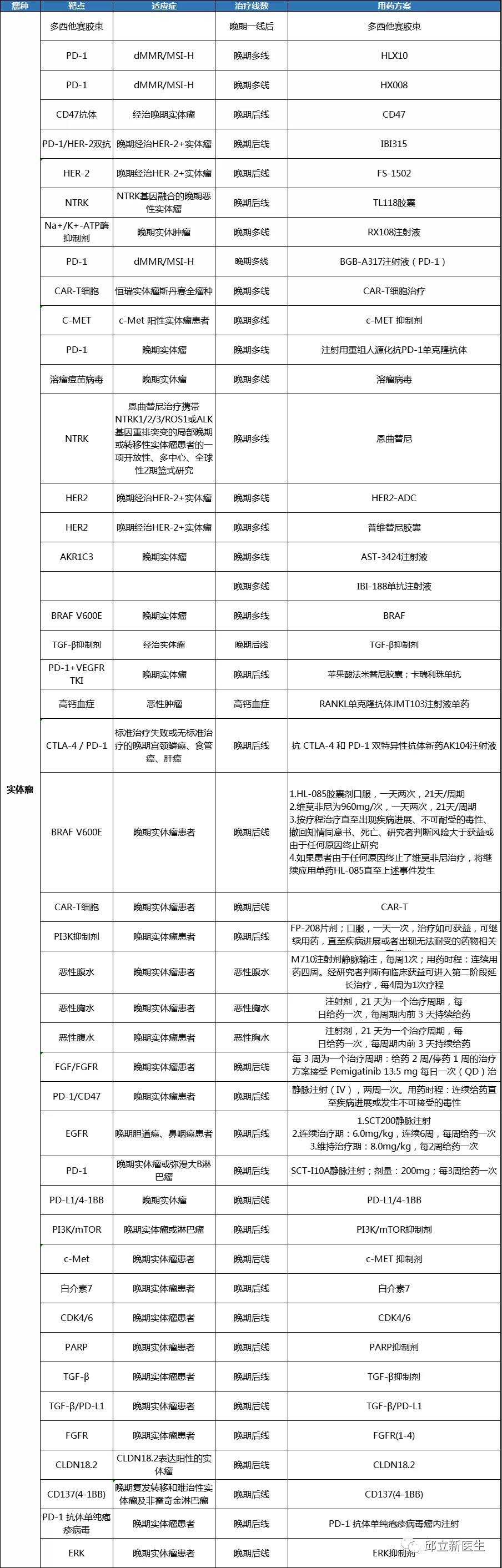
正在招募的临床试验(肠癌 MSI-H、实体瘤)
结直肠癌