跨四线治疗OS达40月余,卡瑞利珠单抗假性进展实为真获益
近年来,免疫治疗的出现极大地改变了肝癌治疗的格局,为肝癌患者带来了新希望。值得欣喜的是,由我国自主研发的PD-1抑制剂卡瑞利珠单抗在经治晚期肝细胞癌(HCC)患者中取得了显著疗效,研究成果于近期成功登上国际顶级期刊《柳叶刀·肿瘤学》。卡瑞利珠单抗由此正式获批肝癌治疗适应症,标志着中国肝癌治疗进入“免疫新时代”。
为了让临床医生更好地了解领域内最新研究进展并将其应用于临床,从而让更多中国患者受益,中国医学论坛报特邀卡瑞利珠单抗治疗经治晚期HCC的Ⅱ期临床研究的主要参与者南京金陵医院华海清教授和成远教授,为我们分析卡瑞利珠单抗的临床应用价值,并分享肝癌研究中的心得体会以及复杂患者的临床管理经验。以下为整理采访精要,以飨读者。

临床医生可靠选择,患者实际获益,卡瑞利珠单抗获批推动我国免疫治疗整体进展
问:卡瑞利珠单抗于今年3月18日获批肝癌适应证,您如何评价此项获批的意义?
华海清教授:卡瑞利珠单抗获批肝癌适应证的意义主要体现在三个方面。
对于肝癌患者来说,多了一种疗效较好且副反应低的药物新选择。众所周知,肝癌的治疗难度较大,且在索拉非尼上市后的近十年间,靶向治疗几乎没有取得突破性的进展。可喜的是,2017年以后免疫治疗的兴起为肝癌领域带来了更多希望。虽然医学研究者在免疫治疗中的探索经历了几多风雨,多项在当时受到诸多关注的研究相继宣布失败,但研究者坚持不懈的付出最终还是收获了成果。卡瑞利珠单抗于今年3月18日获批肝癌适应证,是国家药品监督管理局(NMPA)对研究结果的肯定,同样也是我国肝癌患者的福音。
对于临床医生来说,卡瑞利珠单抗适应证的获批意味着在应用现有治疗药物方案效果不佳时,多了一种安全可靠的治疗选择。这项由秦叔逵教授牵头开展的卡瑞利珠单抗治疗经治晚期HCC的Ⅱ期临床研究获得的成果,使得卡瑞利珠单抗成为了首个获批肝癌适应证的免疫检查点抑制剂。因此对于符合指南用药标准的肝癌患者,临床医生可以放心大胆地应用卡瑞利珠单抗治疗方案。
对于我国肝癌治疗领域来说,卡瑞利珠单抗研发的成功,可以说推动了我国免疫治疗的整体进展。众所周知,免疫治疗是肿瘤领域中的热门疗法,且获得了诸多值得肯定的研究成果。但卡瑞利珠单抗能在难治性癌种——肝癌中获得突破性治疗进展,则表明我国目前的医疗技术研发水平已经跻身世界前列。因此,我们有理由也有信心相信,即便是在难治性癌种中,只要大家秉持锐意进取的研究态度,在经过坚持不懈的探索研究后,我国的免疫治疗一定能够走在国际前沿。
问:作为卡瑞利珠单抗该项研究的主要参与者之一,您如何评价该方案的有效性及安全性?
华海清教授:作为全国开展肝癌研究较早且进行项目较多的中心,南京金陵医院肝癌领域研究在秦叔逵教授的带领下,几乎参与了近些年来国内外所有的肝癌多中心临床研究。而作为团队中的一员,我也有幸参与其中。从目前的研究结果来看,肝癌的中位生存时间在一线治疗中可达至少20个月,在二线治疗中也可达8~13个月左右,证明了免疫治疗兴起后,肝癌治疗水平的进步。
这项由秦叔逵教授牵头开展的卡瑞利珠单抗治疗经治晚期HCC的多中心、开放性、平行、随机、Ⅱ期临床研究(n=217)结果表明,经卡瑞利珠单抗治疗后,患者的ORR为14.7%,6个月OS率为74.4%,中位OS为13.8个月,DCR为44.2%,中位TTR为2个月,整体安全性可控。能获得如此可观的成果,一方面要归功于医务工作者的辛勤劳动,另一方面还要感谢患者的付出。
回顾整个研究进程,是患者的真实获益为卡瑞利珠单抗应用的有效性及安全性“站台”,特别是本研究入组的第一例肝癌患者,为最初对方案心怀忐忑的研究者增加了极大的信心。患者经索拉非尼一线治疗失败,病灶增多,同时合并肺转移。二线应用卡瑞利珠单抗治疗的结果出乎意料,两个疗程以后,患者疗效评估即达到PR,并持续PR,后续患者肿瘤几乎消失,生活质量大大提高。
免疫治疗虽然在多数肝癌患者中起效较慢(2~3个月左右),但患者一旦获益则极有可能长期获益。从现有的报道来看,患者在应用PD-1单抗后,中位有效时间可达15个月,特别是疗效评估为CR或PR的患者,生活质量提高显著。因此与传统化疗和靶向治疗相比,免疫治疗的获益持续性更长。
我认为,虽然仍有部分患者无法从免疫治疗中获益。但整体来看,卡瑞利珠单抗治疗经治晚期HCC的疗效肯定,获益持续性佳且安全性可控,是临床医生治疗肝癌的有力武器。
问:目前2020版《CSCO原发性肝癌诊疗指南》已经发布,相关更新亮点是怎样的?
华海清教授:2020版《CSCO原发性肝癌诊疗指南》的制定贴合我国肝癌现状,对临床应用具有比较重要的指导意义。整体来看,一线治疗仍以靶向治疗为主,同时还囊括了联合治疗方案。更新亮点之一是我国自主创新药物阿帕替尼以Ⅰ级专家1A类证据推荐用于肝癌二线治疗。而更为重要的更新点就是推进了PD-1单抗的应用。基于卡瑞利珠单抗在经治肝癌患者中取得的突出疗效,该方案可能是更适用于我国肝癌患者的治疗优选。
假性进展真获益,卡瑞利珠单抗疗效评估需掌握诊疗全面观
问:在应用免疫治疗时,常出现假性进展,您认为该如何判断疾病真性/假性进展?
华海清教授:假性进展是免疫治疗的特点之一。正常情况下,肿瘤患者的免疫功能被抑制,而PD-1单抗可以恢复T细胞功能,使得T细胞进一步增殖,并迁移到肿瘤内部与之对抗,此时肿瘤病灶暂时性增大,呈现假性进展状态,但继续应用PD-1单抗后,肿瘤病灶开始变小、肿瘤细胞数量逐渐减少。因此在判断免疫治疗后是否发生真或假性进展时,需首先评估患者的主观感受。假性进展患者的机体反应良好,PS评分高,无恶化迹象,部分原有症状甚至减轻或消失。其次需结合中国特色性肝癌特点对患者进行评估。乙肝病毒感染是我国肝癌的主要诱因,约70%的肝癌患者甲胎蛋白较高,因此发生肝癌假性进展时,甲胎蛋白不增反降。
最新的《实体瘤免疫疗效评价标准》,即iRECIST标准指出,若第一次评估疗效时肿瘤进展,可继续应用免疫治疗药物至下次评估。若第二次评估时肿瘤持续增大,则为真性进展;若肿瘤缩小,则为假性进展。
总的来说,结合临床实践并参考权威评价标准判断肿瘤的真或假性进展尤为重要。这也提示了临床医生在应用免疫治疗时不应以偏概全、轻易否定,要掌握治疗的全面观,让患者从免疫治疗中获益。
多选中看优选,免疫精准治疗挑战与机遇并存
问:在真实世界中,晚期HCC患者的病情往往较为复杂,那么如何在这种情况下做好药物或治疗方案的把控呢?
华海清教授:肝癌领域的研究成果往往与临床困惑同在,这就意味着在真实世界诊疗中,临床医生将面临更多挑战。首先,当面对种类繁多的药物或治疗方案时,临床医生需要根据不同靶向或免疫治疗药物的作用机制来进行选择,避免重复。其次要优化免疫治疗的优势人群选择,虽然目前研究资料有限,但已有研究证实,PD-L1表达阳性的患者较表达阴性的患者,对免疫治疗的反应更好,表明了PD-L1与疗效有相关性。另外肿瘤突变负荷(TMB)≥10个突变/Mb或微卫星高度不稳定(MSI-H)/错配修复缺陷(dMMR)阳性的患者,已证实与肝癌免疫治疗的优势人群相关。
相信随着临床及基础研究的进展,免疫治疗的临床应用会更加精准、优越,同时临床医生的诊疗也会更加规范可行。

多线治疗,联合应用,从实际病例看卡瑞利珠单抗长期获益
问:在应用卡瑞利珠单抗治疗经治晚期HCC患者时,是否有一些令您印象深刻的病例呢?您对该病例的诊疗体会是怎样的?
病 例
患者情况:39,肝细胞癌合并肺转移,既往有肝炎、肝硬化病史。
二线诊疗经过:一线索拉非尼治疗失败后,于2017-01-23至2018-02-01予卡瑞利珠单抗(3 mg/kg,每3周1次)治疗,PFS最终达13个月。主要不良事件为1级反应性皮肤毛细血管增生症和1级谷丙转氨酶升高。


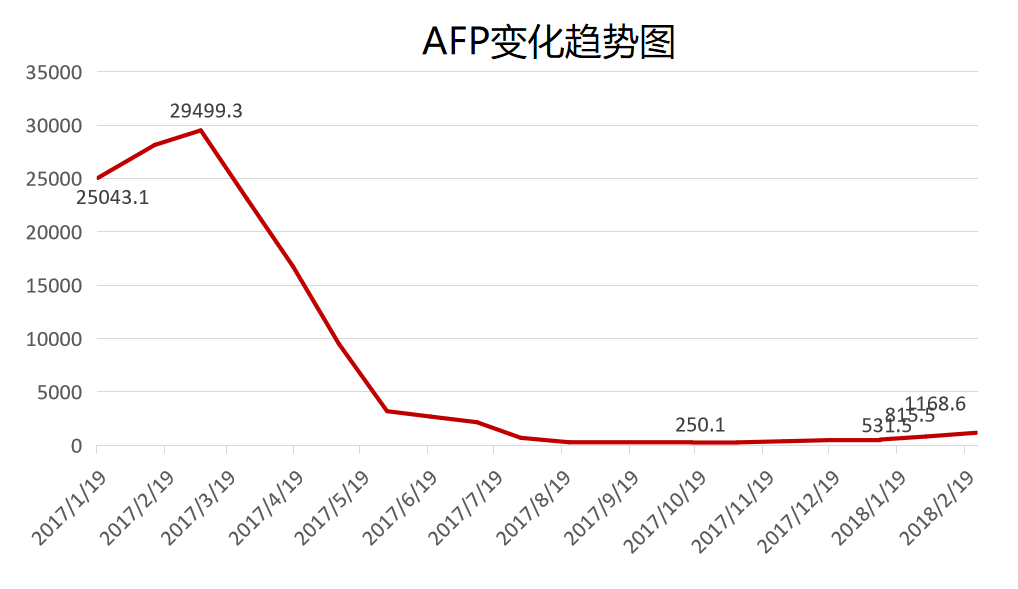
三线诊疗经过:2018-04-05至2018-09-07予卡瑞利珠单抗(200 mg VD d1,每2周重复)联合mFOLFOX4方案(奥沙利铂150 mg VD d1,亚叶酸钙200 mg VD d1,5-FU 0.5 g IV d1,2.0 g CIV46h,每2周重复)治疗10个周期。2018-09-07胸腹部CT示右肺门病灶较前增大,疗效评价PD,三线治疗PFS达4个月。主要不良事件为1级反应性皮肤毛细血管增生症、1级乏力和1级腹泻。

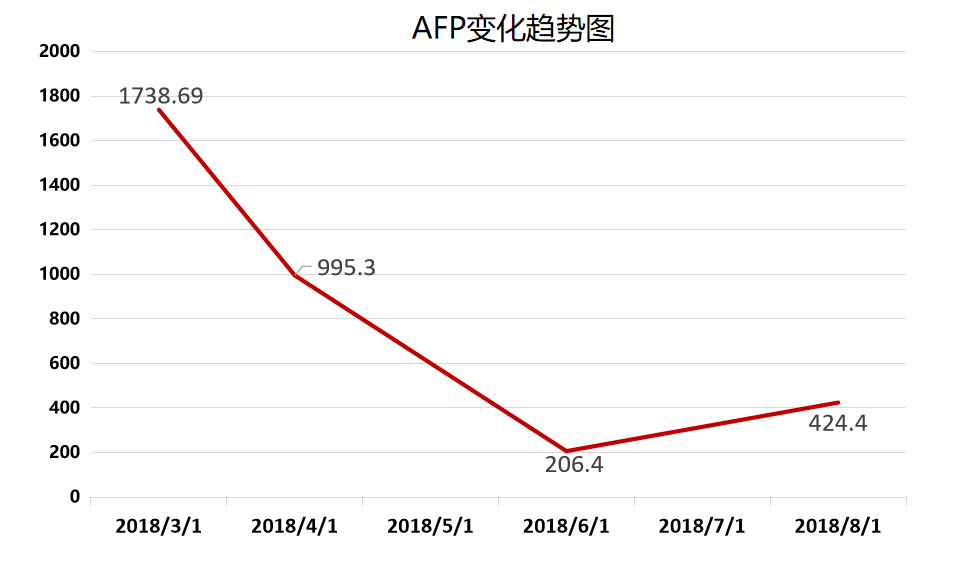
四线诊疗经过:2018-09-21至今予卡瑞利珠单抗(200 mg VD d1,3周重复)联合阿帕替尼(250 mg,口服,每日1次)治疗。2018-10-21至2018-11-18行右肺病灶TOMO刀治疗。患者2019-05-27 胸腹部CT示右肺门病灶较前缩小,疗效评价PR。主要不良事件为1级乏力和1级腹泻。

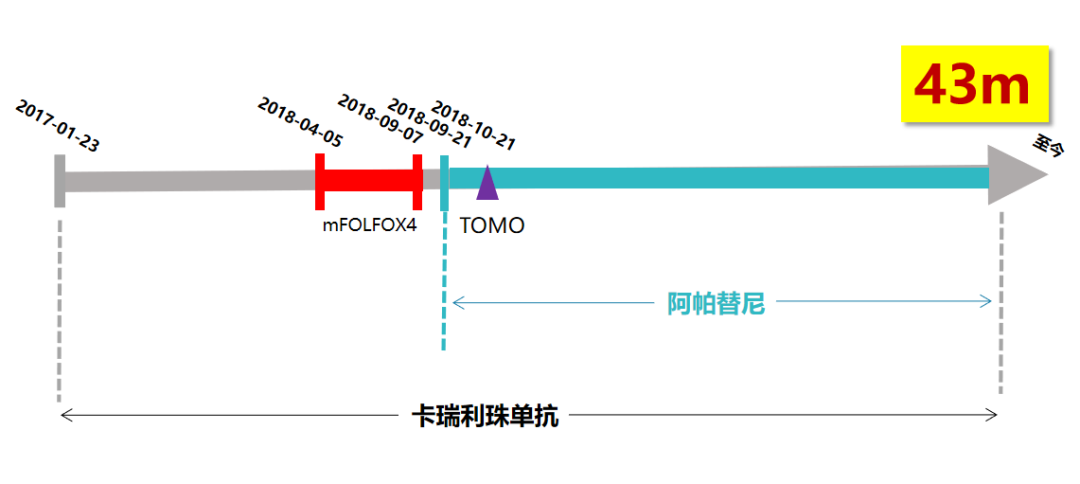
成远教授:首先这位患者的疗效值得肯定。经卡瑞利珠单抗治疗后,患者的肿瘤最大缩小到近一半,PFS达13个月,超过了既往研究的中位OS。
其次,在整个治疗期间,患者总体生活质量高,毒副反应可控,主要不良事件为反应性皮肤毛细血管增生症(RCCEP)、腹泻、乏力和转氨酶升高,且均为1级。作为卡瑞利珠单抗的独特不良事件,RCCEP通常发生在治疗的第一周期,程度多为1~2级,且用药3~4个周期后多数会自行消退。有研究证明,RCCEP的发生率与生存获益和客观疗效有关,因此其有望成为卡瑞利珠单抗临床获益的主要标志。
第三,本例患者历经四线治疗,而每次治疗方案的更换均是经过慎重讨论。在免疫治疗中,若整体肿瘤快速进展,则需换药治疗;若缓慢进展,可以考虑联合其他药物;若个别病灶进展但总体控制稳定,可以在原有基础上联合局部治疗。本例患者正是在卡瑞利珠单抗方案基础上,先后联合化疗、阿帕替尼靶向治疗,并在局部加用放疗后,获得临床获益。
最后,本例患者在治疗前两个月时病灶持续增大,而由第3个月起病灶开始缩小,最终达到PR。通常免疫治疗单独应用的起效时间为3个月左右,但有时临床医生也会遇到肿瘤假性进展的情况(总体发生率<10%)。虽然目前假性进展的发生机制尚无定论,但主流观点认为,大量T细胞和免疫调控细胞进入肿瘤病灶区域后,造成了影像学上肿瘤阴影面积的增大,但实际上这种增大并非来源于肿瘤细胞的复制,而是源于免疫细胞的聚集。因此,假性进展是免疫治疗中的一个利好现象。目前临床通常采用免疫治疗特有的评价标准,给予两次进展机会帮助辨别,除此以外临床医生还可以通过穿刺活检和监测ctDNA的方法协助判断。当然,最终是否继续用药还要结合患者的体能状况、全身症状和肿瘤标记物等情综合评估。