Venetoclax联合治疗复发/难治FL,无化疗效果欠佳,多重联合剂量需求索
滤泡淋巴瘤(FL)患者通常采用利妥昔单抗联合化疗的方案进行治疗,与单纯化疗相比,联合治疗可提高患者的缓解率、无进展生存(PFS)和总生存(OS)。然而,复发/难治患者仍然预后不良,联合靶向药物的治疗可增加化疗的敏感性,进一步提高肿瘤治疗的效果。近日在Blood上发表的开放性Ⅱ期临床研究中(NCT02187861),评估了Venetoclax、Rituximab、Bendamustine与化疗不同的联合方案治疗复发/难治FL患者的疗效及安全性。
研究背景
关于Venetoclax(VEN)

前期临床数据
慢性淋巴细胞白血病(CLL)和非霍奇金淋巴瘤(NHL)患者应用Venetoclax(VEN)+Rituximab(R)或VEN+Bendamustine+R(BR)治疗可能比单纯的R或化疗的效果更佳;FL患者接受VEN单药或联合BR治疗疗效和安全性良好。
研究方法
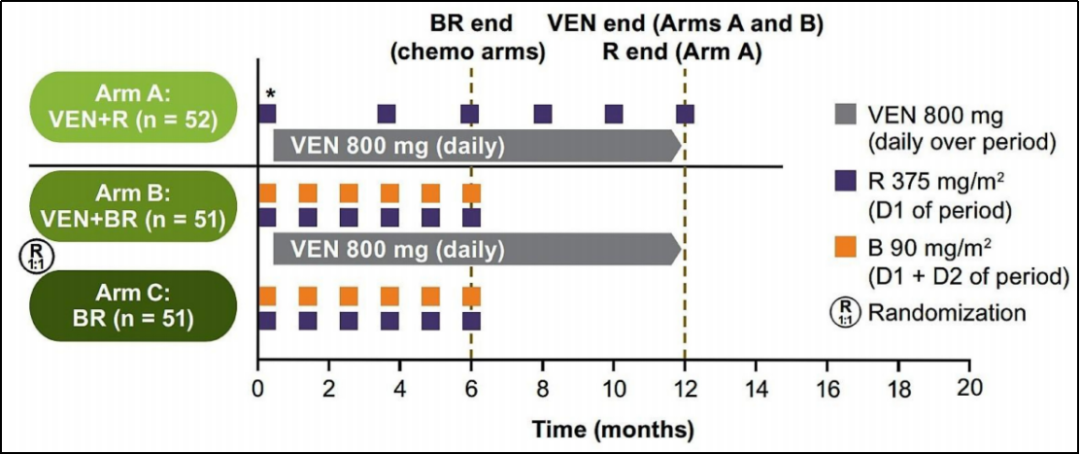
图1 研究方案设计
用药方案
A组:无化疗 VEN(800 mg/d) + R(375 mg/m2);用药时间R:C1: D1、D8、D15、D22;C4、C6、C8、C10、C12: D1
B组:含化疗 VEN(800 mg/d) + B(90 mg/m2) + R(375 mg/m2);用药时间B:D1、D2;R:D1
C组:含化疗 B(90 mg/m2 ) + R(375 mg/2);用药时间B:D1、D2;R:D1
入排标准
入组:年龄≥18岁;1~3a级FL;至少接受过1次治疗。排除:原发性中枢神经系统淋巴瘤,28天内接种过疫苗或接受过化疗。
研究终点
治疗6疗程后,PET评估的完全代谢性缓解(CMR);CT评估的完全缓解(CR),总反应率(ORR)、缓解持续时间(DOR)以及无进展生存(PFS)。
研究结果
人群特征
2014年11月13日至2018年3月16日,8个国家的57个地点共有163例患者登记入组,其中52例、51例、51例患者被随机分配进入A组(VEN+R)、B组(VEN+BR)和C组(BR),入组的3例患者(A组2例,B组1例)未能接受治疗,最终对160例患者进行了疗效和安全性的分析。
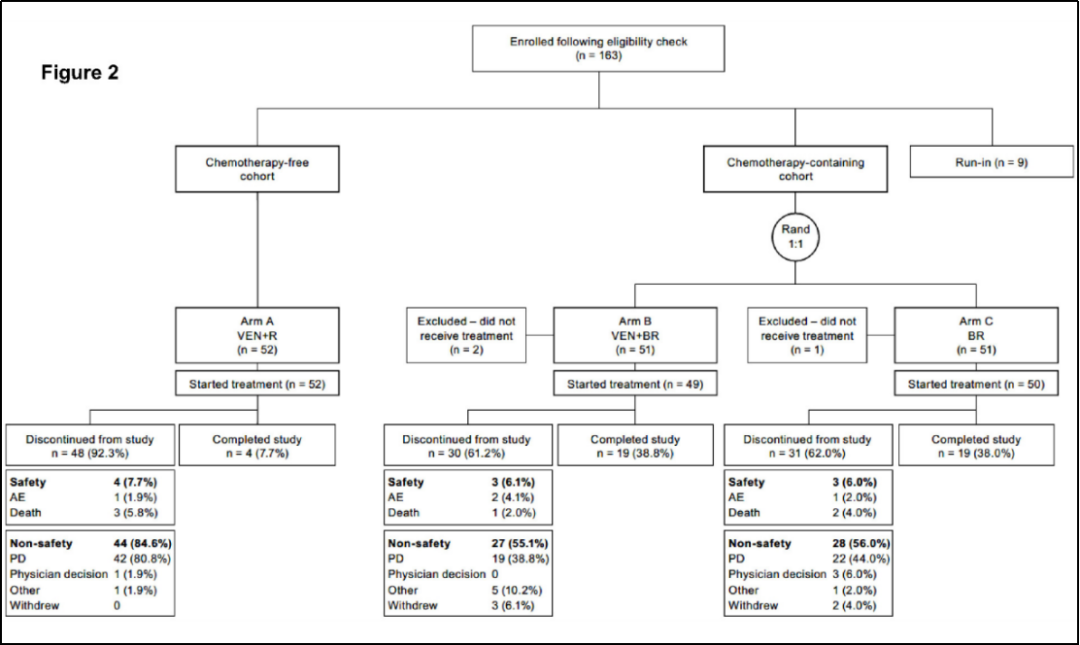
图2 患者入组情况
120例(87.6%)患者BCL-2为阳性(IHC评分为2/3+),各研究组的比例相似。86例(81.1%)患者存在BCL-2重排,各研究组的比例相似。80例(77.7%)患者MRD检测呈阳性。10例患者(A组4例,B组5例,C组1例)接受了自体造血干细胞移植。4例患者由于不良事件(AE)停止治疗,治疗过程中6例患者死亡。
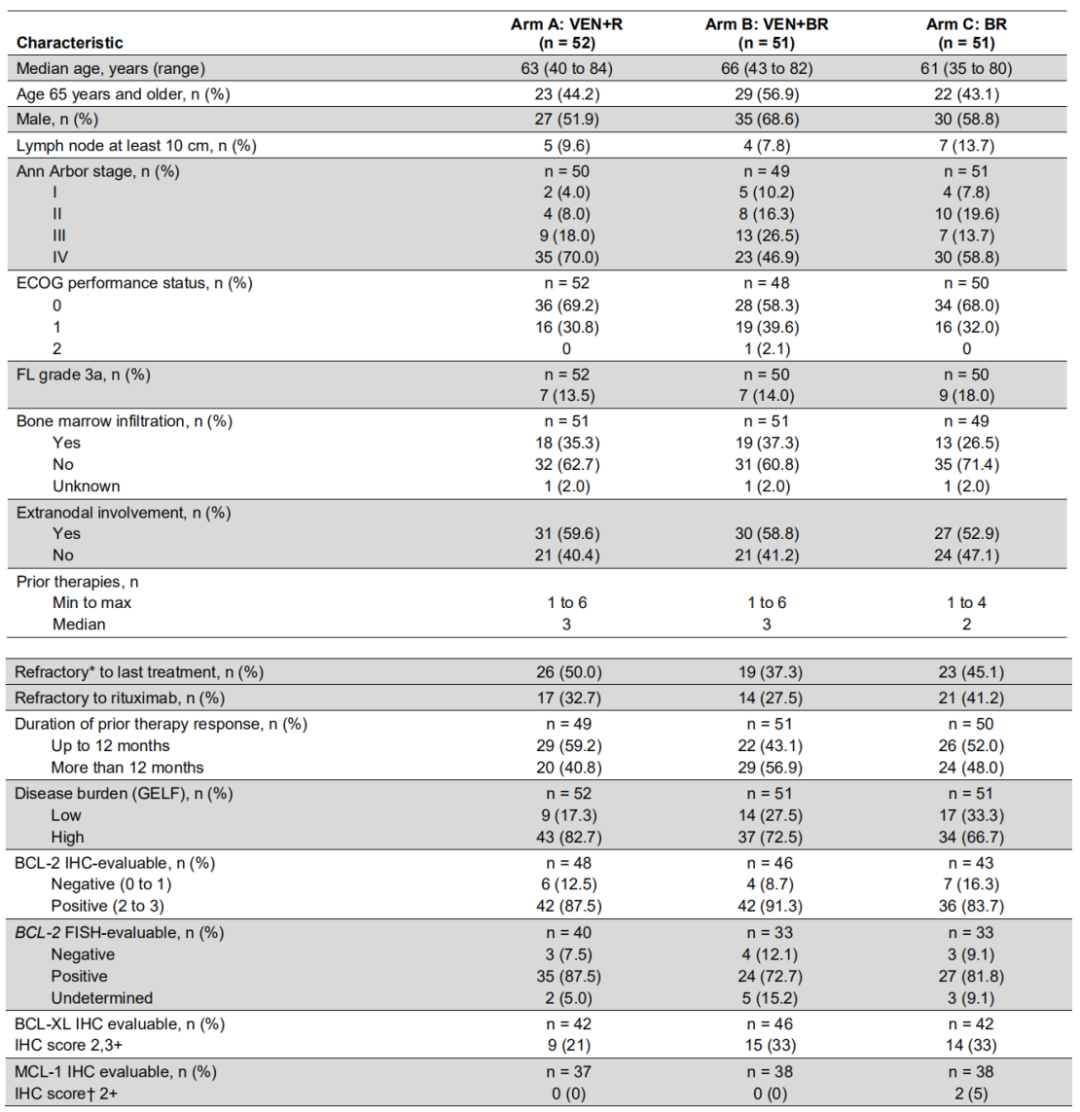
表1 患者基线特征
疗效性
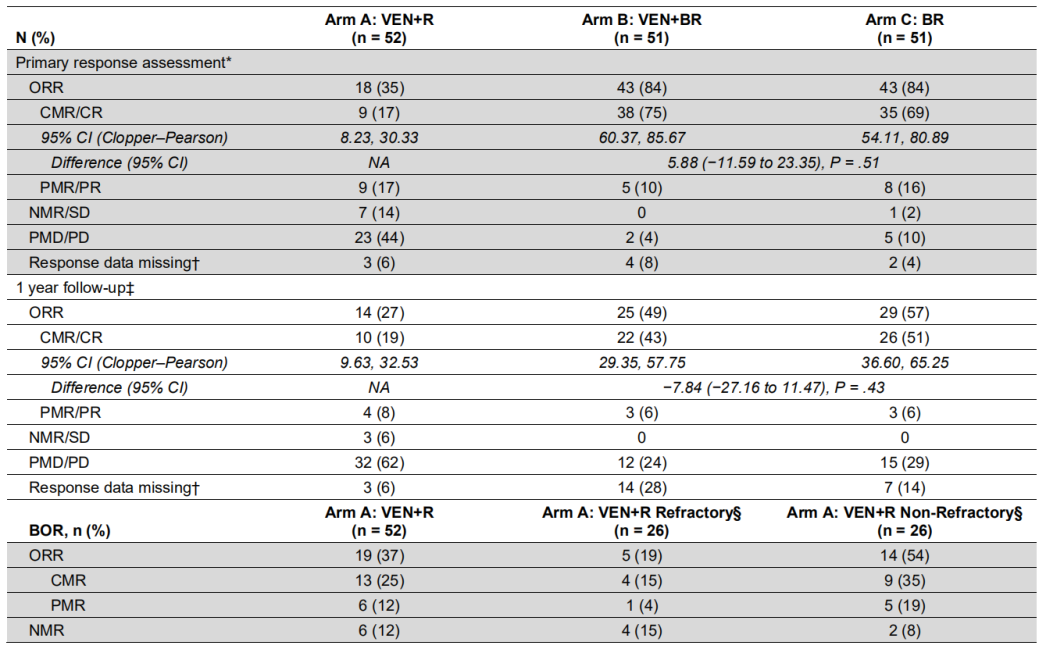
B组与C组的初始反应评估(PRA)的CMR/CR分别为75%和69%,治疗1年后的CMR/CR分别为43%和51%,1年后两组的ORR分别为49%和57%。相比之下,A组患者PRA的ORR较低,为35%,1年后A组患者的ORR为27%。A组患者中部分难治患者的缓解率低于非难治的患者。A组的CMR结果显示,非难治患者为35%,难治患者为15%,而B、C两组中难治和非难治患者没有统计学差异。
表2 三组缓解率
对B组和C组进行18个月的中位随访,B组和C组DOR的风险比为0.69(95% CI,0.38~1.27);两组中位PFS结果相似(HR, 0.69; 95% CI, 0.38~1.24)。A组的中位PFS为6.6个月。
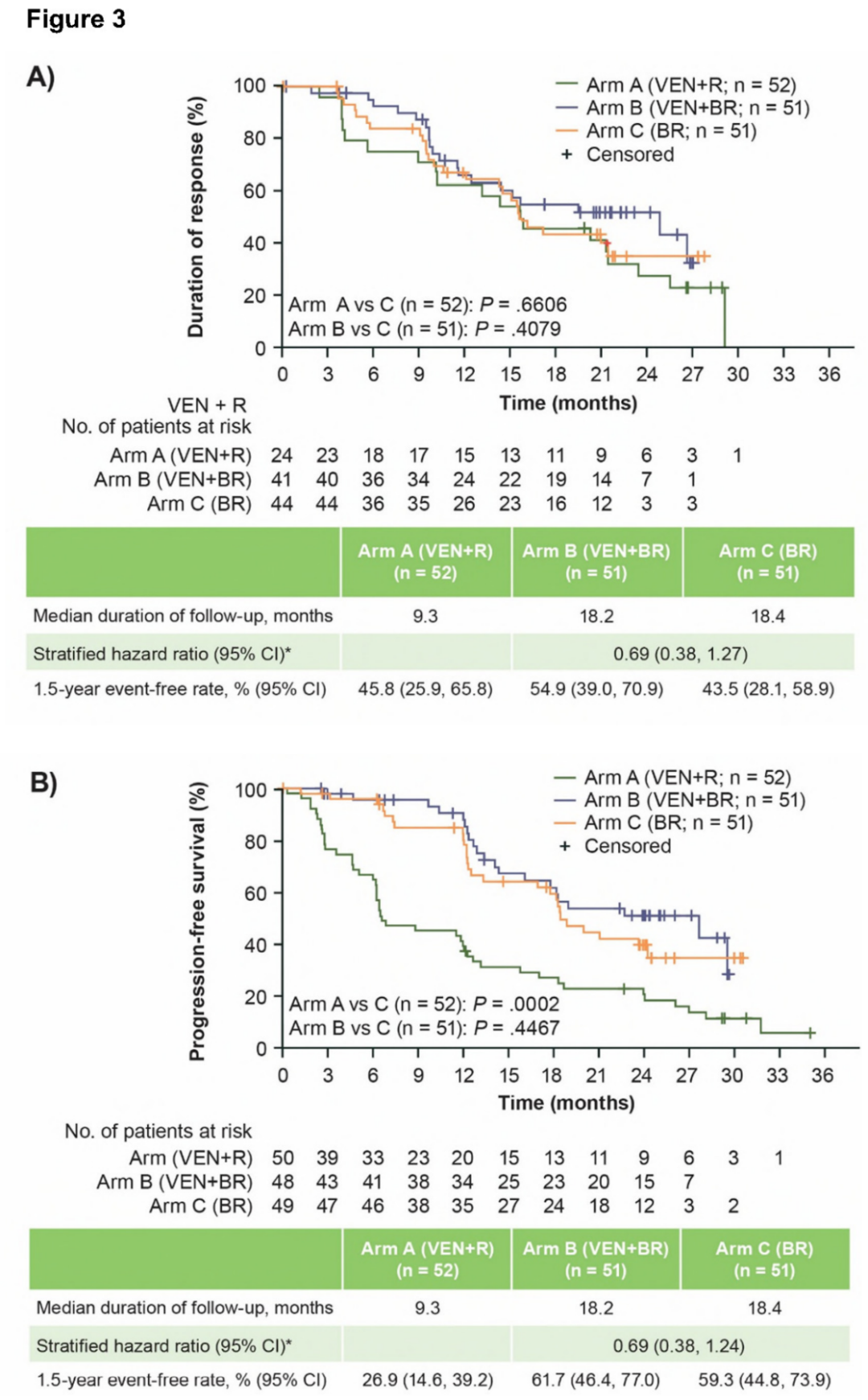
图3 DOR和PFS分析
安全性
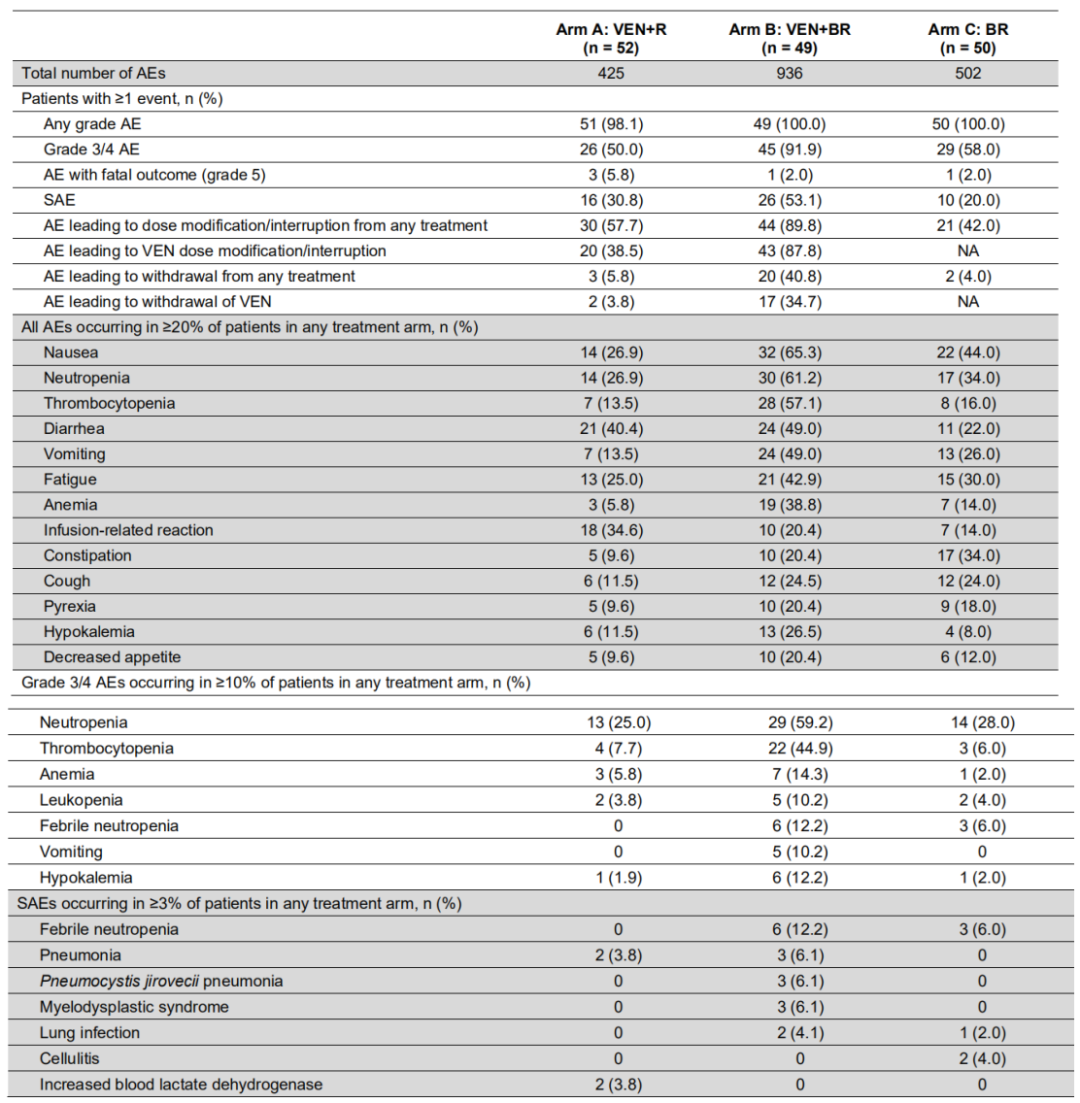
98%的A组患者和所有B、C组患者发生至少1次不良事件(AE),55例患者发生过至少1次严重的AE,其中B组发生率最高,为53.1%。103例患者(42.9%)至少出现了1次3~4级AE,最常见的是中性粒细胞减少和血小板减少。
在5例致死性AE中,A组中出现3例(肺出血、结肠炎、心肌梗死),均被认为与研究治疗无关;B组中出现1例(肺炎),被认为与研究治疗相关;C组中出现1例(肺栓塞导致的缺氧),被认为与研究治疗无关。
63例患者出现AE相关的VEN剂量调整或中断,其中A组20例患者主要由于中性粒细胞减少和腹泻,B组43例患者主要由于中性粒细胞减少和血小板减少。
表3 不良事件
研究结论
大多数接受VEN+ R治疗的患者都是疾病晚期,或进行了大量的预处理,1/3的患者对R耐药,难以持续治疗。与A组总体人群相比,部分非难治的患者有更好的反应率和MRD阴性率。B组和C组患者的CMR/CR率无显著差异,但B组的毒性相对较高,这表明患者对于B组给定的剂量和时间方案的耐受性有限。总之,VEN+R无化疗方案对复发/难治性FL的疗效良好,毒性尚可,值得进一步研究;VEN+BR联合方案导致毒性增加,化疗剂量和/或组合的优化仍有待探索。