一种VEGFR多肽疫苗对二型神经纤维瘤病取得初步疗效

二型神经纤维瘤病(Neurofibromatosis type 2,NF2)是常染色体显性遗传病,本病是由染色体22q12上的NF2基因突变引起,特征性临床表现是双侧前庭神经鞘瘤。另外患者好发脑膜瘤、室管膜瘤等中枢神经系统肿瘤。目前对NF2尚无根治手段,以手术和立体定向放射外科治疗为主,但术后肿瘤常继续生长,而立体定向放射外科不适用于体积较大的肿瘤。既往研究表明,血管内皮生长因子VEGF单克隆抗体贝伐单抗可使NF2患者的肿瘤得到控制,听力获得改善。然而贝伐单抗也存在用药频繁、副作用明显、耐药后快速进展等问题。多肽疫苗免疫疗法的目的是通过注射多肽抗原来激活患者体内的细胞毒性T淋巴细胞(CTLs)。最近发表的一项临床研究利用VEGF受体多肽疫苗对7例NF2患者进行治疗,证实了该疗法的安全性并取得了初步的疗效。
本研究由日本庆应义塾大学医学部开展,共入组7名存在进展性前庭神经鞘瘤的NF2患者,基因组DNA分型为:HLA-A*2402型(5例),0206型(1例),0207型(1例)。1名患者既往曾接受贝伐单抗治疗。VEGFRs多肽疫苗剂量为2mg每剂(包含VEGFR1和VEGFR2多肽),在腋下和腹股沟皮下注射,前4次每周注射1次,后4次每月注射1次,共8次。所有患者均完成8次接种。接种后所有患者可诱导特异性CTL,其中6例患者诱导VEGFR1和VEGFR2特异性CTL,而1例患者仅诱导VEGFR1特异性CTL。3名患者在最后一次免疫后7个月仍可检测到VEGFR2特异性CTL。
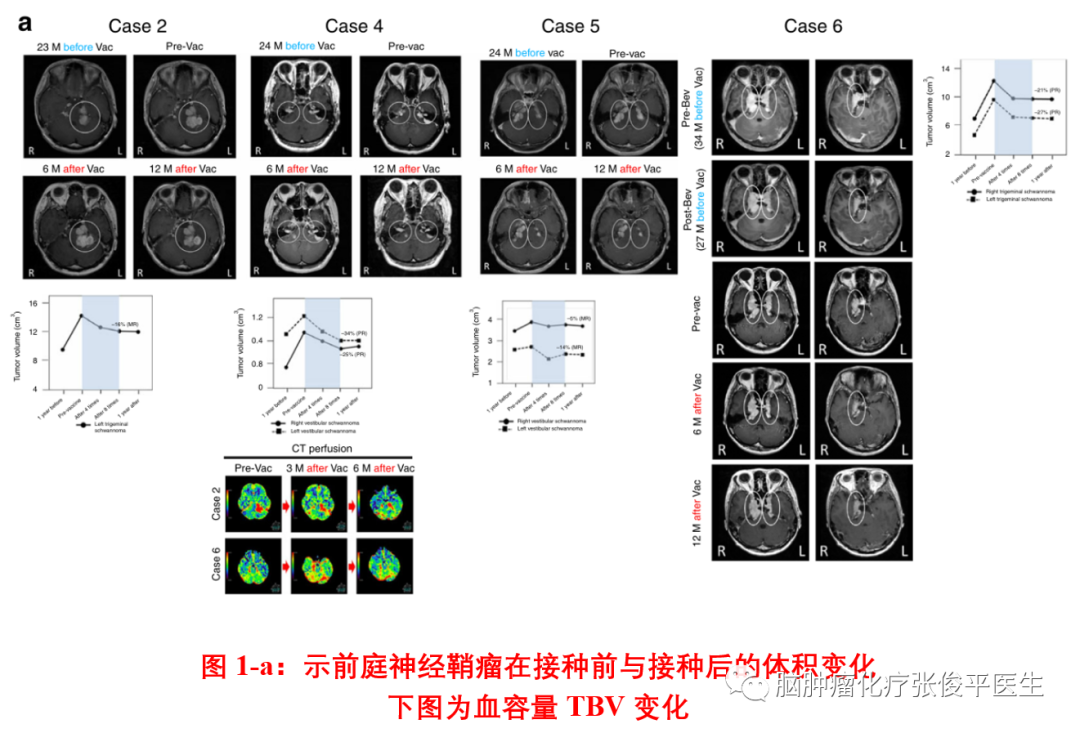
本研究的主要研究目的是评价安全性,次要研究目的是评价治疗后肿瘤体积、听力和免疫反应的变化情况。在安全性方面,5名患者在注射部位出现1级或2级局部皮肤反应,出现硬化、发红和肿胀。无局部溃疡、伤口延迟愈合或消化道出血。4名患者出现1级或2级中性粒细胞减少和贫血。1名患者出现1级高血压。1名患者出现与治疗无关的3级憩室炎。值得注意的是,有1名患者在最后一次接种后五个月出现5级蛛网膜下腔出血,回顾影像学资料提示该患者左颞叶周围存在硬膜动静脉瘘,可能是出血的原因。经孤立委员会评估与疫苗治疗无关。在疗效方面:①言语识别率WRS:在5个可评估的病例中,有2个(40%)观察到WRS有所改善,其余3例无改善。②纯音测听PTA:全部14个可评价耳中,13个PTA无变化,有1名患者的右耳PTA恶化。③神经鞘瘤体积变化:2名患者有单侧及以上的前庭神经鞘瘤达到PR(定义为体积减小达到20%),另外5名患者达到MR(定义为体积减小5%~19%)。另外在全部23个神经鞘瘤中,PR 4例,MR 11例,SD 7例,PD1例(为囊性肿瘤)。肿瘤体积的增长率均明显降低(接种前1年平均39.75±27.74%,接种后1年平均−4.67±15.86%,p=0.0087)。TBV(肿瘤血容量)分析显示,5个肿瘤下降>30%,5个肿瘤下降10%-30%,3个肿瘤上升>10%。④脑膜瘤体积变化:MR2例,SD 1例,PD 1例。肿瘤体积增长率降低。TBV分析显示,1个肿瘤下降>30%。其余肿瘤在治疗过程中无明显下降。
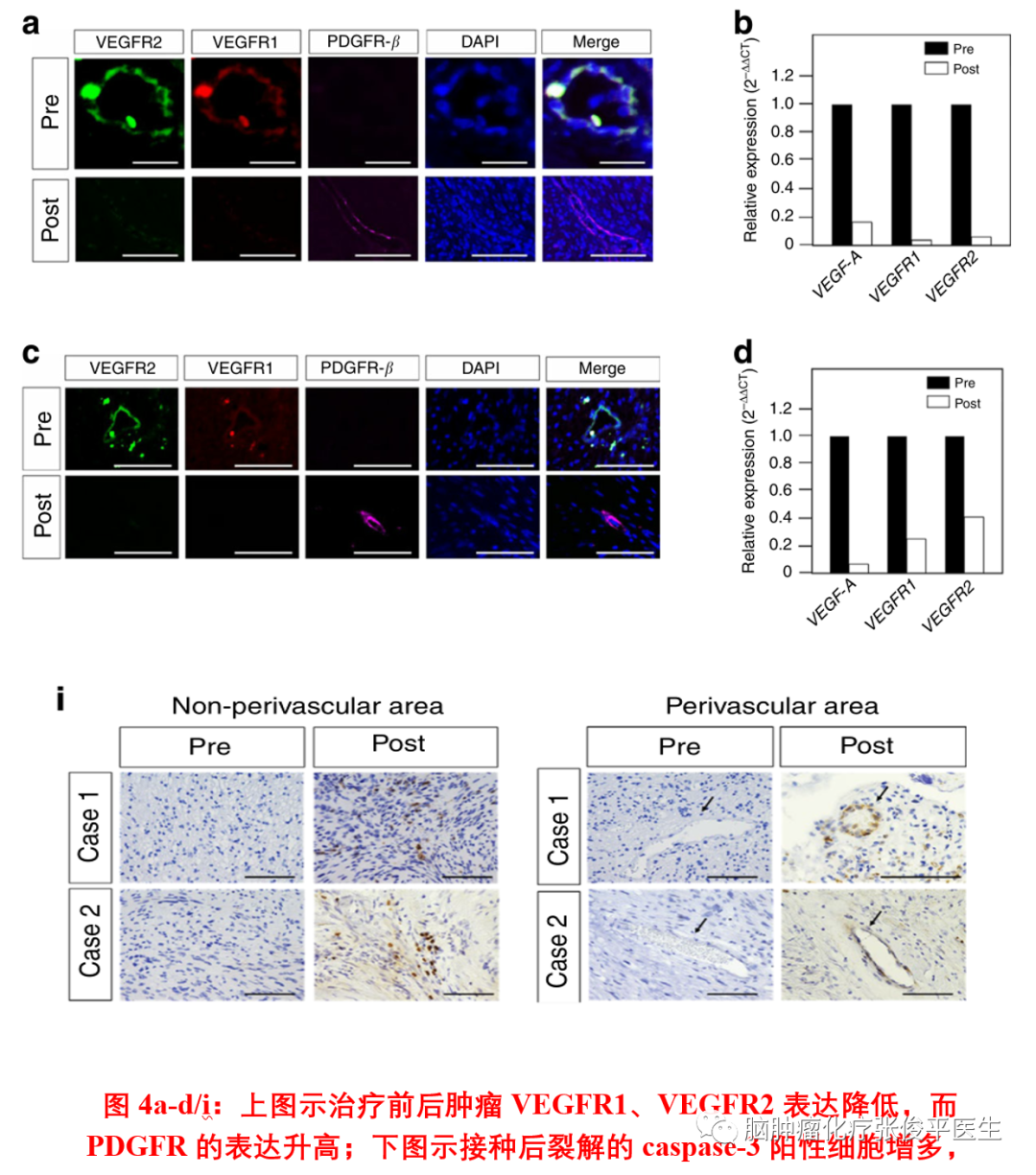
组织病理学研究发现,肿瘤血管在接种前显示较强的VEGFRs表达,无PDGFR-&β;阳性血管周细胞。相反,接种后的肿瘤血管VEGFRs呈阴性或轻度表达,并被PDGFR-&β;阳性的血管周细胞覆盖。VEGF-A在接种后的表达也低于接种前。另外经qPCR分析,肿瘤中VEGF-A和VEGFRs相关基因的表达水平在接种后低于接种前。虽然接种后CD8阳性细胞的总数没有明显变化,但血管周围区域的CD8阳性细胞的数量增加,且肿瘤组织中检测到大量弥漫裂解的半胱天冬酶3阳性细胞,这表明疫苗诱导了肿瘤和肿瘤血管的凋亡。上述现象提示接种疫苗后神经鞘瘤中VEGFRs表达减少,MVD减少,血管结构正常化和周细胞恢复,另外疫苗诱导的特异性CTL介导的杀伤效应可促进肿瘤细胞凋亡。
本研究提示,利用VEGFR多肽疫苗对NF2患者进行免疫治疗可诱导CTL的生成,且未观察到与疫苗相关的严重不良事件。接种疫苗后神经鞘瘤体积以及增长速率的减小与既往应用贝伐单抗的疗效相当。另外,该疗法可改善患者的WRS并提升生活质量。本研究的局限性是样本量有限,后续应对更多患者开展研究以证实多肽疫苗对NF2患者良性肿瘤的治疗效果。
参考文献:
Ryota Tamura et al. A VEGF receptor vaccine demonstrates preliminary efficacy in neurofibromatosis type 2. Nature Communications.(2019)10:5758