生化妊娠
生化妊娠:指发生在妊娠5周内的早期流产,血中可以检测到HCG( 人绒毛膜促性腺激素 )升高,大于25mlU/mL或者尿妊娠试验阳性,但超声检查看不到孕囊,提示受精卵着床失败,又被称为“亚临床流产”。
正常情况下在排卵12天后就试纸可以测出弱阳性,有部分人隔天能测出试纸颜色加深,还有部分是每天都有明显加深。如果连续3天以上没有任何加深的趋势,这个胚胎一般都有问题。
一般似这种情况为胚胎本身质量的不好,或者受精卵结合是偶尔的染色体变异,或者自然的优胜劣汰。一些妇女在做试管婴儿时这种情况比较常见。但是大部分妇女因为没有上医院检查,自己也没在意,就会把它当做月经推迟忽略过去,其实已经是自然流产了。适龄妇女遇到这样的情况不要惊恐,这是大自然淘汰的结果,一般不会影响下一次的怀孕。如果多次发生这样的情况,就要上医院做进一步检查了。
生化妊娠属于亚临床流产,应该与其他由于疾病或意外事故的流产相鉴别。如果是生化妊娠,偶尔一次,不会有大的影响。转经后就可以恢复正常,不影响以后怀孕。
孕酮(PRGE)和人绒毛膜促性腺激素(THCG) 都是妊娠的一个指标,检查结果出现明显的降低,同时有阴道流血,就可以诊断为自然流产。
生化流产的原因有哪些,影响受精卵着床的因素:
1.受精卵本身有缺陷;
2.卵巢黄体功能不健,孕酮分泌不足,子宫内膜异常,影响受精卵的着床;(检查激素六项)
3.子宫因素:子宫发育不良、子宫粘膜下肌瘤、子宫内膜息肉、宫腔粘连、子宫内膜结核等影响受精卵着床;
4.免疫因素:近年来对免疫因素的研究,认为有两种免疫情况影响受孕。
a同种免疫:精子、精浆或受精卵是抗原物质,被阴道及子宫上皮吸收后,通过免疫反应产生抗体物质,使精子与卵子不能结合或受精卵不能着床;
b自身免疫:认为不孕妇女血清中存在透明带自身抗体,与透明带起反应后可防止精子穿透卵子,因而阻止受精;
5.中医调养:如果上述检查均正常就要看看中医能不能发现问题;
6.精神过度紧张,尤其是因未孕而严重的焦虑,心理压力过大。
.ZZY能测到弱阳,但很难达到阳,更不可能到强阳。
2.B超看不到宫内有孕囊。
3.血HCG值很低,只能说明是怀孕了,但不能说明是否着床成功。
4.一般不会超过50天便会自然流产。会有灰白色膜状物流出。
单因素分析
年龄、取卵日子宫内膜厚度、HCG注射日的E2水平及排卵障碍对妊娠结局的影响有统计学意义 (P<0.05) ;其它不孕因素(输卵管炎、内异症、男方因素) 、卵巢反应性、Gn总量、Gn天数、获卵数对妊娠结局的影响无统计学意义 (P>0.05)
笔记一:
随着医学科学的发展, 实验室水平的提高, 辅助生殖技术的日趋成熟, IVF-ET给无数不育夫妇带来了福音, 在其普遍开展带给众多不孕夫妇无限希望的同时, 其临床妊娠率仍然不能令患者满意。IVF-ET的结局受IVF-ET过程中临床和实验室等各方面因素直接或间接的影响, 多年以来, 国内外众多生殖医学工作者都希望通过寻找影响因素, 探究其作用机理, 进而对影响因素进行处理达到改善IVF-ET结局的目的。现阶段的研究对IVF-ET过程中单因素与妊娠结局的关系探讨较多, 而综合考虑多因素间相互作用后与妊娠结局的关系报道较少。目前认为接受IVF-ET治疗患者的年龄较大, IVF-ET过程中胚胎的质量、实验室的培养环境、人为的控制内分泌水平变化和胚胎着床的条件等都可能导致不良IVF-ET结局的发生。
年龄因素
年龄是影响女性生育能力的重要因素, 这一点是受到各研究者公认的。Terriou[1]等回顾分析了10 000个移植周期, 认为35岁以后着床率明显下降。Ziebe[2]等发现, 年龄每增长2.3岁获卵数下降1个, 着床率每10年下降0.8%, 临床妊娠率每年下降0.5%。该文通过多因素Logistic回归分析显示的结果与以上观点相似, 年龄在IVF-ET中与妊娠成功率成负相关, 年龄<35岁者正常分娩率为56%, 年龄>35岁者正常分娩率仅为38%, 因此进一步说明了女性生育能力随着年龄的增长逐渐减弱。
目前认为高龄妇女妊娠率降低的主要原因是, 随着年龄的增长, 尤其是36岁以后, 卵巢体积逐渐发生变化、卵巢的储备能力及反应性下降、卵巢间质血管分布改变等导致的卵子质量的下降[3], 可能与卵子染色体异常的产生增多、卵子的线粒体数量减少、卵胞浆ATP含量下降和卵子的细胞调亡增多有关。卵子处于第一次减数分裂的静止期可长达45年, 但随着时间的延长, 过氧化物对卵子的破坏造成非整倍体卵子的增多及卵细胞的凋亡现象也愈明显。其次, 随妇女年龄的增长卵巢功能降低, 获卵数减少, 可供移植的优质胚胎数减少, 从而间接降低临床妊娠率。此外, 高龄妇女生殖器逐渐退化, 子宫内膜容受性降低[4]也是导致临床妊娠率下降的另一个原因。随年龄增加, 子宫内膜在形态上和功能上发生一系列改变:在形态上出现胶原含量增加, 内膜细胞中雌激素受体减少;在功能上, 子宫血流量和可产生蜕膜的容积可能减少。这些变化都可能导致妊娠率的下降。
年龄已作为衡量IVF-ET结局的重要预测指标之一,随着年龄的增长,女性卵巢功能减退,卵子质量和子宫内膜容受性降低,胚胎非整倍体率增加,胚胎存活率逐渐降低,是造成临床妊娠率下降和生化妊娠率增加的重要原因[2] 。人卵母细胞的细胞遗传学分析表明,卵母细胞非整倍体的增加与女方年龄有直接的关系 。25岁以下女性卵子的非整倍体率约为5%,30岁左右约为10%~25%,大于40岁则高达50%以上 。非整倍体发生的主要机制涉及在减数分裂Ⅰ期和Ⅱ期染色体不分离,以及减数分裂Ⅰ期后姐妹染色单体的过早分离。Grande等研究亦发现胚胎染色体异常发生率随母亲年龄的增加而增加。针对年龄对卵子线粒体功能的影响,有研究发现高龄妇女卵子的线粒体DNA突变率增高 ,卵子中线粒体功能的缺陷使得能量如ATP等生成减少,卵子形成尤其是核纺锤体活性和染色体分离受到影响,并进而导致非整倍体的增多,且ATP生成减少亦会使胚胎种植潜能降低,这些都可能导致高龄妇女临床妊娠率降低。
有文献报道,女性>35岁卵巢储备迅速减少,生育能力呈指数型下降。杨雪等的研究显示,年龄≤35岁组妊娠率为33.9%,>35岁组妊娠率则为13.0%。而Jackson等的研究显示,高龄不育妇女生育力明显下降大约在37~38,到45岁左右生育几率更低。文献报道的高龄助孕妊娠率约为20%。
子宫内膜因素
子宫内膜的容受性受子宫内膜厚度、组织结构及血流的影响, 子宫内膜厚度是反映子宫内膜容受性的主要指标。Basir[5]等发现在IVF-ET周期中, HCG注射日子宫内膜厚度>8 mm的妊娠率比子宫内膜厚度<8 mm的妊娠率高。该资料逻辑回归分析显示取卵日的子宫内膜厚度与妊娠成功率成正相关, 生化妊娠丢失组和临床妊娠流产组分别与足月分娩组比较时, 子宫内膜厚度的差异有统计学意义, 足月分娩组的子宫内膜厚度明显高于前两组。因此, 可以认为在胚胎着床及发育过程中, 一定的子宫内膜厚度是妊娠成功的关健因素之一。一定厚度的子宫内膜在形态学上胶原含量相对减少, 内膜细胞中雌激素受体相对增加;在功能上子宫血流量和可产生蜕膜的容积增多, 子宫内膜容受性升高, 着床率相对增加。在IVF-ET工作中, 超促排卵所引起的高雌激素水平可以增加子宫内膜厚度, 提高子宫内膜容受性, 有可能提高着床率和临床妊娠率。
育龄期女性的子宫内膜在月经周期中随体内激素变化而呈现出不同的影像特征,根据Gonen分型标准分为3种形态:排卵前在雌激素作用下,内膜增厚、血管间质也增多,形成增殖期内膜,超声显示为外层和中央为强回声,内层呈低回声,宫腔中线回声明显的三线征,为A型;排卵后内膜受孕激素影响,分泌活动旺盛而使回声增强、均质,厚度进一步增加,中央孤立回声和子宫肌层回声一致,宫腔中线回声不明显者为B型;均质强回声,无宫腔中线的回声为C型。
目前子宫内膜类型与妊娠结局之间的关系尚不确定。Jarvela等的研究发现内膜类型与临床妊娠有关系,并有学者认为,卵泡晚期内膜类型在一定程度上可以预测妊娠结局。赵静等的研究显示A、B、C型内膜组的胚胎着床率依次降低,差异比较具有显著性(P<0.05)。陈玲等的研究发现排卵前不孕组的A型子宫内膜(28/46.7%)明显少于正常对照组的A型子宫内膜数(37/67.1%),而B型和C型子宫内膜均高于正常对照组的相应类型,提示排卵前A型子宫内膜是受孕成功的内膜容受最佳类型。本研究结果显示,子宫内膜类型由A型到C型,每增加1个级别,生化妊娠发生的比数比例为1.976,即A、B、C型子宫内膜对应的生化妊娠的发生率依次升高。因内膜主要受体内雌孕激素调节,推测这可能与激素水平的变化、子宫内膜血管生成和血管舒张能力改变有关。然而汤惠茹等的研究表明,取卵日B型内膜更利于胚胎着床(P<0.005),也有文献报道子宫内膜类型不能预测妊娠结局。故子宫内膜类型对妊娠结局的影响还需大样本的进一步研究。
HCG注射日血清E2水平
HCG注射日过低的E2水平表明患者对控制性超促排卵的反应差, 患者卵巢储备少, 获卵数少, 可供移植的胚胎数量少, 往往导致较差的妊娠结局, 这一点已获得多数研究者的认同。一致认为, 获卵数≤4个, HCG注射日E2<500 pg/ml或平均每日促性腺激素(Gn) 剂量≥300 IU, 总Gn用量≥44支, Gn刺激时间≥15天, 是卵巢反应不良的表现, 而卵巢反应不良则往往提示有卵巢储备功能的降低。血清E2水平在HCG注射日明显升高, Simon[6]等学者认为胚胎着床前血清E2水平过高≥2 997 pg/ml不利于胚胎种植, 但是对胚胎质量无影响。而钟依平[7]等报道HCG注射日血清E2水平并非影响IVF-ET妊娠结局的因素。
该资料的研究显示, HCG注射日血清E2水平对妊娠结局的影响有统计学意义, Logistic回归分析表明, HCG注射日的E2水平与妊娠成功率呈正相关, 可能是因为过低的雌激素使子宫内膜发育不全, 影响胚胎着床和胚胎发育, 从而导致生化妊娠率和临床流产率较高。而适量的雌激素, 促使子宫内膜上皮和间质增殖发生蜕膜样变, 为胚胎着床及其后的发育提供良好的条件。但也有研究发现, 过高的E2有溶黄体的作用, 也干扰孕激素对子宫内膜的作用, 抑制子宫内膜种植窗口胞饮突的形成[8], 使子宫内膜的容受性下降, 此观点在该文中并未得到证实, 原因可能是各种因素的交互作用减弱了单个因素对妊娠结局的影响。
排卵障碍
该研究在单因素分析中显示排卵障碍对妊娠结局的影响有统计学意义(P=0.045) , 但Logistic回归分析中并未发现排卵障碍与妊娠结局之间的相关性。分析其原因可能为该因素与患者的卵巢反应性及其它不孕因素间存在交互作用。但从该文结果及临床角度来看, 排卵障碍可认为是影响IVF-ET后妊娠结局的因素之一。
优胚率对生化妊娠的影响
谭秀群等的研究中,PCOS患者分别采用拮抗剂方案和长方案,两组优胚率比较(拮抗剂组:50.14±25.27,长方案组:56.04±25.06)差异无统计学意义(P>0.05)。关于单一优胚率对妊娠结局的影响,国内外研究尚较少,本研究显示,优胚率是生化妊娠发生的保护因素,优胚率≥0.5对优胚率<0.5的生化妊娠发生的比数比例为0.339。
移植胚胎数对生化妊娠的影响
我国卫生部颁布的《人类辅助生殖技术管理办法》中规定自2003年10月起,年龄小于35岁的患者第一次移植胚胎数目不得超过2枚,年龄≥35岁或者第二次移植的患者可以移植3枚胚胎。陈华平等的研究显示,移植3个胚胎的临床妊娠率(41.01%)高于移植2个胚胎组(28.75%),差异有显著性(P<0.05)。张雪等的研究也发现移植1个、2个、3个及以上冷冻解冻胚胎的妊娠率分别为9.29%、19.21%、37.32%,其中移植3个及以上胚胎者的妊娠率高于移植1个和2个胚胎者的妊娠率(P<0.05)。本研究结果与之相似,移植胚胎数>2个对移植胚胎数≤2个的生化妊娠发生的比数比例为0.410,即移植3个及以上胚胎可相对移植1个或者2个胚胎可降低生化妊娠的发生率,从而提高妊娠率。但江楠等的研究结果显示,冻融胚胎移植周期中,年龄<35岁妇女移植胚胎数量从3个减少至2个,临床妊娠率并没有显著降低,这与国外Wang等及国内宋韬等的报道一致,并且与文献报道的新鲜胚胎移植周期结果也相符。Dean等认为导致不同结论的原因可能与胚胎质量有关。
移植后4天E2值对生化妊娠的影响
按照胚胎发育及着床的规律,在IVF-ET过程中,受精卵的植入约于受精后第5-6天开始,第11-12天完成,如果移植在体外培养3 d的胚胎,则胚胎着床约发生在ET后的第4-5天。目前,关于血清E2、P值的研究多集中于HCG注射日、取卵日、移植日等时间点,关于移植第4天的激素水平是否与妊娠结局有关,国内外的大样本研究还很少。有国外学者证实,在IVF/ICSI周期黄体期的第3天血清E2、P的值,妊娠组高于未妊娠组。Ganesh等的研究结果与之相似,发现黄体中晚期E2水平的上升预示更高的妊娠率,而E2水平下降,则提示较低的妊娠率。本研究结果提示,移植后4天E2值是生化妊娠的保护因素,移植后4天E2值≥100pg/ml对移植后4天E2值<100pg/ml的生化妊娠发生的比数比例为0.130,即移植后4天E2值≥100pg/ml有利于降低生化妊娠的发生率,从而提高妊娠率及活产率。而毛增辉等的研究显示ET后第4天妊娠组与未妊娠组E2、P浓度没有明显差别。有研究证实,在着床后l d即可检测到由囊胚的滋养层细胞分泌的HCG,并在种植后大量合成,可强有力的刺激黄体分泌E2、P等,故认为此是由于胚胎着床刚刚完成或者尚未完成,黄体分泌功能尚未复苏所致。因此,移植后4天的E2水平是否能够影响妊娠结局尚不确定,需要进一步的研究。
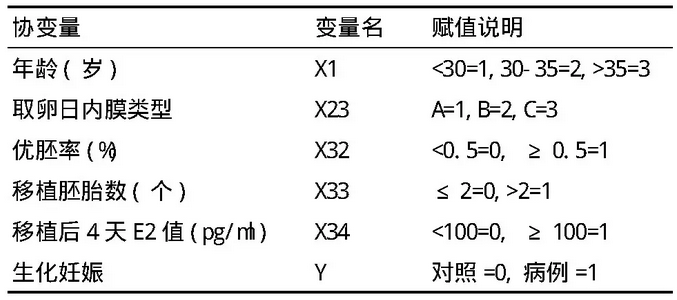
生化妊娠发生的部分相关因素赋值
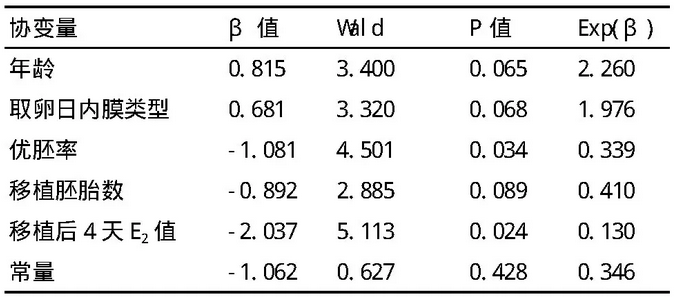
对生化妊娠结局影响最显著的协变量
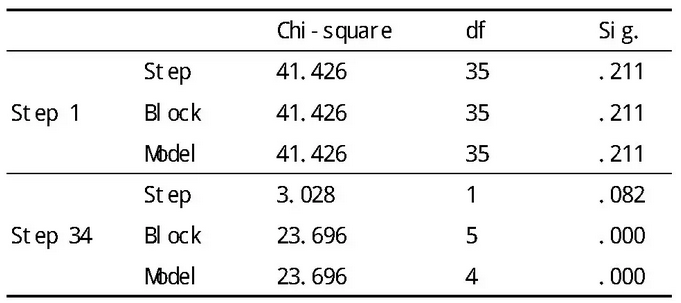
Omnibus Tests of Model Coefficients
既往生化妊娠率
192例中, 既往无生化妊娠病史66例, 有1次生化妊娠65例, 有2次生化妊娠42例, 有3次生化妊娠14例, 有4次生化妊娠5例。192例既往共有1 047次妊娠, 其中生化妊娠211例(20.15%) 。
既往自然流产次数及IVF-ET自然流产率
C组既往自然流产次数(P<0.05) 及既住IVF-ET自然流产率(P<0.012 5) 均显著高于A组及B组。A组与B组比较, 既往自然流产次数(P>0.05) 及既往IVF-ET自然流产率(P>0.012 5) 差别均无统计学意义。

3组患者的年龄、BMI、既往自然流产次数及既往IVF-ET自然流产率比较Tab 1 Comparison of age, BMI, the number of previous spontaneous abortion and the rate of previous spont
BMI:体质量指数;IVF-ET:体外受精和胚胎移植.A组:无生化妊娠组;B组:1次生化妊娠组;C组:≥2次生化妊娠组.与C组比较, ☆:P<0.05, △:P<0.012 5.
保胎治疗后妊娠结局
截止至2017年1月, 192例中妊娠者172例, 其中A组61例, B组56例, C组55例。黄体酮保胎治疗后, C组的活产率显著低于A组及B组(P<0.012 5) , 自然流产率及SANK率显著高于A组及B组(P<0.012 5) ;A组与B组比较, 活产率、自然流产率及SANK率差别无统计学意义(P>0.012 5) 。3组的生化妊娠率及SAAK率差别无统计学意义 。

3组妊娠结局的比较Tab 2 Comparison of pregnancy outcomes among three groups
SANK:正常染色体核型;SAAK:异常染色体核型.A组:无生化妊娠组;B组:1次生化妊娠组;C组:≥2次生化妊娠组.与C组比较, △:P<0.012 5.
受精卵形成及着床是胚胎早期发育的2个重要过程, 任何干扰此过程的因素均可导致不孕或早期流产。受精卵着床经过定位、粘附和侵入3个过程。生化妊娠主要发生于受精卵着床开始至完成前, 临床上可表现为血或尿HCG高于正常值, 但超声检查宫腔内外均未见到孕囊, 随后妊娠自然终止。Wilcox等报道, 首次测得HCG阳性为着床开始, 多于排卵后6~12d出现, 着床延迟与生化妊娠相关。有研究报道, 生化妊娠的发生率为8%~33%。结果显示, RSA患者的生化妊娠率为20.15%。生化妊娠的病因尚不十分清楚, 胚胎质量差或子宫内膜容受性低下是最主要的原因。
生化妊娠及URSA诊疗已成为生殖医学研究的热点。目前认为流产次数越多, URSA发生率越高。既往自然流产次数越高, IVF-ET自然流产率就越高, 既往有>3次自然流产史的患者, 行IVF-ET自然流产率为34%。本研究结果显示, ≥2次生化妊娠组的既往自然流产次数及IVF-ET流产率均显著高于无生化妊娠组及1次生化妊娠组;而无生化妊娠组与1次生化妊娠组间2个指标的差别则无统计学意义。提示既往≥2次生化妊娠组的复发性流产率更高。因此详细询问URSA患者的既往生化妊娠病史对于临床评估具有一定参考价值。但其具体机制尚有待于进一步研究。
同时该研究对入组患者均根据病情给予黄体酮保胎治疗, 并对其妊娠结局进行前瞻性研究, 结果显示, ≥2次生化妊娠的URSA患者与0~1次生化妊娠的URSA患者比较, 前者的活产率较低, 自然流产率较高;而无生化妊娠组与1次生化妊娠组比较, 活产率及流产率差别则无统计学意义。提示重复生化妊娠史的URSA患者生殖能力降低。有研究报道, 既往有生化妊娠史的女性, 行IVF后自然流产率高于无生化妊娠史的女性[7,8]。本研究结果与之相似。同时笔者对于妊娠结局为自然流产的患者进一步行绒毛染色体核型分析, 结果显示, ≥2次生化妊娠组SANK发生率显著高于0~1次生化妊娠组, 但3组间的SAAK发生率差别无统计学意义。因本研究病例数较少, 有待扩大样本量进一步验证。
综上所述, 既往≥2次生化妊娠的患者复发性流产更为严重, 保胎治疗后其活产率较低, 自然流产和SANK风险较高。因此, 对于既往存在≥2次生化妊娠病史的URSA患者, 临床医师应予以高度重视。而探讨生化妊娠与URSA之间的相互关系及作用机制, 研究有效的治疗方法, 对于提高活产率、降低流产率极为重要。
着床失败、生化妊娠和流产
辅助生殖技术作为治疗不育症的一个有效手段, 近几年在国内外得到了广泛应用, 虽然妊娠率不断提高, 但体外受精-胚胎移植(IVF-ET) 失败仍占较大比例, 这其中包括着床失败、生化妊娠、流产以及异位妊娠。其中, 不明原因的着床失败和复发性流产备受关注, 而生化妊娠在自然受孕和IVF人群亦有较高的发生率。对于临床医生和患者来说, 着床失败、生化妊娠和流产都意味着IVF-ET治疗没有获得预期结局, 但这三者是一码事吗?
要说清楚这个问题, 有必要重温着床的概念。着床(implantation) 是指处于活化状态的胚泡与处于接受态的子宫相互作用, 最后导致胚胎滋养层与子宫内膜建立紧密联系的过程, 而着床失败是指胚胎与子宫内膜在建立这种紧密联系的过程之前的某个环节发生异常, 导致胚胎不能着床。生化妊娠是指胚胎已经开始着床, 滋养外胚层侵入子宫蜕膜层, 胚胎分泌的β-HCG进入母体血液并达到可检测出的水平, 只是之后由于某种原因, 妊娠没有继续, 血或尿中的β-HCG只是一过性的升高。之所以叫生化妊娠, 是指妊娠仅进行至用生物化学方法可以检测到的阶段, 没有发展至能用超声诊断出孕囊的阶段, 可算是早期妊娠丢失(First TrimesterPregnancy Loss, FTPL) 的一种特殊类型。流产则是发生在胚胎着床以后的事件, 是临床妊娠的丢失。因此, 着床失败、生化妊娠和流产均属于胚胎或妊娠丢失的范畴, 但发生在不同的生理阶段, 不是一码事。
导致着床失败、生化妊娠和流产的原因也是不同的。
在胚胎发育和着床过程的任何一个阶段发生异常均有可能导致着床障碍。着床失败实质上是由比较复杂的病因导致的, 由于着床过程极为复杂并且受到诸多因素的精细调控, 现阶段还不可能明确每一例着床失败的确切病因, 其主要由母体因素、胚胎因素以及二者间对话异常所致。母体因素包括子宫内膜容受性降低(宫腔结构异常、输卵管积水、内膜菲薄或形态欠佳、内膜容受性相关分子表达异常等) 、免疫学异常、高凝状态或易栓症等;胚胎着床能力下降主要是由于胚胎染色体异常、非整倍体胚胎、不良的培养环境等导致的;而胚胎与内膜的对话开始达成免疫相容和新生血管形成, 从而完成种植过程, 二者间的对话异常可能导致着床失败的发生。
在着床和早期胚胎发育过程中, 母体和胎儿组织间的免疫相容和免疫排斥是一个动态平衡的过程, 任何干扰因素打破了这种平衡, 都可能导致生化妊娠。虽然发生生化妊娠的相关影响因素可能是多方面的, 但发生机制目前仍不清楚, 可能与胚胎、内膜、免疫调节、促排卵方案等因素有关。Dick-ey等对81例患者排卵前内膜厚度与生化妊娠关系进行了研究, 发现HCG日或黄体生成素(LH) 峰日的内膜厚度<9 mm者生化妊娠的几率较高, 达到21.9%(7/32) , 而当日内膜厚度≥9 mm的患者无一例出现生化妊娠(0/49) , 差异有显著性(P<0.0025) ;而且生化妊娠的发生与内膜的类型有关, 当子宫内膜形态为三线型内膜时, 生化妊娠的发生率低(r=0.26, P=0.01) , 但与患者年龄、既往有流产史无关, 而临床妊娠后的流产则与患者年龄(r=0.26, P=0.01) 和既往流产史(r=0.25, P=0.013) 显著相关。因此, 他们认为大部分生化妊娠可能是由内膜因素所致, 可能是缘于解剖、免疫或其他原因所致的内膜容受性的降低, 而流产则主要是由胚胎遗传学缺陷导致, 二者的发生原因不同。近年来随着胚胎植入前非整倍体筛查(PreimplantationGenetic Screening, PGS) 的广泛应用, 为研究生化妊娠、流产的原因提供了帮助, 大多数关于PGS的研究认为经过染色体筛查后可明显降低FTPL, 但未降低生化妊娠率。2003年Troncoso等通过PGS筛选整倍体胚胎移植后, 对62例行PGS后妊娠病例与同期非PGS妊娠周期进行比较(非PGS周期有62例为D3胚胎移植, 62例为囊胚移植) , 三组人群生化妊娠比例分别为25.8%、24.2%和25.8%, 无显著差异(P>0.05) , PGS并未降低生化妊娠的发生。由此, 更进一步说明胚胎染色体异常不是生化妊娠的主因, 而内膜情况、促排卵方案等可能是其主要原因。而经过PGS筛选后, 早期流产率明显降低说明胚胎染色体异常是导致流产的主要原因之一。除此之外, 导致流产的原因还包括内分泌异常、自身免疫因素和感染因素等, 而中期妊娠的丢失多由于生殖道异常, 如宫颈松弛等因素导致。
IVF失败对于患者来说是一个很沉重的打击, 从满怀希望到梦想破灭, 其心理承受的沮丧和压力是可想而知的。对于他们来说, 除了面对这一次的失败结局外, 更关心的是如果接受下一次治疗, 成功的机会有多大。目前多数学者的研究都认为, 生化妊娠、流产是后续IVF治疗成功与否的阳性预测指标。De Neubourg等发现, 发生早期胚胎丢失的患者有更多的优质胚胎和冷冻胚胎, 下一次IVF更容易成功。Levy等的研究也发现, 和总的IVF人群相比, 生化妊娠、流产的患者下次能够继续妊娠的概率要明显增高。Pearson等对2, 245例患者IVF结局进行统计, 发现第一周期出现生化妊娠或流产者再行IVF获得活产的机会要高于第一周期着床失败者(分别为54.1%、61.4% 和46.5%) 。北京大学第三医院生殖中心2011年的资料(临床资料, 尚未发表) 也显示在新鲜移植周期发生着床失败、生化妊娠和流产的患者, 在随后的第一个解冻周期的临床妊娠率分别43.6%、51.7%和54.1%, 也表明前一个移植周期发生生化妊娠、流产是后续IVF治疗成功与否的阳性预测指标。
总之, 虽然IVF失败是医生和患者都不想见到的, 但是我们要仔细分析失败的具体原因。着床失败、生化妊娠和流产的产生原因、发生机制和发生过程都是不同的, 要针对不同情况做到个体化处理, 对症治疗, 为下一次的IVF治疗成功争取更大机会。
冻融囊胚移植周期生化妊娠相关因素一:
1983年首例冻融胚胎移植(frozen-thawed embryo transfer, FET) 成功妊娠, 之后随着技术的改进, 妊娠率逐渐提高, 尤其是玻璃化冷冻技术的成熟和广泛应用、囊胚移植的开展, 临床妊娠率高达50%以上, 但生化妊娠率仍高达12%~30%, 导致助孕失败, 增加患者的经济负担和心理压力。生化妊娠指胚胎已经着床, 但是由于某种原因妊娠终止, β-人绒毛膜促性腺激素(h CG) 只是一过性升高。目前对玻璃化冷冻囊胚解冻移植周期生化妊娠的报道较少, 发生机制尚不清楚, 因此我们回顾性分析了近3年发生的70例生化妊娠, 希望找到影响因素并采取针对性措施, 改善FET的助孕结局。
生化妊娠是早期妊娠丢失(first trimester pregnancy loss, FTPL) 的一种特殊类型, 在自然受孕的妇女中发生率为30%, 我们的数据显示冻融囊胚移植中发生率为15.05%, 与文献报道12%~30%相符。FET周期生化妊娠发生机制尚不完全明确, 可能与胚胎染色体异常(主要为非整倍体) ;母体内分泌、免疫等异常;环境中有毒、有害物质等有关。国内外研究较少, 尤其对胚胎染色体、环境因素的检测相对困难, 因此我们分析了临床常见的一些指标:患者一般情况、病史、内膜准备方式、冻融囊胚移植过程中的相关数据, 观察到女方年龄、SCH是FET周期生化妊娠的危险因素。
重视高龄女性患者
女性年龄越大, 卵母细胞线粒体、纺锤体老化和同源染色体不分离、姐妹染色单体过早分离越容易发生, 导致卵细胞染色体非整倍体发生率增加、胚胎质量下降, 进而导致妊娠率下降、生化妊娠率、流产率增加。我们的数据分析显示生化妊娠组年龄比正常宫内妊娠组高(P>0.05) , 与文献报道一致。我们进一步分析高龄导致生化妊娠是否与胚胎质量下降有关, 数据显示生化妊娠组有优质胚胎的周期所占比例比正常宫内妊娠组略低, 但差异无统计学意义。
可能的原因有:我们采用囊胚培养后FET, 一部分异常胚胎经过培养、冷冻、复苏后已经淘汰;形态学评分标准不能完全反映胚胎染色体是否正常及预测胚胎发育潜能, 形态学表现为优质胚胎的染色体异常发生率高达25%;即使对胚胎进行植入前非整倍体筛查(preimplantation genetic screening, PGS) , 选择染色体正常的胚胎移植, 也未降低生化妊娠率。可见高龄导致FET周期生化妊娠不完全与胚胎质量有关。
高龄女性生育力降低的另一个主要原因是子宫内膜容受性下降, 表现为子宫内膜血流和雌孕激素受体减少, 基质细胞中DNA含量降低[10]。临床评估子宫内膜容受性的指标有:子宫内膜厚度、分型、蠕动波、基底血流及子宫动脉血流指数等, 其中最简便的是子宫内膜厚度。有研究显示, 子宫内膜厚度<9 mm者生化妊娠发生几率升高。我们的研究显示生化妊娠组与正常宫内妊娠组子宫内膜厚度无统计学差异, 可能与我们对内膜<8 mm的周期取消移植有关。在今后的工作中有必要进一步研究两组患者的子宫内膜蠕动波、血流指数等。
重视高龄不孕患者, 促排卵前尽量改善卵母细胞质量, 移植前尽量改善子宫内膜容受性有望降低生化妊娠率。
FET前重视甲状腺功能检查并纠正SCH可减少生化妊娠
SCH患者无明显临床症状, 主要依靠实验室检查来诊断。不育妇女中SCH的发生率约占4%~15.4%。甲状腺素在维持人类正常生殖功能中发挥重要作用:TSH、甲状腺激素及受体在人卵巢颗粒细胞和卵母细胞均有表达, 协同卵泡刺激素(follicle stimulating hormone, FSH) 调节颗粒细胞增殖, 促进黄体生成素(luteal hormone, LH) /h CG受体表达及E2、P分泌;T3可协同表皮生长因子(epidermal growth factor, EGF) 刺激细胞滋养层细胞的增殖潜能和合体滋养层细胞的分化, 促进滋养层细胞的侵入。SCH对生殖的影响:抑制FSH分泌, 抑制颗粒细胞合成E2、P及卵母细胞发育;升高的T S H通过负反馈使促甲状腺素释放激素(thyrotropin releasing hormone, TRH) 升高, 多巴胺分泌减少, 引起高泌乳素血症, 导致排卵障碍、黄体功能不足、月经稀发甚至闭经;甲状腺素协同EGF的作用下降, 影响胚胎着床及正常妊娠的维持;降钙素可通过升高细胞内Ca2+浓度调节子宫内膜细胞分化和胚泡发育, 在胚胎植入中发挥重要作用, SCH时降钙素水平降低, 影响胚胎着床。因此在FET周期, SCH主要通过影响胚胎着床能力、子宫内膜容受性导致生化妊娠。我们的数据显示生化妊娠组SCH发生率、未治疗或治疗后未正常的周期所占比例都比正常宫内妊娠组高(P<0.05) , 与文献报道一致。
2012年美国内分泌协会临床实践指南建议, 有SCH或不孕症病史、年龄>30岁、甲状腺抗体阳性等情况的妇女, 孕前最好控制TSH<2.5 m IU/L。实践也证实在孕前及时发现并治疗S C H, 维持TSH<2.5 m IU/L, 能提高胚胎种植率、临床妊娠率, 降低生化妊娠率[16]。目前国内外对合并SCH的FET患者研究较少, 更没有相应的指南或共识, 因此需要深入、详细地研究SCH在FET周期中导致生化妊娠的机制, 制定相应的诊断、治疗指南。
ICSI适应证患者本身可能存在严重的精子或卵子缺陷, 导致胚胎质量差、发育停滞, ICSI操作过程也可能损害卵母细胞、影响胚胎发育, 因此有必要探究ICSI是否与生化妊娠有关。我们的数据显示两组患者不孕因素、ICSI周期所占比例没有统计学差异, 与文献报道一致[3]。FET周期, 胚胎经过囊胚培养、冷冻、复苏过程, ICSI操作对胚胎的影响可能已经弱化。
有研究报道合并自然流产史的患者发生生化妊娠的概率比无自然流产史的患者高。我们的数据显示两组患者合并自然流产史的比例无统计学差异, 可能与FET助孕过程有关:患者FET前做了充分的检查和治疗, 已经根除了导致既往自然流产的原因;FET首选优质囊胚移植;充分的黄体支持、密切的随访也杜绝了可能导致生化妊娠的因素。子宫内膜异位症产生的炎性因子、抗子宫内膜抗体, 输卵管积液产生的炎性因子, PCOS的内分泌、代谢异常等可能影响胚胎发育、着床, 导致生化妊娠。我们的数据显示生化妊娠组和正常妊娠组是否合并上述疾病没有统计学差异, 与王雪等的研究结论一致, 可能与解冻移植囊胚前预处理充分、纠正了内分泌和代谢异常、对输卵管积液患者行输卵管结扎术、对合并子宫内膜异位症的患者给予Gn RH-a预处理有关。母体内分泌、免疫异常也可能导致生化妊娠, 我们对这部分患者先进行治疗, 并在助孕过程中维持正常状态, 因此未对其进行比较。
我们的数据显示生化妊娠组和正常妊娠组患者周期准备方式没有统计学差异, 因此, 鉴于自然周期的优势:经济、简便、副作用小, 我们对大多数排卵正常的患者采取自然周期。
综上所述, FET前关注高龄患者, 重视甲状腺功能检查及治疗有助于减少生化妊娠。导致FET周期生化妊娠的原因十分复杂, 可能为多个因素共同作用, 高龄及SCH只是其中2个因素, 今后还需更深入、细致地研究。另外, 每个生殖中心的患者特点、治疗措施、实验室培养条件均不同, 需要结合自己的实际情况寻找最可能的原因并针对性治疗。
冻融囊胚移植周期生化妊娠相关因素二:
随着IVF-ET的不断成熟, 其作为治疗不孕症的有效手段在临床中得到广泛运用, IVF-ET治疗的主要目的为抱婴回家, 我国各生殖中心的IVF-ET妊娠率仍然不是很高, 其中生化妊娠影响很大, 在临床工作中生化妊娠不但影响了IVF-ET的结局, 也增加患者的经济负担和心理压力。
生化妊娠是指HCG大于正常值, 但超声检查宫腔内、外均未见到孕囊而妊娠终止 。生化妊娠在自然受孕的妇女中发生率约为30% , 而在辅助生殖技术受孕妇女中约为12%~30% 。到目前为止, 生化妊娠的发生机制尚不清楚, 国内外研究也较少。
随着年龄的增大, 卵子质量的下降, 胚胎非整倍体发生概率逐渐增加, 在临床上已无争议。年龄已作为衡量IVF-ET结局的重要预测指标之一, 妇女年龄大, 卵巢功能减退, 胚胎非整倍体率增加, 子宫内膜容受性降低 , 是造成临床妊娠率下降和生化妊娠率增加的重要原因。本研究中, 根据年龄分组后, >35岁组生化妊娠发生率最高(5/12, 41.7%) , 三组生化妊娠率比较, 差异有统计学意义(P<0.05) 。
近年来, 不孕症的发病率逐年增加, ICSI技术也不断成熟, 为众多男性不育症患者带来了福音。在受精后第6天受精卵滋养层开始分泌微量HCG, HCG的产生直接与滋养细胞的数量和发育有关, 被认为是早期预测妊娠结局的一个最有价值的生化指标 。一研究认为ICSI可能会导致较低的HCG水平 。迟洪滨等 首次发现新鲜移植周期中, 生化妊娠组胚胎移植后14 d的HCG水平在ICSI受精组较常规IVF低(90.90 IU/L vs.120.50 IU/L) , 差异具有统计学意义(P=0.032) , 而接受常规IVF与ICSI体外受精后临床妊娠者(除外生化妊娠) 血中HCG浓度差异无统计学意义。造成ICSI组血清HCG水平下降的确切原因尚不清楚, 可能与ICSI来源的胚胎胚胎种植延迟所致 。本研究中, IVF和ICSI来源的胚胎的生化妊娠发生率无统计学差异, 说明ICSI技术并不影响胚胎的发育。
解冻后胚胎的质量和子宫内膜的容受性是影响FET成功的关键因素, 因此内膜的准备是冻融胚胎临床治疗的重要环节。本研究显示人工周期和自然周期两种方法准备内膜并不影响FET的治疗结局, 人工周期激素替代的目的在于模拟自然周期排卵的内分泌状态准备内膜, 主要用于月经不规则或者内膜较薄者, 由于药物费用相对高, 患者的接受性差。理想的胚胎种植环境是有正常排卵的自然周期的内膜, 因此对于大多数排卵正常的患者, 我们仍然采取自然周期准备子宫内膜。自然周期行冻胚移植相对人工周期外源性激素类药物少, 费用少, 患者也更容易接受。
着床失败、生化妊娠和流产发生于胚胎发育的不同时间段。生化妊娠又称为亚临床流产, 是早期流产的一种, 是IVF治疗中妊娠丢失的重要影响因素之一。早期自然流产发生机制可能主要是胚胎染色体异常(主要为非整倍体) , 导致胚胎着床障碍;母体内分泌异常导致的黄体功能不全、母体的免疫异常及生殖器畸形等也可能是发生早期自然流产的重要因素。同时外界环境, 如砷、苯、氯丁二烯、甲醛、铅、氧化乙烯等化学物质过多接触, 均可导致母体内环境发生改变, 导致流产 。
Wang等报道自然流产与妊娠丢失次数呈正相关, 第一次妊娠终止发生自然流产的危险性是11%~13%, 第二次为13%~17%, 第三次发生的概率为80%, 且既往存在1次自然流产史的患者行辅助生殖技术后自然流产率为20%, 有2次自然流产史者约为26%, 有3次自然流产史的约为34%, 流产的次数越多, 复发率越高。本研究提示既往有合并自然流产史的患者发生生化妊娠的概率比无自然流产史的患者高(P<0.05) 。推测其原因可能是, 既往有流产史的患者存在胚胎染色体异常、免疫因素的危险性均比无流产史的患者高, 而且有流产史患者可能合并宫内组织残留, 行刮宫操作, 导致子宫内膜机械性损伤, 从而导致子宫内膜容受性降低。
生化妊娠主要是胚胎着床过程已经开始但未能完成 , 其发生机制目前仍不清楚。通过本研究可以发现年龄和既往流产史是影响生化妊娠发生的重要因素, 推测主要是由于年龄增加引起的胚胎质量下降和胚胎染色体异常及母体免疫因素异常导致的结果。
复发性流产患者发生生化妊娠的高危因素
生化妊娠超声检查无孕囊妊娠 。正常受孕妇女因初检不到位, 常将妊娠理解为“月经延迟”而未重视。国内对≥3次妊娠、孕28周前胎儿丢失称为复发性流产(RSA) 。RSA患者因过度紧张通常会选择在月经未过期或性生活10天就行绒毛膜促性腺激素(β-hCG) 检查, 增加了临床生化妊娠发生几率。反复流产与生化妊娠均可造成女性生理、心理影响 。目前生化妊娠的病因成为国内外关注焦点。本文对门诊未孕RSA患者生化妊娠的病因进行分析, 探讨可能危险因素。
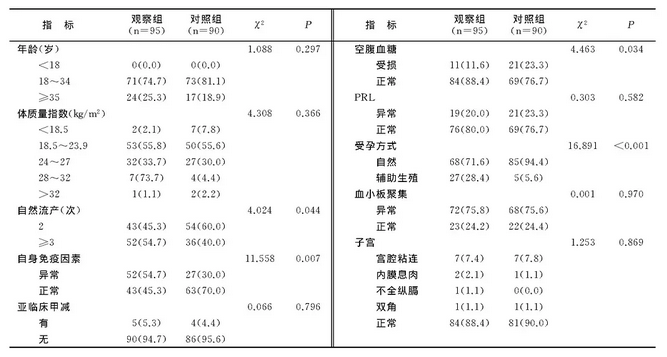
两组RSA患者临床指标比较[例(%) ]
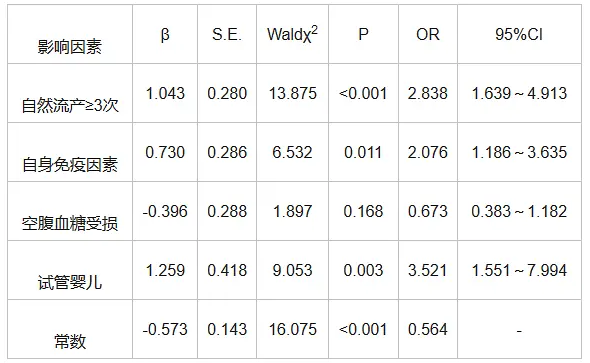
RSA患者生化妊娠危险因素的多因素分析
生化妊娠临床中称为不明部位妊娠、隐匿性流产。诊断标准:早期妊娠不足6周, 血清HCH<2400IU/L, 48h血清HCG升高<50%, 孕酮<72.6mmol/L与子宫中膜厚度<10mm。对生化妊娠病因研究不多。本文分析发现, RSA患者自身免疫因素异常、辅助生殖、流产≥3次是出现生化妊娠危险因素。表明人工受孕的妇女仍伴生化妊娠的危险。通常辅助生殖阶段生化妊娠发生率占12%以上, 可能与子宫内膜容受性相关。卵胞浆中单精子注射(ICSI) 对胚胎着床与生化妊娠发生的影响在业内争论不一。 因此, 临床针对习惯性流产或长期不孕而渴望受孕的妇女, 找到疾病的源头采取治疗后, 再考虑辅助生殖技术受孕。
相关文献指出, 既往有流产史妇女生化妊娠发生率高于无流产史者。本文流产次数≥3次是生化妊娠发病危险因素。由于既往流产妇女多伴胚胎染色体异常风险, 同时流产次数过多, 刮宫术使子宫内膜侵损严重、容受性衰退。有学者指出, 多次流产、母体免疫因素异常均是造成生化妊娠的危险因素。患者免疫抗体阳性, 使胚胎着床几率降低, 增加了生化妊娠风险。Alijotas-Reig等研究提示, 自身免疫系统失常与生殖失败相关, 病因不明的RSA可能伴自身免疫失调, 临床称 “亚临床自身免疫疾病”或“生殖关联自身免疫异常综合征”。近年研究发现, 抗核抗体阳性是RSA危险因素, 主要是妊娠初期影响了子宫内膜生长, 使胚胎无法成功着床。
抗磷脂抗体综合征临床表现为复发性流产、血小板减少及动静脉血栓形成, APS 是诱发重复流产的孤立危险因素。ACA经阻滞胎盘合体滋养细胞集聚, 使滋养细胞分裂与增值功能受影响, 降低了滋养细胞的侵蚀能力, 减弱子宫螺旋动脉血管重铸功能, 增加流产几率及胚胎着床难度。现阶段与自身免疫因素造成生化妊娠的病理研究有待深入探讨。国内研究提示, 子宫内膜厚度、容受性、卵子质量、精子质量等均与生化妊娠呈现相关性。有学者指出, 年龄与生化妊娠发生具有相关性。本研究结果中生化妊娠并未发现受年龄因素的影响, 还需进一步深入探讨。
综上所述, 针对生育需求的RSA妇女, 应有效控制生化妊娠发生。自身免疫因素异常、辅助生殖、流产≥3次均是造成RSA患者出现生化妊娠危险因素, 在临床应予以重视。
宫腔内人工授精治疗后生化妊娠或临床妊娠的相关因素
近年对已婚育龄妇女在月经周期后半期采用β -人绒毛膜促性腺激素( human chorionic gonadotropin,HCG) 放射免疫法进行检测,发现约30% ~ 40% 的受精卵在着床后至月经前发生流产,临床仅表现为月经稍推迟、月经量稍增多,这种情况考虑为生化妊娠。既往大部分妇女由于早孕检测不及时,生化妊娠常被误以为是“月经延迟”而被漏诊。胚胎通过了生化妊娠阶段,才过渡到临床妊娠阶段。超声下见妊娠囊者为临床妊娠( 包括异位妊娠) 。生化妊娠的机制仍未明确,可能与配子及胚胎在受精及着床过程中遇到不良因素有关,例如胚胎与子宫内膜的发育不同步或胚胎发育过程中血管生成缺陷等引起。 本研究通过分析宫腔内人工授精( intrauterine insemination,IUI) 治疗后生化与临床妊娠两种不同结局,比较男方精液优化处理后的参数、患者一般情况、促排卵方案等相关资料,尝试寻找出影响生化妊娠发生的因素,以改善IUI妊娠结局以及提高抱婴率。
胚胎由精子、卵子受精后卵裂构成,因此精液的异常可能影响精子的受精能力以及受精卵分裂,使胚胎发育异常,导致不良妊娠结局。但目前研究中,IUI中精液质量对妊娠结局的影响仍存在着争议。Lewis认为,传统上有赖于显微、生化技术评估男性精液的质量,其精子浓度、活力、畸形率等参数不能准确预测IUI妊娠结局。本研究亦证实,两组患者精液优化后的各项常规精液参数比较,差异无统计学意义( P > 0. 05) ,故考虑优化后的精液对IUI术后妊娠结局的影响较小。
子宫内膜的容受性是胚胎成功着床的关键环节之一。胚胎与子宫内膜的同步性是影响胚胎成功种植的一个主要因素。早期大部分学者认为子宫内膜厚度与妊娠结局相关,随后较多研究认为内膜厚度与妊娠结局无关,而子宫内膜血流检查可作为预测子宫内膜容受性较好的无创方法。本研究发现子宫内膜形态与IUI周期中生化、临床妊娠的发生有一定联系。B超下子宫内膜形态于排卵期分为三型: A型,三线型; B型,回声较均匀,宫腔中线回声不明显; C型,团块状回声。IUI当天A型子宫内膜的患者,临床妊娠的概率高; 而IUI当日B型子宫内膜患者,生化妊娠的概率较高。本研究也证实IUI日A型子宫内膜在临床妊娠组的构成比明显高于生化妊娠组。Clancy研究认为,更多关注子宫内膜有助于解开人类进化生物学的几个问题,如低种植率、高早孕流产率等。
本研究中,两组患者的年龄、不孕年限、体质量指数、不孕诊断、病因及IUI方案比较,差异均无统计学意义( P > 0. 05) ,考虑与样本量较少有关,仍需大样本的研究结果支持。总之,胚胎着床是多个因素协同作用的结果,任何一个环节异常都可能导致植入障碍。接受IUI助孕的妇女常有多年不孕,心理承受能力脆弱。生化妊娠影响了IUI的妊娠结局,同时增加了不孕症夫妇的精神压力及经济负担,临床医师应给予足够的重视。
淋巴细胞免疫治疗反复生化妊娠流产
据相关研究显示, 生化妊娠流产是指在患者妊娠期5 周内引起的早期流产。近年来, 生化妊娠流产患者呈上升趋势, 患者均伴有4 次以上的流产史, 称为反复生化妊娠流产, 导致反复生化妊娠流产的主要因素为;(1) 患者受精卵本身患有缺陷,(2) 子宫因素;患者伴有子宫粘膜下肌瘤、宫腔粘连、子宫内膜结核等疾病,(3) 免疫因素影响等。本院对生化妊娠流产患者采用常规治疗和淋巴细胞免疫治疗, 淋巴细胞免疫治疗取得较为可观的效果。
淋巴细胞免疫治疗是指;抽取患者丈夫体内的静脉血, 分离出淋巴细胞, 然后注射入患者体内, 从而使患者体内封闭抗体产生。患者体内的胚胎基因其中一半来自患者本身, 另一半来自患者丈夫, 由于胚胎会引起患者体内免疫系统的排斥反应, 当患者体内的封闭抗体减少时, 易导致患者体内的免疫系统攻击胚胎, 从而导致生化流产情况发生, 大多数足月妊娠分娩患者, 主要是因为在妊娠期胚胎刺激患者体内产生封闭抗体, 从而保护体内胚胎免受伤害。而淋巴细胞免疫治疗能够使患者体内产生封闭抗体, 从而维持妊娠, 避免反复生化流产情况发生。
经研究表明, 观察组、对照组两组生化妊娠流产患者采用不同的方式治疗后, 观察组生化妊娠流产患者在妊娠结局的比较中显著优于对照组, 由此可见观察组生化妊娠流产患者采用的淋巴细胞免疫治疗效果更为显著。
综上所述, 淋巴细胞免疫治疗反复生化妊娠流产具有良好的治疗效果, 值得在临床中进一步推广及运用。
米非司酮配伍米索前列醇终止生化妊娠的前瞻性临床分析
米非司酮配伍米索前列醇终止生化妊娠的安全性 药物流产目前已被公认为是一种安全、有效的非手术终止妊娠的抗早孕方法, 但用于终止生化妊娠的研究报道并不多, 潜在的异位妊娠可能是限制其应用的重要原因。随着超声诊断及检验技术的发展, 临床上有最大程度降低异位妊娠误诊及避免异位妊娠破裂的可能, 相对而言异位妊娠的发病率仅为1%~3%。术前阴道超声严格筛查可使早期临床妊娠的识别时间明显提前, 且对附件区包块有较高的分辨率。而近年的研究认为子宫内膜三线状改变、内膜厚度≤9 mm及对称、均匀性增厚是鉴别早期异位妊娠有意义的指标。术前血β-hCG水平及孕囊直径与孕龄相关。有研究认为孕5周血β-hCG>1 000 mIU/ml时阴道超声可检测出孕囊, 当孕囊平均直径>10 mm且血β-hCG达到3 000 mIU/ml以上时, 阴道超声可检测出卵黄囊。因此, 通过血β-hCG检查可筛选部分疑似异位妊娠病例。术后密切随访如孕囊的排出、血β-hCG下降程度等可进一步排除异位妊娠病例。该研究中生化妊娠组服用米索前列醇后第3天复查血β-hCG均有较大幅度的下降, 血β-hCG平均下降率为92.4%。此外, 应用米非司酮是早期异位妊娠治疗的首选方法之一。即使为早期异位妊娠病例, 米非司酮的使用可起到杀胚作用, 至少不会促使异位妊娠包块的破裂。Goksedef BP等的研究提示血β-hCG超过5 000 IU/L是输卵管妊娠破裂的高危因素。在该研究中生化妊娠组术前血β-hCG平均值为1 209.2 IU/L, 最高值为2 552.01 U/L, 远低于上述输卵管妊娠破裂的风险值。因此, 术前的严格筛查及术后的严密随访, 做到早期诊断、早期治疗, 异位妊娠破裂导致大出血甚至危及生命的可能性会大大降低。而最近的研究也提示宫腔外生化妊娠行保守治疗疗效确切, 效果明显高于临床异位妊娠, 认为对疑为宫腔外生化妊娠的非意愿性妊娠者不必等待至发展为临床异位妊娠再做处理。
米非司酮配伍米索前列醇终止生化妊娠的流产效果 2003年世界卫生组织(WHO) 的调查结果表明药物流产有效率为92.3%~94.7%, 该研究结果显示生化妊娠组完全流产率97.4%。药物流产用于终止早期妊娠方便安全有效, 但其术后阴道出血时间长、出血量多等不良反应的存在使其可接受性受到了一定影响。目前研究认为药物流产术后阴道出血时间长、出血量多等不良反应主要是由于绒毛及蜕膜组织残留引起。对于药物终止早期临床妊娠, 大多数研究认为妊娠时限越短、孕囊直径越小, 药物流产后阴道出血量就越少、出血持续时间也越短。该研究发现早期临床妊娠组服用米索前列醇后孕囊未排出前出血量较多, 多于平素月经量, 孕囊排出后则出血量明显减少;生化妊娠组出血平缓, 如平时月经量, 两组均无因出血多而需紧急清宫者。该研究结果提示生化妊娠组阴道流血平均持续时间为6.1天, 而对照组平均阴道流血持续时间为8.8天, 可见药物流产终止生化妊娠较早期临床妊娠明显缩短了阴道流血时间。
米非司酮配伍米索前列醇终止生化妊娠的注意事项和术后随访的重要性 术前应严格掌握适应症和禁忌症, 术中应严密观察孕囊排出、阴道流血情况及药物不良反应。告知患者如出现严重腹痛或阴道流血多于月经量等情况需及时复诊, 未见孕囊排出者应及时复查血β-hCG, 必要时复查B超以排除异位妊娠可能。
总之, 该研究提示生化妊娠阶段药物流产是可行的及安全的, 完全流产率高, 阴道流血时间短, 流血量少, 月经恢复快。但该研究纳入的样本量较少, 仍有待于今后多中心、大样本、前瞻性随机研究。对尚处于生化妊娠阶段非意愿妊娠的妇女, 应详细解释病情, 帮助其做出合理选择, 行药物流产前取得知情同意是可考虑的处理方式。
胚胎移植术后9和11d血清β-HCG值对妊娠结局的预测价值
移植术后9和11 d血清β-h CG值对治疗结果的早期诊断作用
不孕症患者普遍存在焦虑心理,胚胎移植术后希望尽早知晓治疗结果。目前国内生殖中心判断患者是否妊娠普遍选用的时间点是胚胎移植术后的14~16 d。那么,这个时间点是否可以前移及最早可以前移到什么时候呢?
Caroline等通过对154例患者177个IVF周期的检测,发现ET后12 d(即取卵后15 d)血β-h CG值可准确诊断妊娠和预测妊娠结局。Legro等对77例胚胎移植后9 d的供卵IVF周期使用放射免疫法测定β-h CG值,发现虽然受精后6 d滋养层形成时开始分泌微量HCG,但胚胎移植后9 d可能由于胚胎延迟着床,或滋养细胞的增殖还没有达到一定的数量时不能分泌足够量的HCG,因此胚胎移植后9 d单纯进行β-HCG的测定不能准确地预测妊娠结局。而黄仲英等则采用微粒子酶免疫分析法(MEIA)对80例IVF-ET术后的患者于胚胎移植后2 d隔日测血β-h CG,发现未孕组在移植后8 d降至0~16(m U/m L),多数在10 d降至0,宫内继续妊娠组在移植后8或10 d开始有不同程度的回升,且从8 d开始,妊娠组血β-h CG水平明显高于未孕组,差异有显著性,因此,作者认为IVF-ET妊娠的早期诊断,至少可提前到ET后12或10 d,甚至可早至ET后8 d。
鉴于以上报道,目前胚胎移植术后第9~11天血清β-h CG值对IVF治疗结局的判断和妊娠结局的预测尚无明确结论。因此,本文采用化学发光法对227名行胚胎移植术的患者在移植后9 d和11 d检测其血β-h CG值对她们的治疗结局进行了早期诊断。本文结果表明,未孕组9 d血β-h CG值为7.49±5.54 U/L(0~22 U/L),11 d血β-h CG值为2.71±2.36 U/L(0~10 U/L),明显低于生化妊娠和临床妊娠组。大部分未孕组患者9 d血β-h CG值已经降至诊断界值10 U/L以下,但由于部分患者黄体支持时应用了外源性HCG的干扰,导致这部分未孕患者9 d血β-h CG值高于诊断界值10 U/L,但所有未孕组患者11 d血β-h CG值较9 d均有进一步下降趋势,11 d与9 dβ-h CG比值为0.27,明显低于生化妊娠组(0.86)和临床妊娠组(2.63)。与Legro等的结论一致,本文中单次检测移植9 d血β-h CG值并不能准确判是否妊娠,但9 d、11 d血β-h CG值结合11 d与9dβ-h CG比值则可准确诊断是否妊娠的治疗结局。对于这部分明确种植失败的患者,则可及时终止不必要的黄体酮注射,减少她们身体的痛苦和心理焦虑等待的时间。
移植后9 d和11 d血β-h CG值对妊娠结局的预测价值
胚胎移植术后早期血β-h CG值不仅具有诊断患者是否妊娠的作用,而且具有预测患者妊娠结局(如:生化妊娠、流产、异位妊娠、多胎妊娠等)的功能。
本研究显示临床妊娠组IVF-ET后9 d和11 d血清β-h CG值高于生化妊娠组,且以移植9 dβ-HCG=49.05 U/L为界值时,预测临床妊娠的敏感度为73.2%,特异度为87.5%,阳性预测率为97.6%(HCG≥49.05 U/L时提示为临床妊娠),阴性预测率为31.8%(HCG<49.05 U/L时提示为生化妊娠);而以移植11dβ-HCG=51.2 U/L为界值时,预测临床妊娠的敏感度可达到98.2%,特异度为87.5%,阳性预测率98.2%(HCG≥51.2 U/L时提示为临床妊娠),阴性预测率为87.5%(HCG<51.2 U/L时提示为生化妊娠);11 d的ROC曲线下面积为0.948,提示11 dβ-HCG对于生化妊娠或临床妊娠的结局具有高度预测价值。
IVF-ET后多胎妊娠的发生率远高于自然妊娠。本研究中双胎妊娠率为32.14%(36/112)。双胎妊娠组的9 d和11 d血清β-HCG水平显著高于单胎妊娠组(127.93±40.61 vs 62.95±31.55 IU/L,379.71±157.42 vs166.43±89.46 IU/L),而两组间11 d/9 dβ-HCG比值并无显著差异,这说明HCG绝对定量与胚胎着床数目有关,而HCG倍增速度则可能与滋养细胞的发育有关。本研究中,单胎及双胎妊娠以移植9 dβ-HCG=105.15 U/L为界值时,预测单胎妊娠的敏感度为81.1%,特异度为90.5%,阳性预测率为82.9%,阴性预测率为89.06%;11 d以β-HCG=241.75 U/L为界值时,预测单胎妊娠的敏感度为83.8%,特异度为87.3%,阳性预测率为78.9%,阴性预测率为90.16%。9 d及11 d的β-HCG值对单双胎具有相似的预测价值(9 d及11 d的ROC曲线下面积分别为0.897与0.899)。目前国内外文献关于单次血清β-HCG值预测多胎妊娠的最早时间为胚胎移植后12 d,本研究显示,预测多胎妊娠的时间点可提前至移植后9 d。
本研究中,早期流产率为4.46%(5/112),宫外孕发生率为6.25%(7/112),宫内并宫外孕率为0.89%(1/112)。胚胎移植后9 d、11 d流产组和宫外孕组血清β-HCG值均显著低于双胎和单胎妊娠组(P<0.01),但流产组和宫外孕组血清β-HCG值无统计学差异。在本研究中,胚胎移植后9 d、11 d血清β-HCG值预测流产和宫外孕的ROC曲线下面积分别为0.206和0.194,均小于0.5,提示9 d、11 d的血清β-HCG值均不能预测早期流产、宫外孕的发生。这可能与流产和宫外孕患者滋养细胞分泌的异常模式有关,也可能与本研究样本量偏少有关,以后尚需扩大样本量进一步验证。
胚胎质量和冻融周期
体外受精-胚胎移植(in-vitro fertilization and embryo transfer, IVF-ET) 治疗的最终目的是出生健康婴儿。虽然全世界范围内IVF-ET的妊娠率已超过40%, 但是抱婴回家率仍停留在30%左右。生化妊娠和早期胚胎停止发育不但影响了体外受精(IVF) 的结局, 也给患者带来了巨大的身心痛苦。生化妊娠、胚胎停止发育的相关影响因素较多, 可能与胚胎、内膜、免疫调节、促排卵方案等因素有关, 但目前其发生机制仍不清楚。很多患者和临床医生将生化妊娠和胚胎停止发育的主要因素归结为胚胎质量。那么, 在IVF-ET冻融周期中, 胚胎的质量是否会影响临床结局导致生化妊娠或早期胚胎停止发育?如果是有影响, 实际工作中能否采取措施避免或改善生化妊娠或早期胎停的临床结局?本研究回顾性分析了IVF-ET助孕后生化妊娠患者、早期胚胎停止发育患者和继续妊娠患者的临床资料, 探讨胚胎质量对生化妊娠和胚胎停止发育周期的影响, 旨在最终提高抱婴率。
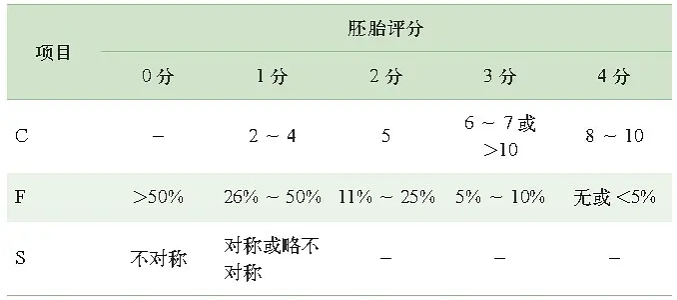
D3胚胎评分标准Tab 1 The scoring standard for embryo on the third day after embryo transfer
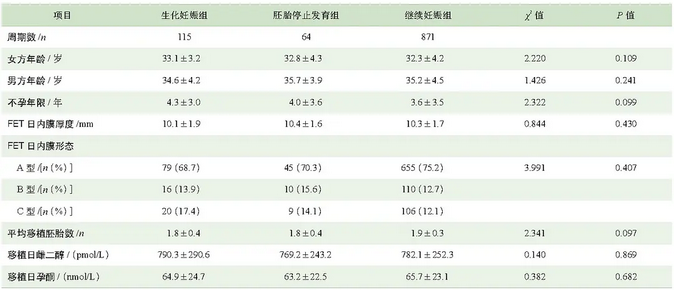
一般临床资料比较Tab 2 General clinical characteristics of the patients
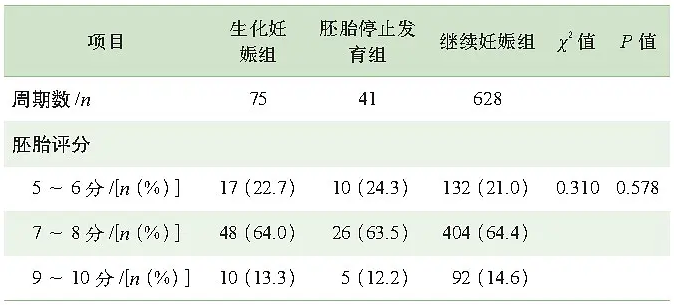
D3胚胎评分与生化妊娠和胚胎停止发育的关系Tab 3 Relationship between embryo score on D3 and biochemical pregnancy or arrest embryo development
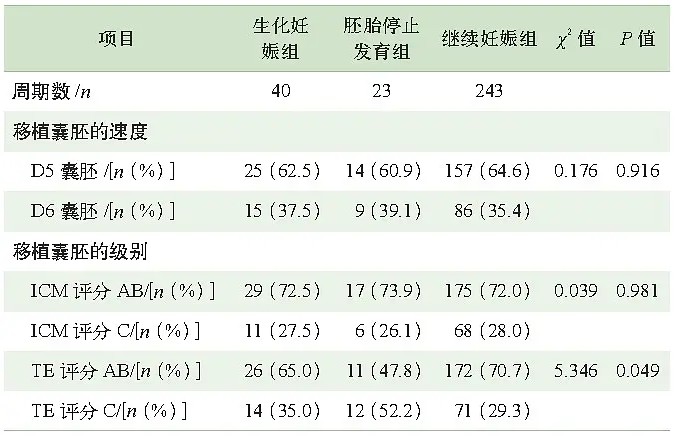
D5/6囊胚质量与生化妊娠和胚胎停止发育的关系Tab 4 Relationship between the quality of blastocyst and the biochemical pregnancy or the arrest of embryo developmen
生化妊娠是指β-HCG大于正常值, 但B超检查宫腔内、外均未见到孕囊而妊娠终止。胚胎停止发育是指妊娠早期胚胎因某种原因所致发育停止, B超检查表现为妊娠囊内胎芽或胎儿形态不整, 无胎心搏动, 或表现为妊娠囊枯萎。在美国, 调查显示人群总自然流产率为10.9%, 而辅助生育技术总流产率为14.7%。辅助生育治疗中, 胚胎经过人为筛选, 择优移植, 理论上流产率应当低于普通人群, 然而事实上, 其流产率依然较高。如何降低辅助生育妊娠的流产率, 提高活产率, 一直备受关注。另外, 自然妊娠早孕胚胎停止发育发生率呈逐渐增加趋势, 可能与感染、环境污染、辐射和长期暴露于有毒化学物质环境等不良环境因素增加有关。对于辅助生育技术助孕后妊娠患者, 女性高龄、夫妇或胚胎染色体异常是早期自然流产的常见原因。但很多患者和临床医生都会把生化和胎停的主要因素归结为胚胎质量。那么, IVF-ET冻融周期中, 胚胎的质量是否会影响临床结局导致生化妊娠或早期胚胎停止发育?本研究在限定女方年龄、不孕原因、不孕年限、授精方式、内膜准备方案等后比较胚胎质量及评分在生化妊娠和早期胚胎停止发育中的意义。
胚胎质量不是生化妊娠的主要原因
评价胚胎质量的方法很多, 目前临床上主要是通过胚胎的形态学表现来评价胚胎质量, 并挑选移植/冷冻胚胎。本研究通过量化D3移植胚胎的质量, 发现所移植胚胎的质量在生化妊娠组和继续妊娠组之间没有统计学差异。这个结论与平时临床医生或患者持有的观点即生化妊娠是胚胎发育潜能欠佳不一致。当然, 通过胚胎发育速度、碎片程度、细胞均一度等形态学指标对D3移植胚胎评分存在一定的局限性。如何评价胚胎发育潜能选择优质胚胎移植是改善胚胎着床率、降低多胎妊娠率的关键环节。囊胚在体外培养过程中经历了胚胎的再次选择, 理论上囊胚移植能够达到更高的妊娠率和活产率。因此我们又比较了生化妊娠组和继续妊娠组在移植D5囊胚比例和移植D6囊胚比例上的差异, 以观察胚胎发育速度的差异是否会影响到胚胎质量及评分进而导致生化妊娠。结果发现两者在胚胎发育速度上的差异没有统计学意义。那么所移植的囊胚的级别不同是否会导致生化妊娠?结果我们发现ICM评级为A/B和C的移植囊胚所占的比例, 或TE评级为A/B和C的移植囊胚所占的比例, 在2组之间比较, 均没有统计学差异。我们的研究提示囊胚移植对于生化妊娠没有明显的改善。形态学上的评分主观性太强而并不能完全代表胚胎真实的发育潜能。2003年Troneoso等通过胚胎植入前遗传学筛查(PGS) 筛选整倍体胚胎移植后, 对62例行PGS后妊娠病例与同期非PGS妊娠周期进行比较, 3组人群生化妊娠比例比较, 无显著性差异, 表明PGS并未降低生化妊娠的发生。由此可见除了胚胎质量及评分, 胚胎染色体异常也可能不是生化妊娠的主要原因。
囊胚TE评级状况可能会影响早期胚胎停止发育
我们比较了早期胚胎停止发育组和继续妊娠组所移植胚胎, 发现D3胚胎评分, 及D5/6囊胚比例在2组之间的差异均无统计学意思, 也就是说早期胚胎停止发育与D3的胚胎质量及评分、囊胚的发育速度无关。但早期流产组TE评级为C的囊胚所占的比例要高于继续妊娠组, 2组之间比较差异也有统计学意义, 这就意味着继续妊娠与否与囊胚的TE相关, 与文献报道一致。Ahlström等认为TE的形态学与胚胎的种植率、妊娠率呈正相关。Honnma等发现TE的形态学与继续妊娠率呈明显的正相关。我们分析继续妊娠与否与囊胚的TE相关的原因可能有:(1) TE细胞能够产生HCG, 而且高级别的TE细胞分泌HCG时间更早, 分泌量更多, HCG能够刺激黄体合成和分泌更多孕激素, 能够调节子宫内膜对植入胚胎的容受性, 在母胎对话和成功维持妊娠中发挥着重要作用(2) TE细胞非整倍体的发生率与其评级呈明显的相关性, Alfarawati等发现与评级为A的TE细胞相比, 评级为C的TE细胞非整倍体发生率明显升高。
综上所述, 胚胎质量可能不是生化妊娠的主要原因, 而TE的评级可能是胚胎早期停止发育的原因之一, 优质囊胚不仅可以提高妊娠率还可以降低流产率。因此, 我们建议尽可能行优质囊胚移植, 对于TE评级为C的胚胎如果有条件可以在移植前检查胚胎的染色体, 避免植入核型异常的胚胎, 这样有助于降低流产率;在没有条件的情况下要充分告知患者, 知情同意下再选择TE为C的囊胚进行移植。
生化妊娠病因及治疗的研究进展
受精卵在受精后第6~7 d开始着床,大约在第9 d滋养层细胞分化为细胞滋养细胞和合体滋养细胞,开始分泌人绒毛膜促性腺激素(human chorionic gonadotropin,HCG),第11~12 d完成。着床经历定位、附着及植入3个阶段。在植入后任何环节出现问题,都可能导致着床最终失败。临床上表现为血清HCG大于正常值,但超声检查宫腔内外均未见到孕囊,然后妊娠状态自然终止,通常称为生化妊娠(biochemical pregnancy)又称为不明部位妊娠、隐匿性流产 。随着辅助生殖技术的广泛应用,生化妊娠以其高达50%~60%的发生率日益受到关注 。关于生化妊娠的病因尚不清楚,目前发现生化妊娠与母体因素和胚胎因素均有关,子宫内膜的厚度和容受性、卵子的质量以及胚胎质量与生化妊娠的发生密切相关 。也有研究表明,母体激素水平、免疫水平可能参与了生化妊娠的发病 。而胚胎染色体等其它因素对生化妊娠的发病影响并不显著。生化妊娠的处理关键是确定妊娠部位,适时终止妊娠,目前尚无特定的处理方法 。
生化妊娠的病因研究进展
1.1 子宫内膜的厚度与容受性
子宫内膜是胚胎种植的“土壤”,是正常受孕的关键部位,内膜厚度、形态及其容受性都影响着妊娠结局。Dickey等 回顾性分析了81例患者排卵前子宫内膜厚度及类型与生化妊娠的关系,结果发现在HCG注射日或黄体生成素(luteinizing hormone,LH)峰日子宫内膜厚度<9 mm的患者生化妊娠发生概率较高,而HCG注射日宫内膜厚度>9 mm的患者没有出现生化妊娠,此外还发现当子宫内膜形态为三线型内膜时,生化妊娠的发生率低,可能是缘于解剖、免疫或其他原因所致的内膜容受性的降低。
近年来,Abdallah等 研究了1 774例辅助生殖患者的妊娠状况,发现在接受了促排卵治疗后,患有子宫内膜息肉(<2 cm)的患者生化妊娠的风险较子宫内膜正常者高,而这一差异可能是由于胚胎植入后的早期发育阶段受到了局部炎症反应的影响所致。子宫内膜息肉还会影响内膜的容受性 ,其机制可能是:(1)内膜息肉作为占位性病变,影响精子运动及胚胎的植入 ;(2)息肉组织可能产生胎盘蛋白,抑制NK细胞活性,使内膜容受性减弱而影响胚胎种植 ;(3)息肉会降低内膜容受性分子HOXA10和HOXA11的mRNA水平 。
邹琳等 将经宫腔内人工授精(intrauterine insemination,IUI)患者的子宫内膜形态于排卵期B超下分为3型:A型,三线型;B型,回声较均匀,宫腔中线回声不明显;C型,团块状回声,研究发现IUI日子宫内膜呈B型的患者生化妊娠率较其他型高,提示生化妊娠可能与IUI日子宫内膜的形态和容受性有关。Lin等 发现在血清瘦素水平增高的多囊卵巢综合征(poly cystic ovanian syndrome,PCOS)患者生化妊娠率明显升高,这与高瘦素水平激活STAT3信号通路,下调g-Ena C表达,使子宫内膜容受性降低有关。
1.2 母体激素水平
母体内各种激素对排卵、受精、着床各个过程都有一定影响,但激素水平和生化妊娠的相关机制目前尚不十分清楚。
有关雌二醇(estradiol,E2)水平与生化妊娠的关系目前存在争议。Liu等 在研究早期流产的病因中报道,接受辅助生殖(in vitro fertilization,IVF)的患者有22%发生生化妊娠,而在诱导排卵过程中这些患者的E2水平很高,提出生化妊娠可能是由于高E2阻止胚胎植入造成的。而Melnick等 在IVF周期的第28 d测定患者体内E2、HCG以及孕酮水平发现,E2≤50 pg/m L或者HCG<50 m IU/m L的患者有较高的生化妊娠率,IVF早期E2低水平往往提示妊娠结局较差,建议在妊娠早期监测E2或E2联合HCG预测妊娠结局,指导临床治疗。
在新近的研究中发现 ,接受IVF治疗的患者在口服补充E2和黄体酮进行子宫内膜准备时,恒定剂量补充E2的患者较增加剂量补充的患者,生化妊娠的发生率显著升高,提示E2与生化妊娠的发生可能有关。
在月经周期的中期,LH浓度达到峰值并诱发排卵前卵泡的第一次减数分裂,这一阶段对于确保卵泡成熟、成功受精以及胚胎的适度发育都至关重要。Esposito等 提出,在一个IVF周期中,卵泡晚期内源性黄体生成素水平低(<3 m IU/m L)会显著减少受精率并且增加生化妊娠率。
E2和LH与妊娠的结局关系密切,其浓度也影响生化妊娠的发生,就目前研究结果分析,E2过高或者过低均会影响生化妊娠的发生,因此确定临界值尤为重要,此外LH也与生化妊娠有关,但母体激素作用机制尚不清楚,有待进一步的研究。
1.3 卵子质量
卵子质量直接影响胚胎的质量,从而与生化妊娠发生相关。林蕾等 回顾性分析了行体外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET)治疗过程中发生生化妊娠的94例患者(生化妊娠组)和获得单胚胎种植单胎分娩的177例患者(对照组)的临床资料,对两组的卵子和胚胎质量进行比较,发现生化妊娠组出现胞浆颗粒化、极体碎裂、卵周隙增大及滑面内质网等异常形态的卵子比例明显高于对照组,而正常形态卵子比例则低于对照组,但两组获得的优质胚胎数和移植胚胎质量评分比较差异无统计学意义,提示IVF-ET中卵子质量下降是生化妊娠发生的重要原因,改善卵子质量可能是降低IVF-ET生化妊娠发生率、提高IVF临床妊娠率的有效手段。
1.4 胚胎质量
胚胎的质量往往通过其种植能力与种植后的发育能力影响妊娠结局 。Marek等 对辅助生殖中胚胎质量与生化妊娠的发生进行了回顾性研究,比较冻胚与新鲜胚胎生化妊娠的发生率。发现使用冻胚的患者生化妊娠的发生率较高,而且在不同年龄组发生率保持一致,因此排除了年龄因素对生化妊娠的影响。研究发现患者使用冻胚进行种植导致生化妊娠发生率高的原因可能是在冷冻前胚胎已经存在问题,或者可能是冷冻对胚胎产生了一定的影响。Zeadna等 在研究中发现,使用囊胚的患者生化妊娠发生率要低于使用卵裂期胚胎移植的患者,而且选择质量好的胚胎进行移植往往生化妊娠发生率较低。Liu等 发现PCOS患者的生化妊娠发生率远较正常人高,可能与PCOS患者产生质量较差的卵母细胞进而影响胚胎质量导致植入能力减弱有关。同样Troncoso等 和Liu等 也报道过生化妊娠的发生与胚胎质量有关。
1.5 胚胎染色体
胚胎染色体对胚胎质量存在一定的影响,对生化妊娠有无影响呢?早在1993年,Dickey等 就提出,染色体核型异常的胚胎不是引起生化妊娠的原因。在最近的研究中,Liu等 在研究中发现Y染色体长臂无精子症因子(AZF)微缺失的患者与Y染色体正常的患者在接受辅助治疗时形成的胚胎质量无明显差异,妊娠结局、生化妊娠率等也无显著差异。Luna等 在胚胎植入的研究中,一组采用经全面染色体筛查后的整倍体胚胎,另一组则使用Day3或Day5胚胎,发现两组的生化妊娠率相似,因此排除了生化妊娠与染色体核型的关系,认为生化妊娠与胚胎代谢的关系更为密切。Ghazal 在研究中使用了比较基因组杂交技术(a CGH)选择胚胎进行种植,与未使用该技术对比,生化妊娠的发生并没有得到明显改善。迄今为止的研究结果表明,生化妊娠与胚胎染色体异常的关系不大。
1.6 其他
此外,有研究表明生化妊娠与患者年龄及既往生化妊娠或流产史有关 ,免疫因素可能也是影响生化妊娠的发生因素 。还有学者提出生化妊娠可能与男性年龄和精液质量有关 ,Hessel等 认为精子活动性可以影响胚胎质量从而影响妊娠结局,导致生化妊娠。最近,Ramer等 提出脑源性神经营养因子(brain-derived neurotrophic factor,BDNF)生成减少会增加胚胎种植失败以及种植后发育不良的易感性,BDNF在子痫患者体内的浓度易发生变化,这种变化可能与其发生生化妊娠有关,生化妊娠的明确病因还有待进一步的研究。
生化妊娠的血清学及超声检测意义
1 生化妊娠的超声特点
因受环境、内分泌及大龄等因素影响,目前临床上在自然受孕及不孕不育的病例中生化妊娠发病率仍占一定比例。一般发生在孕5~6周;是胚胎着床失败导致的早期妊娠丢失,属于PUL范畴。正常妊娠时理想的阴道超声最早在妊娠5周时可见孕囊,一般认为孕5周且血清β-h CG值>1000 IU/L时阴道超声才可探测到孕囊,当孕囊平均直径>10 mm且血β-h CG值3 000 IU/L时阴道超声可检测出卵黄囊 ;但实际上妊娠6周时仍有超过10%的妊娠囊未能确切检出,这不仅可能是胚胎缺陷等因素引起,也因孕卵分裂发育的囊胚期到有确切的声像图需一定时间间隔,即:正常宫内妊娠也会有超声的生理“妊娠盲区”,因此也给生化妊娠的早诊更带来了困惑。临床上当胚胎发育到7周以上时才最容易看得见 。因早孕期滋养层细胞生长活力和数量、孕卵着床部位以及内分泌和血供的不同;其子宫内膜厚度存在一定差异,尤其子宫内膜本身的形态、代谢、厚度及生殖内分泌功能等容受性变化也是影响胚胎能否成功着床的重要因素之一,当排卵前LH峰日或h CG日的子宫内膜厚度≤9 mm时,生化妊娠的发生率较高,若当日子宫内膜厚度>9 mm时则很少有生化妊娠的发生;当内膜呈三线型时生化妊娠发生率也较低 。有研究认为生化妊娠的子宫内膜血管指数及血管血流指数均较持续宫内妊娠者低。本研究显示,生化妊娠的发生与患者年龄、既往流产史等因素无关,其子宫内膜厚度与宫内妊娠组差异无统计学意义,与张烁等 研究结果有异,但与异位妊娠组的子宫内膜厚度相比有差异,即异位妊娠者子宫内膜最薄;与宫内早孕者及生化妊娠者相比差异有统计学意义。陈智毅等 采用ROC曲线下面积(AUC)方法客观评价两种以上诊断系统指标,寻找最大约登指数(YI)即最佳阈值点,将子宫内膜厚度取值10.5 mm确定为早期可疑异位妊娠预测的最佳指标之一。本研究认为,采用内膜厚度10 mm作为筛查包括异位妊娠在内的生化妊娠的临界值其灵敏度为76%,特异度为62.1%。然而观察发现异位妊娠与正常宫内妊娠、生化妊娠间子宫内膜厚度常存在着一定的交叉重叠,不能作为单一的预测指标。
2 血清P对生化妊娠的预测作用
孕早期若孕酮合成或作用的任何环节被干扰或P偏低都可引起阴道流血导致生化流产或先兆流产等,因此血清P波动是PUL的显著特点。正常妊娠5~10周P水平是稳定的,与孕龄无关,因此血清P水平高低可作为早孕期胚胎存活及保胎治疗的重要参考依据之一。虽然生化妊娠和异位妊娠血清P水平存在交叉,难以确定它们的绝对界限,但可筛查估计其发生的临界值为进一步处理做出预测判断。李武等 根据ROC曲线指出,诊断异位妊娠等早期不良妊娠的准确度排位是:血β-h CG 48 h/0 h(AUC=0.85)变化为首选,其次是P(AUC=0.81),再次是子宫内膜厚度(AUC=0.79)。目前血清P水平国内外尚无统一标准,Stern等 报道以P为15.9 nmol/L为界鉴别异位妊娠及不能存活的宫内妊娠病人的敏感度和特异度分别为90.5%和93.3%。本研究显示,生化妊娠组P平均水平显著高于异位妊娠组,多数生化妊娠组(75.03%)病例的P在31.20~72.60 nmol/L范围内,而当血清P水平>72.60 nmol/l时,未见异位妊娠的发生,同时出现生化妊娠的概率也较低。杨燕飞等 研究认为,异位妊娠血清P水平均低于17.5 nmol/L。除去个体差异和排卵延迟等因素影响一般认为,正常血清P水平孕4周时应>15.9 nmol/L,孕5周>31.80 nmol/L,孕6周>63.60 nmol/L,低于此阈值则高度怀疑异位妊娠尤其是第4周时更为明显,此时更易鉴别正常和异常妊娠。本研究显示分别以P≤72.60 nmol/L、31.2 nmol/ml为界值预测生化妊娠及异位妊娠,其敏感度和特异度分别是84.3%、80%及70.1%、72.2%,因此提示可以以血清P值≤72.60 nmol/L作为生化妊娠的参考预测界值,以P≤31.80 nmol/L为异位妊娠的参考预测值。这虽然可作为从宫内妊娠中筛查的参考依据,但在生化妊娠、宫内早孕与异位妊娠三者之间此P水平仍存在一定程度交叉,因此误诊易发生在交叉值处。有报道在异位妊娠中,当β-h CG低于5 000 m IU/m L时,血清孕酮和β-h CG的水平呈正相关,而在正常和异常宫内妊娠者并无此正相关关系;本研究虽未显示此种相关性但提示当血清P 48h呈下降趋势时提示发生生化妊娠的几率较大。
3 血清β-h CG的48 h动态水平趋势
一般孕卵受精的第7~10天即可检测出血清β-h CG>10 IU/L以上,孕5周达1 000 IU/L以上 ,临床上虽然受排卵延迟、胚胎发育个体差异以及检测误差等因素影响,β-h CG值随孕周变化有较大幅度的波动,但活性良好的胚胎β-h CG水平有隔日倍增的动态变化规律,当绒毛发育不良或滋养细胞凋亡或接近凋亡时分泌的β-h CG量就会明显减少,因此有学者 认为,当早孕≤7周时以血清β-h CG 1 500 IU/L为预测界值来鉴别异位妊娠,其敏感度为84.9%,特异度为89.6%,ROC曲线下面积为0.922。本研究认为当早孕≤6周时分别以血清β-h CG 1 000 IU/L及2 400 IU/L作为异位妊娠和生化妊娠的预测界值,其敏感度分别是83.4%、85.5%,特异度分别为84.5%及75.7%,此与国内多数学者结论相近。Chung等 研究认为,血清β-h CG水平的连续动态测定对生化妊娠、异位妊娠等的鉴别诊断较有意义,在正常妊娠的4~8周,β-h CG水平2 d内即可增加一倍,最低可增长50%以上。本研究显示,生化妊娠的48 h血清β-h CG上升幅度<50%(或β-h CG 48 h/0 h<0.5)所占比率低于异位妊娠,前者可能是胚胎着床前已停止发育、滋养细胞开始逐步凋亡并停止分泌h CG,后者则因血供差、滋养细胞数量少及生长缓慢h CG分泌较少。研究还显示两者间48 h血清β-h CG水平下降比率有不同,生化妊娠组48 h血β-h CG下降比率要多于异位妊娠组,即大部分生化妊娠患者48 h血β-h CG水≤平呈下降趋势;这与胚胎停育和体内β-h CG半衰期较长有关。故提示临床当48 h血清β-h CG水平未呈上升趋势或幅度较小尤其呈下降趋势时结合预测界值应首先考虑有可能是生化妊娠。
4 三指标联合预测
当早孕≤42 d有不规则阴道出血,无典型下腹痛和里急后重,阴道超声宫内宫外均未见孕囊及盆腔包块或积液短期难以做出判断时,为能给早期准确诊断提供预测参考范围可在详细询问病史、注重临床表现基础上联合三指标检测,进一步完善相关辅助检查。即当血清β-h CG≥2 400 IU/L且隔日翻倍、P≥72.60 nmol/L、B超宫内外虽未见孕囊及包块但子宫内膜增厚≥10 mm,则宫内妊娠可能性大;当血清β-h CG≤2 400 IU/L、48 h血清β-h CG水平基本平稳尤其呈下降趋势、P≤72.60 nmol/L及子宫内膜厚度≤10 mm时发生生化妊娠的几率较高;当血清β-h CG≤1 000 IU/L、48 h血清β-h CG水平上升≤50%、P≤31.20 nmol/L及子宫内膜厚度≤8 mm时要警惕异位妊娠的发生,上述综合指标检测预测PUL的敏感度分别为91.6%、94.7%、84%,特异度分别为84.5%、81.3%、76%,故可作为PUL的早期诊断参考指标。若同时合并盆腔附件增厚或包块囊肿与异位妊娠难以鉴别时,可详细追问病史,必要时可行改良诊刮术、后穹隆穿刺及腹腔镜等及时排除异位妊娠诊断。结合临床表现为临床早期筛查提供参考意见,有效提高早期诊断准确率,避免过早干预或将宫内早孕误诊为宫外孕,造成不必要的医疗纠纷 。
生化妊娠筛查及药物流产临床效果观察
目前由于尿妊娠试验试纸的精度提高及科普知识的宣传, 使得非意愿妊娠的妇女提早自我检测和就医, 有大量的门诊患者要求尽早明确诊断并给予相应处理。通常让处于生化妊娠的非意愿妊娠妇女等待10d左右直至超声确诊后再予相应的处理, 依然是目前处理生化妊娠的主要方法。制约生化妊娠早期治疗的主要因素:①生化妊娠阶段无法排除异位妊娠。②生化妊娠阶段终止妊娠不便于临床观察效果。但待确诊后无论是宫腔内妊娠人工流产或药物流产, 还是宫腔外妊娠保守或手术治疗, 带给患者的身心与经济压力均较大。
hCG是人绒毛膜合体滋养层细胞分泌的多肽类激素, 由α亚基和β亚基以非共价键形式结合而成, 对维持正常妊娠有重要意义。正常妊娠在排卵后7~10d开始能测到β-hCG, 孕5周时血β-hCG达1 000IU/L以上。
人体孕激素是雌激素合成的前体, 由卵巢、胎盘和肾上腺皮质产生, 主要来源于卵巢的卵泡膜细胞和排卵后的黄体细胞。血清孕酮在8周前维持一定水平, 即“非孕龄依赖”。陈远征报道以17.5nmol/L为临界值区别宫内与宫外孕的诊断效率为99.4%。
因此, 对生化妊娠阶段病例应用血清β-hCG联合P检测排除异位妊娠, 共筛查196例, 临床证实均为宫内妊娠, 为后续药物流产提供了依据, 减少医疗隐患。
米非司酮配伍米索前列醇终止停经49d之内宫内妊娠, 多年来大量临床病例证明安全有效, 但出血量较多、时间偏长、完全流产率76%左右, 一直困扰着临床医生。
本组观察提示, 生化妊娠组药物流产的完全流产率达97.37%, 明显高于常规早孕组, 且出血时间、总量明显较对照组减少。与张大荣、戚小霞报道结果相符。
对于特别早期的生化妊娠流产时, 无法观察到孕囊排出, 需注意以下问题:凡经历经量增多, 一度达到或超过月经量, 后减少, 也是流产的一个信号。1周后及时复查B超, 见子宫内膜厚度明显变薄、宫腔线清晰、附件等无异常包块回声, 提示完全流产, 否则应提高警惕, 结合出血量等决定严密随访或及时清宫。
综合上述临床结果, 可以认为血清β-hCG联合孕酮(P) 检测可有效排除早期不典型异位妊娠, 应用米非司酮配伍米索前列醇终止生化妊娠安全、有效, 值得临床进一步推广使用。
生化妊娠早期治疗效果分析
目前由于尿妊娠试纸的精确度提高及科普知识的宣传, 使得非意愿妊娠的妇女提早自我检查和就诊, 所以生化妊娠率明显提高, 制约生化妊娠早期治疗的主要因素1、生化妊娠阶段无法排除异位妊娠;2、生化妊娠阶段终止妊娠不便于临床效果观察.但让处于生化妊娠的非意愿妊娠妇女等待10天左右直至超声确诊后无论是宫内妊娠人工流产或药物流产还是宫外妊娠或手术治疗, 带给患者的身心与经济压力均较大.近年来异位妊娠发病率明显升高, 有报道原来异位妊娠发病率为2%, 而近年增至2-3倍, 异位妊娠的早期诊断决定治疗方法的选择及预后情况, 因此早期诊断治疗尤为重要.异位妊娠患者的早期保守治疗方案, 目前有效的为米非司酮配伍甲氨蝶呤, 米非司酮可抑制胚胎生长, 因此生化妊娠阶段应用米非司酮为今后的保守治疗异位妊娠奠定了基础.
总之, 生化妊娠尽早实施药物治疗, 可减少异位妊娠破裂发生率, 也可减少不完全流产时大出血, 减少了异位妊娠手术及人工流产手术的机率, 治疗效果是显著的.
生化妊娠尽早治疗固然好, 但应注意告知有宫内妊娠及宫外妊娠可能, 并签治疗同意书, 亦可选择中药治疗.
体外受精-胚胎移植治疗中卵子和胚胎质量对生化妊娠周期的影响
体外受精-胚胎移植技术(IVF-ET) 是最为广泛运用的辅助生殖技术, 当前IVF-ET发展迅速, 获得的成果有目共睹, 然而从实际数据看, IVF成功率不高, 生化妊娠还在其中占了不小比例, 原因暂不明确[1,2,3]。本研究探讨卵子、胚胎的质量对生化妊娠周期的影响, 以期发现生化妊娠出现的原因, 提高治疗成功率。
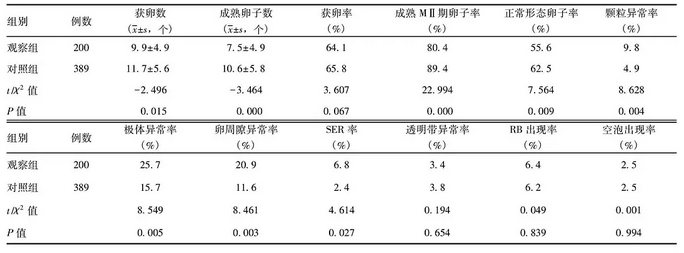
观察组与对照组卵子质量比较
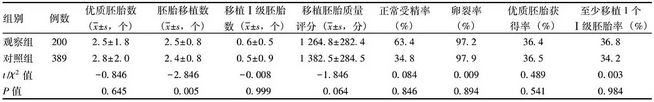
两组胚胎质量对比
IVF-ET治疗可解决女方因输卵管病变导致精卵结合困难、子宫内膜异位症、排卵困难, 以及男方少精、弱精症导致不孕, 最初的1978年的第一例试管婴儿被称为人类医学史上的奇迹, 此后该项技术因其实用性不断进步, 力图在前人的基础上提高其成功率。
通过两组一般情况及卵子、胚胎质量对比可以发现, 卵子质量与胚胎质量是IVF-ET成功与否的重要影响因素。本研究中, 两组平均年龄差异无统计学意义, 但观察组年龄≥35岁患者明显较多, 毫无争议的是年龄较大导致了卵子质量下降, 具体表现为观察组成熟MⅡ卵子率明显低于对照组, 且运用目前最为普遍的卵子形态学特征观察来进行卵子质量评定, 发现进行ICSI的观察组卵子更易出现异常。异常形态卵子再发育为胚胎会使囊胚形成难度加大, 而对异常形态的卵子进行染色体检查, 该类卵子易产生非整倍体, 文献推测异常是在卵子发育与成熟时发生的。综合各种因素显示, 观察组患者年龄较大导致的卵子质量下降是生化妊娠发生的重要原因。卵子异常也导致了胚胎质量的下降, 讨论胚胎质量对生化妊娠的影响, 临床上仅通过最常用的观察胚胎的形态学特征进行胚胎质量判定是不合适的, 并不能完全代表胚胎质量。在取卵后3 d IVF-ET治疗要求进行卵裂期的胚胎移植。早期提出的原核期卵裂期的胚胎质量评分经过近年发展有了较为成熟的综合评分体制, 进行了原核期卵裂期胚胎形态与发育阶段的综合考虑。以此种标准本研究比较了两组的正常受精率、卵裂率、优质胚胎形成率, 另外本研究认为移植胚胎的实际质量并不能被移植前的总体胚胎质量代表, 进行了针对移植胚胎的原核期和D3卵裂期的观察, 其形态学特征表现出来的综合评分, 这些数据显示两组之间的胚胎质量的形态学特征表现出来的差异并无统计学意义。但结果表明这些胚胎着床率差异很大, 成功率也很不同。文献显示胚胎染色体异常是这种情况的原因, 形态学特征并不能显示出染色体异常, 即形态学特征表现为优质胚胎的胚胎也有25%发生染色体异常使其无法正常着床。据研究结果进行推测, 卵子质量较差可能影响了胚胎质量导致了生化妊娠的出现。
生化妊娠的产生原因是胚胎着床的失败, 具体过程尚不清楚。但本研究发现卵子质量的差异可导致生化妊娠。可以通过遗传学检查来保证卵子的形态和染色体状态都为优质, 从而改善卵子质量导致生化妊娠的结果。但是生化妊娠的确切原因还需要进一步的研究来降低其发生率。
让处于生化妊娠的非意愿妊娠妇女等待、随访至能够用超声诊断有孕囊后再予以治疗, 是处理生化妊娠的主要方法。目前, 由于生殖健康知识的普及, 加之用于诊断早孕试纸的精度提高, 使得许多非意愿妊娠的妇女提早自我检测, 在月经未到期或超过1~2d即来就诊, 本研究中有16例未到停经日期就通过自测尿妊娠试验, 疑似阳性来就诊, 经过血清β-hCG和B超检查确认为生化妊娠。本组观察显示, 米非司酮配伍米索前列醇用于终止血清β-hCG≤2 000U/L的生化妊娠, 其完全流产率达到98.5%( 110/112) , 尤其对血清β-hCG﹤500U/L的生化妊娠, 完全流产率达到100%, 说明药物终止生化妊娠同药物终止早期临床妊娠一样, 妊娠时间越早, 血清β-hCG的水平越低, 药物流产的效果就越好。大量文献及临床均证实, 药物终止妊娠的孕期越短, 各项副作用均越轻, 李翠兰等研究认为对早孕者越早施以药物流产, 其发生多量或长期出血的可能性越小。为了验证生化妊娠阶段是否也有同样的规律, 本研究将观察组分为血清β-hCG﹤500U/L和β-hCG 500~2 000U/L两组生化妊娠, 通过观察, 药物终止生化妊娠同样具有用药越早, 其后出血量多或时间长的可能性越小。
生化妊娠阶段无法排除异位妊娠的可能, 是临床药物终止生化妊娠的最大顾虑, 为此本研究对观察组选择终止生化妊娠病例的停经时间和血清β-hCG的值进行了严格控制, 特别对血清β-hCG控制在2 000U/L以内。本次研究观察组对象(Ⅰ组、Ⅱ组) 无异位妊娠情况, 并不能说明观察对象中一定无异位妊娠病例, 不排除有处于生化妊娠阶段的异位妊娠病例的存在, 所以知情同意和严密随访显得非常重要。当然目前临床已有大量有关米非司酮保守治疗异位妊娠的报道, 这也为米非司酮用于异位妊娠的生化妊娠阶段的安全性提供了实践依据, 表明不一定需要等到排除异位妊娠, 确定为宫腔内临床妊娠后再行处理。
临床早期妊娠妇女服用药物后恶心、呕吐的副作用明显高于生化妊娠妇女, 是早孕反应和药物不良反应的叠加作用, 而并非是服用药物的副作用;生化妊娠阶段一般尚无早孕反应, 所以此阶段服用药物后的恶心呕吐反应比例小, 从而可使药物的吸收更加完全, 血药物浓度更高, 达到杀胚胎的效果, 提高完全流产率;发生腹痛的对象生化妊娠者也少于临床妊娠者, 且均能忍受, 这与生化妊娠宫腔内组织少, 相应的子宫收缩强度弱有关, 一般孕囊排出后或服用米索前列醇12h后好转, 不必特殊处理。
总之, 米非司酮配伍米索前列醇终止生化妊娠完全流产率高于终止临床早期妊娠, 阴道流血时间更短, 恶心、呕吐、腹痛等副反应发生更少。
移植术后第14天血清β-HCG对辅助生育妊娠结局的预测
辅助生育技术已成为治疗不孕不育症的有效方法,由于多年的不孕不育经历以及高达22%的不良妊娠结局使得施行辅助生育的妇女经历巨大的精神压力,因此早期预测妊娠结局对患者的精神状态以及临床决策的选择都有非常重要的作用。既往研究表明移植术后早期β-HCG水平可以很好预测妊娠结局,然而血清β-HCG预测值在不同研究中可能由于检测时间、方法、移植胚胎时间以及培养体系等不同存在明显差异,因此分析不同移植周期中血清β-HCG对妊娠结局的预测值就显得至关重要。 国内外研究均有报道鲜胚周期移植后血β-HCG的预测值 范围,但对于冷 冻周期移 植(FET)后血 β-HCG预测值报道甚少。本研究旨在比较移植术 后第14天血清β-HCG在预测新 鲜周期移 植与FET不同妊娠结局上的差异。
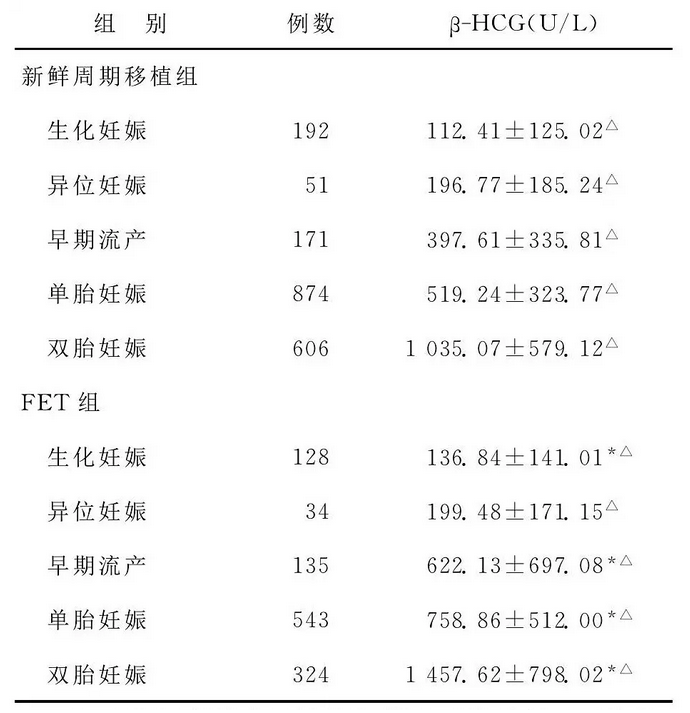
新鲜周期与 FET 第14天血清β-HCG水平(±s)
注:新 周 组 冷 周 组 亚 组 两 比, △P<0.05;冷 周 组 新 周 组 应 组 两 较,*P<0.01
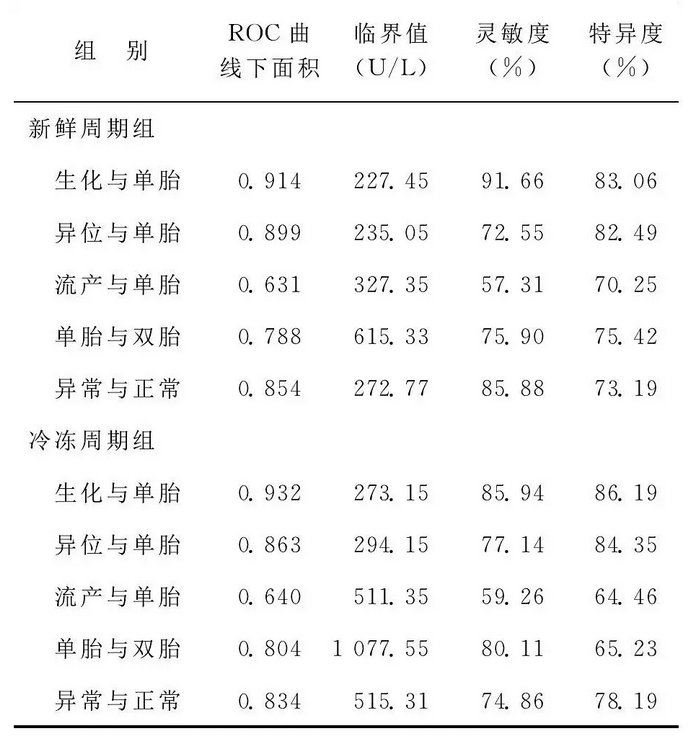
不同亚组间β-HCG切割值以及灵敏度特异度
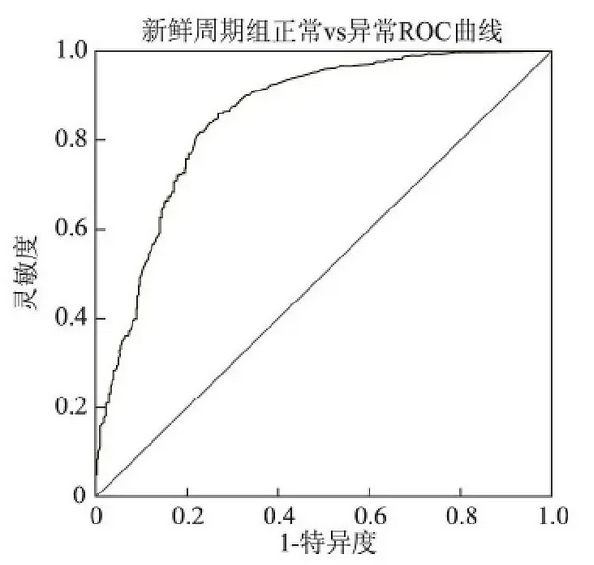
IVF-ET/ICSI新鲜周期移植后正常妊娠 ROC曲线
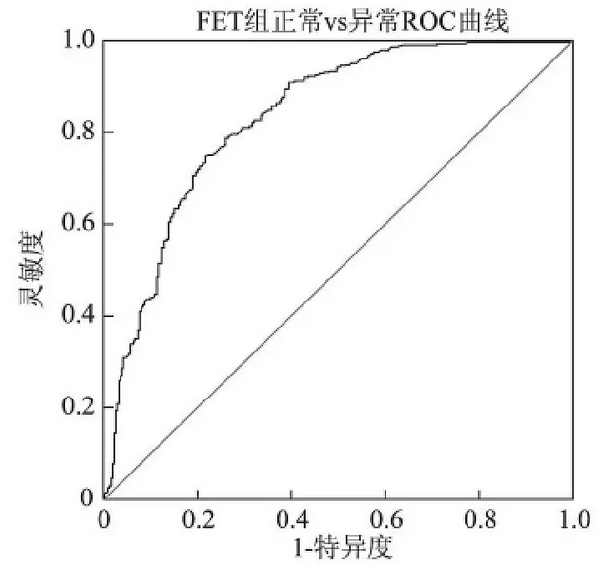
FET 后正常妊娠与异常妊娠 ROC曲线
辅助生育中随着冷冻技术的逐渐发展,FET在临床中发挥了非常重要的作用。Khalaf等报道提示冷冻周期的妊娠率低于新鲜周期,且流产率高于新鲜周 期。 但有学者 报道两者 相比无明 显差异。因此早期预测FET的妊娠结局显得尤为重要。早期HCG水平主要代表的是滋养细胞层的大小和功能,多项研究表明,在新鲜移植周期血清HCG水平对妊娠结局的预测发挥了重要的作用,然而预测数 值各项研 究均有差 异。 分析其影 响血 β-HCG水平的可能因素,有研究提示胚胎培养体系的差异会影响胚胎生长速度和胚胎种植。研究表明,冷冻周期和新鲜周期比较,不同冷冻技术对血 β-HCG水平将产生影响,玻璃化冷冻技术对胚胎冷冻的损伤明显减少,妊娠率明显增高,其移植早期孕妇血β-HCG水平明显增高。还有学者提出,子宫内膜的不同准备方法也影响胚胎的种植,新鲜周期与冷冻周期β-HCG的差异也可能与内膜准备情况差异有关。早期血清β-HCG水平与移植时间密切相关,Kathiresan等研究表明,移植第5天的胚胎与移植第3天胚胎相比,血清HCG水平明显增高。本文提示冷冻周期移植组移植后第14天血清β-HCG水平均明显高于新鲜周期移植组,除异位妊娠组外差异均有统计学意义。推测冷冻周期与新鲜周期虽然都为移植第3天胚胎,但胚胎植入内膜发育存在先后,根据血β-HCG的水平推测在冷冻周期胚胎着床时间可能更早于新鲜周期,但还需要进一步的实验证实。
由于正常妊娠和异常妊娠组,血清β-HCG水平存在一定的的重叠,单一血清β-HCG水平无法预测妊娠结局,因此通过ROC曲线法寻找不同妊娠结局间的切割值,可以作为推测妊娠结局的重要指标。 Urbancsek等研究发现,移植术后11dβ-HCG< 50 U/L可预测生 化妊娠。Poikkeus等通过ROC曲线确定774例妊娠患者移植术后12d血清 β-HCG值水平,认为76U/L为活胎和不良妊娠的最适切点值。徐蓓等通过ROC曲线对采 卵后16d血清β-HCG水平做回顾性分析,发现当β-HCG值>500U/L,继续妊娠率达95 %,其生化妊娠、单胎妊娠、双胎妊娠 的切割值 分别为134 U/L、 375U/L和690U/L。李艳等提示正常妊娠组与流产组临界值197.27U/L,多胎妊娠组与单胎妊娠组临界值613.94U/L。本文数据提示:新鲜周期移植组血清β-HCG水平<227.45U/L生化妊娠可能性大,血清β-HCG<235.05 U/L异位妊娠可能性大,血清β-HCG<327.35U/L有可能早期流产,当血清β-HCG水平>615.3U/L,双胎妊娠的可能性大。在FET组,β-HCG<273.15U/L时,生化妊娠可能性大,β-HCG<294.15 U/L,存在异位妊娠风险,β-HCG<511.35U/L早期流产风险增高,血清 β-HCG>1 077.55U/L时,双胎可能性大。在新鲜周期组,本文数据与既往研究结果趋势相同,并且双胎的切割值接近。
比较正常妊娠与异常妊娠组,新鲜周期的血清 β-HCG切割值为272.77U/L,ROC曲线下面积为0.854,其预测的灵敏度和特异度分别为85.88%、 73.19%。FET周期两组 的血清β-HCG切割值515.31U/L,ROC曲线下面积为0.834,其预测的灵敏度和特异度分别为74.86%、78.19%。提示在新鲜周期移植后血清β-HCG>272.77U/L正常妊娠可能性大。FET后血清β-HCG>515.31U/L正常妊娠可能性大。冷冻周期的血β-HCG切割值明显高于新鲜周期。可能原因是由于冷冻周期激素水平、子宫内膜 状态更接 近于自然,利于胚胎 着床, FET时间早于新鲜周期,造成血β-HCG水平早期升高明显,也可能存在冷冻技术对于胚胎质量及滋养细胞的影响,故在冷冻周期需要更高的血β-HCG水平才能预测正常妊娠结局。切割值的提出可以告知患者妊娠成功及不良妊娠的可能性。一方面缓解患者的不良和焦虑情绪,同时可以更好地指导患者进一步治疗方案是选择放弃还是继续保胎治疗,避免盲目保胎带来的进一步伤害。对于血β-HCG水平低于正常切割值范围的患者可采用复查48h后血HCG的方法更好地指导临床决策。
本研究的局限在于可能存在的选择偏移。部分患者血β-HCG当地检测,未列入研究范畴。为防止检测方法差异,数据均选择为我院检测β-HCG水平者。本研究尚存在一定缺陷:未按照不同病因、不同治疗方案及不同内膜准备方案分类分析预测值,因不同原因行IVF助孕患者血清β-HCG水平也存在差异,因此在今后的研究中可细化分类后统计不同原因及不同助孕方案后血清β-HCG水平对妊娠结局的预测意义。
本研究表明移植术后第14天血清β-HCG水平可以很好预测新鲜周期移植以及FET后妊娠的持续性以及病理妊娠的可能性,且发现在冷冻周期中需要更高的血β-HCG水平才能预测正常妊娠。由于检测仪器、所用试剂和测定方法检测时间,移植时间胚胎冷冻复 苏技术等 的不同,不同研究 中血清 β-HCG值可能存在一定的差别。本文报道的HCG水平的切割值不一定适合其他生殖中心。因此,各中心需根据自身的数据总结提出适用于本中心的切割值,从而更好地指导临床治疗。
以孕酮水平确定冻融胚胎移植时间的临床研究
在FET方案中,自然周期的应用十分广泛。因P的浓度及作用时间在内膜的转化及种植前准备中发挥了最为关键的作用,故我们提出了这种通过检测排卵后血清P水平确定FET时机的方法。这种方法的关键是如何确定P的界值。通过文献得知,自然周期中,排卵日的P升高并不显著,D1的P水平也在9.54nmol/L以下;随后,P水平逐渐升高,D2 的P水平在9.54~19.08nmol/L;D3 的P水平约19.08~25.44nmol/L;D4的P水平升至25.44~31.8nmol/L。本研究连续监测月经周期正常的志愿者的血清P水平,也得到了相似结果。
在MPR方案中,我们设定P≤9.54nmol/L为排卵日(D0),9.54nmol/L
为了证实MPR方法的有效性,我们将MPR治疗患者的结局与MOR组进行比较。本研究结果提示,在基本情况及周期治疗情况具有可比性的患者中,MPR治疗可以获得与MOR相似的临床结局。两组的临床妊娠率、持续妊娠率及种植率无显著性差异。表明MPR在确定FET时机方面具有与传统MOR法相似的效果。事实上,两种治疗方法确定的移植时间并不完全一致,但是相似的结局可能提示内膜的容受性是一段时间而不是特定的时间点。既往的研究也发现胚胎的种植窗从P作用的48h以后开始,并可能持续4d。
尽管没有证据支持MPR方案优于MOR方案,但是MOR组有着更高的生化妊娠率。多元因素回归分析也显示MPR是降低生化妊娠的孤立因素。MPR可能有助于降低生化妊娠率。通常认为只有生化妊娠(而无临床妊娠)意味着胚胎着床的失败,由于两种治疗方法确定的移植时间并不完全一致,使移植时内膜的转化程度也不尽相同,这可能导致了子宫内膜的容受性及胚胎着床结局的差异,即两组生化妊娠率的差异可能是由移植方案确定的移植时机不同引起的。BMI是另外一个影响生化妊娠率的因素,虽然具体原因仍不清楚,但是已有研究发现过高或过低的BMI均与FET后流产相关。
虽然我们未能证实MPR在治疗结局上的优越性,但是与MOR相似的妊娠率及以下优点使其更具应用价值:首先,MPR可能发现一些潜在的黄体功能不全患者。在治疗中我们发现个别患者在B超确定排卵后P不出现升高,隔日再次检测P水平上升仍不明显,甚至无上升。这种现象可能是黄体功能不全的一种表现,而MPR可以筛选出这类患者,并于下个周期可采用人工周期FET,避免移植后的不良结局。 其次,即使发生未破裂卵泡黄素化,MPR仍可决定移植时机。通常发生未破裂卵泡黄素化时,MOR很难确认排卵时机,从而增加了FET的周期取消率,而只要P水平达到设定值,MPR仍能通过P水平确定移植时机。最后,MPR方法方便了患者。患者不再需要频繁来到医院密切监测卵泡生长,只要确定有优势卵泡发育且排卵即可通过一次血清检测确定移植时机。
越来越多的研究表明,新鲜周期的分泌前期内膜处于“亢进”的状态,并不适合胚胎的种植。同Gn刺激下的新鲜周期内膜相比,FET周期的内膜更易于控制,因此FET周期中胚胎及内膜发育的同步化将更有利于妊娠。不同于以往的认识,近期的随机对照研究同样证实,FET周期的妊娠率显著高于新鲜周期移植,且FET可能有助于改善持续妊娠率及IVF治疗的结局。这些事实都提示,FET可能是进一步提高IVF治疗效果的有效手段,而我们的研究旨在寻找更合适的FET时机,并为提高FET临床结局提供新的思路。
在自然周期FET的患者中,通过使用MPR可以获得与MOR相似的临床妊娠率及持续妊娠率,但MPR可能有助于降低只有生化妊娠(而无临床妊娠),即降低妊娠丢失率。目前,我们的研究暂无充分证据表明MPR与MOR的优劣性,故仍需要扩大样本量得出进一步结论。然而,MPR在应用中也显示了自身的一些优点,本结果为进一步开展P为基础的自然周期FET方案提供了依据。
孕酮和HCG联合检测在诊断生化妊娠中的意义
生化妊娠是指受精卵结合着床失败, 受精卵着床于受精卵形成后一周左右开始, 包括定位、附着和植入三个过程, 其中任何一个过程出现问题均可导致生化妊娠, 实质上亦属于早期流产的一种, 仅血中可检测出HCG的升高而B超检查无法显示孕囊形成。生化妊娠发生的原因尚未完全明了, 与胎儿及母体因素均有关, 其中子宫的容受性、母体激素的分泌及胎儿的质量与生化妊娠的关系密切。生化妊娠的误诊或漏诊对患者及家庭影响严重, 因此早期准确的诊断尤为重要。临床上对早期流产的诊断主要依靠B超, 该方法效果显著, 但对于生化妊娠很难发现。孕酮及HCG的检测可起到较好诊断作用, 但研究表明单独一种检测仍具有较大误诊率。
B超是临床检测早期妊娠及流产的常用方式之一, 其有效性能较高, 正常妊娠一般在孕5周左右即可通过阴道超声查见孕囊, 孕囊继续生长, 当其直径达10mm以上且血HCG值达3000IU/L时即可通过B超查见卵黄囊。但B超对生化妊娠的早期识别仍有较大盲区。目前尿妊娠实验的精度和准确度都有了一定的提高, 患者的提早自我要求诊断意识也较强, 由于B超诊断的有限性, 生化妊娠很难与异位妊娠及其他原因早期流产相鉴别, 给患者及家庭带来极大困扰, 也对医疗诊治造成较大阻力。因此, 寻求一种早期准确而有效的诊断生化妊娠的方法成为临床关注的重点。
HCG是一种由α和β两种亚基以共价键的形式结合而成的由人绒毛膜合体滋养层细胞分泌的多肽类激素。其中, β亚基具有较高的生物活性及免疫反应特性, 故检测时一般以βHCG为主。正常妊娠在孕后7d左右可检测到HCG的分泌, 前3周分泌速度最快, 8周时达总量最高峰。生化妊娠时由于母体激素分泌缺陷, 合体滋养层细胞发育不良, 常导致HCG分泌严重不足, 高峰时间也叫正常妊娠推迟3~8d。本研究结果中显示, 正常妊娠组HCG量平均为(12417.5±301.9) IU/m L, 而生化妊娠组仅为(9831.5±220.8) IU/m L, 两组相比差异显著, 经统计学分析, P<0.05。究其原因, 除母体合成或分泌h CG功能受限外, 可能与胎儿本身的质量或着床位置有密切联系。有研究表明, 生化妊娠与胚胎代谢关系密切。
孕酮是由母体卵巢的卵泡膜细胞和排卵后形成的黄体细胞合成, 与卵巢、胎盘及肾上腺皮质三者均相关。早期妊娠监测孕酮可作为黄体功能及胚胎发育的一个较好的评价指标, 与HCG不同的是孕酮反应的是滋养层细胞的功能而非存活状态。生化妊娠时, 母体滋养层细胞功能较正常妊娠弱, 故孕酮的合成分泌较少。本研究结果中显示, 正常妊娠组孕酮量平均为(35.7±2.8) ng/m L, 而生化妊娠组为(19.5±1.4) ng/m L, 两组相比差异显著, 经统计学分析, P<0.05。
本研究以于我院治疗的生化妊娠患者为研究对象, 拟探讨孕酮及h CG联合检测对生化妊娠的早期诊断价值, 结果显示:单独行孕酮检测诊断生化妊娠的准确率为76.56%, HCG检测准确率为63.28%, 两组均显著低于联合检测组的84.37%, 经统计学分析, P<0.05。孕酮检测诊断生化妊娠的灵敏度78.78%, 特异度为74.19%, HCG检测灵敏度为63.63%, 特异度为62.75%, 两组均显著低于联合检测组, 经统计学分析, P<0.05。综上所述, 孕酮联合HCG检测可更好地诊断生化妊娠, 利于患者早期诊断, 具有高准确率, 特异性、灵敏度高等优势, 值得临床推广应用。