周彩存教授:2020年肺癌治疗进展大盘点
1月31日,由北京市希思科临床肿瘤学研究基金会、东方临床肿瘤研究中心与中国医药创新促进会抗肿瘤药物临床研究专业委员会共同主办的“2020抗肿瘤新药研究及肿瘤治疗年终大盘点”以线上会议的形式顺利召开。会议期间,同济大学附属上海市肺科医院周彩存教授分享了2020年度非小细胞肺癌(NSCLC)治疗领域的重要进展。
01 靶向治疗
EGFR突变
辅助治疗
ADJUVANT CTONG1104研究
2020年最重要的研究进展之一当属ADJUVANT CTONG1104研究。该研究首次证实,辅助吉非替尼治疗对比标准双药化疗可显著改善EGFR突变阳性II-III(N1-N2)期NSCLC患者无病生存期(DFS)。既往结果显示,两组的中位DFS分别为28.7个月和18.0个月(HR=0.6,P=0.0054)。
2020 ASCO大会上,该研究公布了随访80个月时,OS最终分析结果以及DFS更新结果。更新结果显示,吉非替尼组和化疗组的中位DFS分别为30.8个月和19.8个月(HR=0.56,P=0.001),两组的中位OS分别为75.5个月和62.8个月(HR=0.92,P=0.674)。两组的5年OS率分别为53.2%和51.2%。
ADAURA研究
III期ADAURA研究旨在评估IB-IIIA期EGFR敏感突变的NSCLC患者在手术完全切除±辅助化疗后,分别接受奥希替尼和安慰剂辅助治疗(3年)的疗效和安全性。主要终点为研究者评估II-IIIA期患者的DFS,次要终点包括DFS(全人群)等。
2020年4月,由于奥希替尼在EGFR突变阳性NSCLC辅助治疗中取得压倒性疗效,孤立数据监察委员会(IDMC)建议提前揭盲,2020年ASCO大会上,ADAURA研究重磅公布研究结果。
2020 ESMO大会上,ADAURA研究再次公布更新结果并同步发表《NEJM》杂志。最新结果显示,在470例II-IIIA期患者中,与安慰剂相比,奥希替尼使II-IIIA期患者的中位DFS显著延长,两组的中位DFS分别为未达到和19.6个月(P<0.001,HR=0.17)。总人群(IB-IIIA,682例)中,奥希替尼组的中位DFS同样显著优于安慰剂组,分别为未达到和27.5个月(HR=0.20,P<0.001)。两组的2年DFS率分别为89% vs 52%。
奥希替尼组和安慰剂组中,分别有2%和11%患者发生中枢神经系统(CNS)相关疾病复发或死亡,分别有1%和10%患者发生CNS复发。
EVIDENCE研究
EVIDENCE研究是一项多中心、随机对照III期研究,旨在评估埃克替尼对比标准辅助治疗用于II-IIIA期EGFR敏感突变NSCLC患者术后辅助治疗的疗效和安全性。主要终点为DFS。
2020 WCLC大会上,周彩存教授公布了更新结果,结果显示,与化疗组相比,埃克替尼显著延长了患者DFS,两组的中位DFS分别为46.95个月和22.11个月(HR=0.36,P<0.0001)。亚组分析显示,所有亚组中,埃克替尼组的DFS均优于化疗组。
术后辅助TKI之争议:辅助治疗能否单靠DFS指导用药,是否需要OS的改善,还有待进一步证实。目前来看,DFS改善之后,至少首先改善了患者的生存质量,若能进一步改善OS,治疗模式和方案必定写入指南。
EGFR突变晚期NSCLC的治疗
按EGFR突变类型相关临床研究汇总
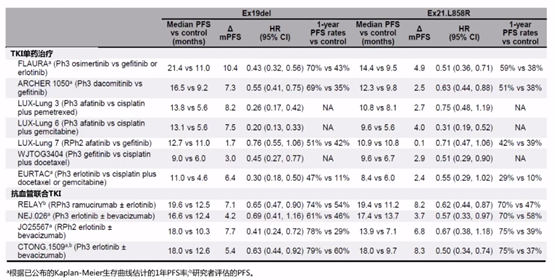
中国学者在2020 ASCO大会上公布了一项III期临床研究,结果提示,放疗在寡转移NSCLC患者中占据重要地位。
SINDAS旨在评估EGFR TKI±局部放疗在EGFR突变寡转移患者中的疗效。结果显示,中位随访19.6个月时,EGFR TKI+放疗和单药组的中位无进展生存期(PFS)分别为20.2个月和12.5个月(HR=0.6188,P<0.001),中位OS分别为25.5个月和17.4个月(HR=0.6824,P<0.001)。
EGFR TKI+局部放疗可显著改善寡转移患者的PFS和OS。即使在晚期NSCLC中,MDT讨论仍有重要意义,研究提示,放射治疗可使患者有更好的临床获益。
CHRYSALIS研究
对于20外显子插入突变患者,一线标准治疗方案仍是铂类化疗,后续治疗无明确选择方案。Amivantamab(JNJ-61186372)是一种新型、全人源化EGFR-MET双特异性抗体,可靶向经典EGFR突变和EGFR耐药突变以及MET突变、MET扩增。
2020年3月,双特异性抗体Amivantamab获FDA突破性疗法认定,用于含铂化疗期间或之后进展的EGFR 20外显子插入突变转移性NSCLC患者。2020 ASCO、2020 ESMO、2020 WCLC大会上,CHRYSALIS研究接连公布更新结果。最新结果显示,中位随访9.7个月时,研究者评估的ORR为40%,临床获益率(CBR)为74%。中位缓解持续时间(DOR)为11.1个月。
EXCLAIM研究
2020 WCLC大会上,周彩存教授首次公布了I/II期EXCLAIM研究扩增队列的结果,以及既往接受含铂治疗队列的综合分析结果。结果显示,中位治疗时间为6.5个月。孤立审查委员会(IRC)评估的ORR为23%,研究者评估的ORR为32%。中位DOR未达到。IRC评估的中位PFS为7.3个月,研究者评估的中位PFS为7.1个月。在经铂类治疗队列和EXCLAIM扩增队列中,Amivantamab治疗后,分别有82%和80%患者靶病灶有缩小,该研究同样取得了令人振奋的结果。
EGFR 20外显子插入突变靶向治疗研究探索一览

ALK融合
ALK融合晚期NSCLC一线治疗选择包括克唑替尼、阿来替尼、布加替尼和塞瑞替尼。
ALEX研究
ALEX研究旨在评估阿来替尼对比克唑替尼用于初治ALK+晚期NSCLC的疗效。5年更新数据显示,阿来替尼组中位OS仍未达到(成熟度仅37%),克唑替尼组的中位OS为57.4个月。阿莱替尼组和克唑替尼组的5年OS率分别为62.5%和45.5%。该研究提示,对于ALK+患者,一线治疗首选阿来替尼,更多患者可以得到“治愈”。
eXalt3研究
III期eXalt3研究旨在评估恩沙替尼对比克唑替尼用于初治ALK+患者的疗效和安全性。2020 WCLC大会上公布的更新结果显示,2020年12月8日数据截止时,中位随访时间为27.6个月,IRC评估恩沙替尼组和克唑替尼组的中位PFS分别为31.3个月和12.7个月(HR=0.5,P<0.0001)。
恩沙替尼研究数据与布加替尼、阿来替尼接近,恩沙替尼也是疗效较好的ALK抑制剂,有望成为ALK+患者的一线治疗选择。第二代ALK抑制剂阿来替尼、布加替尼、塞瑞替尼的安全性优于克唑替尼。
CROWN研究
2020 ESMO大会上,III期CROWN研究首次公布结果,该研究旨在评估劳拉替尼对比克唑替尼在初治ALK+ NSCLC患者中的疗效和安全性。2020年3月20日截止数据时,BICR评估的劳拉替尼组和克唑替尼组的中位PFS分别为未达到和9.3个月(HR=0.28,P< 0.001),两组的客观缓解率(ORR)分别为76%和58%。OS数据尚未成熟,仍需进一步随访。劳拉替尼的安全性与克唑替尼类似。
少见突变
MET外显子14跳跃突变
MET外显子14跳跃突变相关靶向药物疗效汇总和获批情况

HER2突变
2020 ASCO大会上,II期DESTINY-Lung01研究公布了DS-8201在HER2突变晚期NSCLC患者中的疗效。2019年11月25日数据截止时,中位随访时间为8个月。孤立评审委员会(ICR)确认的ORR为61.9%,疾病控制率(DCR)为90.5%,中位PFS为14个月。研究结果令人鼓舞,研究者拟在中国开展相关研究。
KRAS G12C突变
2020年11月,I期CodeBreak 100研究结果发表于《NEJM》杂志。结果显示,中位随访11.7个月时,sotorasib用于KRAS G12C突变患者的ORR为32.2%,DCR为88.1%,中位PFS为6.3个月。此外,sotorasib在基因共存突变患者中仍表现出临床活性,但样本量较小,需增加样本量并进行进一步随访。
2020 WCLC大会上,II期CodeBreak 100研究首次公布,结果显示,124例患者基线时至少有1个可测量病灶并可评估疗效。46例患者达到确认的缓解,其中3例为完全缓解,43例部分缓解。ORR为37.1%,DCR为80.6%,中位PFS为6.8个月。
02 免疫治疗
免疫治疗用于PD-L1高表达人群
KEYNOTE-024研究
免疫治疗进展是肺癌治疗领域的巨大进步。2020 ESMO大会上,KEYNOTE-024研究公布5年随访结果。结果显示,帕博利珠单抗较化疗仍表现出更好的OS和更持久的获益。虽然化疗组有55%患者交叉至帕博利珠单抗治疗,帕博利珠单抗组5年OS率较化疗组提升近一倍(31.9% vs 16.3%),帕博利珠单抗组和化疗组的中位OS分别为26.3个月和13.4个月(HR=0.62),中位DOR分别为29.1个月和6.3个月。我们相信,免疫治疗可使部分肺癌患者长期生存。
IMpower 110研究
III期IMpower 110研究进一步验证了免疫治疗单药在经选择NSCLC患者中的疗效。
2020年10月,IMpower110研究发表于《NEJM》杂志,IMpower110研究纳入初治IV期非鳞状或鳞状NSCLC患者。结果显示,在PD-L1高表达NSCLC患者中,阿替利珠单抗组的中位OS显著优于化疗组(20.2个月 vs. 13.1个月)(HR=0.59,P=0.01)。
EMPOWER-Lung1研究
EMPOWER-Lung 1 是一项多中心、开放标签、全球III期研究,旨在评估cemiplimab用于PD-L1≥50%(肿瘤细胞)初治IIIB\IIIC\IV期鳞状或非鳞状NSCLC的疗效和安全性。2020 ESMO、2020 EMSO ASIA接连公布研究结果,最新结果显示,在PD-L1 ≥50% ITT人群中,中位随访10.8个月时,cemiplimab组和化疗组的中位OS分别为未达到和14.2个月(HR=0.57, P=0.0002),两组的2年OS率分别为50.4%和27.1%。两组的中位PFS分别为8.2个月和5.7个月(HR=0.54,P<0.0001)
研究结果再次提示我们,对于PD-L1高表达患者,可选择免疫单药治疗。但是,免疫单药治疗的疗效仍有较大改善空间,疗效如何改善是研究者目前面临需解决的问题。
免疫联合治疗
来自日本的一项II期研究纳入PD-L1 TPS≥50%初治NSCLC患者,探索了阿替利珠单抗+贝伐珠单抗用于初治NSCLC患者的疗效和安全性。结果显示,联合治疗的ORR达到64.1%。绝大多数患者治疗后肿瘤明显缩小,中位DOR为10.4个月。中位PFS为15.9个月。1年PFS率为54.9%。结果令人鼓舞,仍需III期临床研究进一步验证。
KEYNOTE-598研究
2020 WCLC大会上,KEYNOTE-598研究首次公布结果,这是一项随机,双盲,III期临床研究,旨在评估帕博利珠单抗联合伊匹木单抗相比帕博利珠单抗单药一线治疗PD-L1 TPS≥50%且无EGFR或ALK基因突变的转移性NSCLC患者是否可以进一步提高疗效。
结果显示,帕博利珠单抗+伊匹木单抗组和帕博利珠单抗+安慰剂组的中位OS分别为21.4个月和21.9个月(HR=1.08,P=0.74),中位PFS分别为8.2个月和8.4个月(HR=1.06),两组的ORR均为45.4%。帕博利珠单抗联合治疗并不能改善转移性NSCLC患者的疗效。
免疫联合化疗用于未经选择人群
晚期驱动基因阴性非鳞NSCLC一线免疫联合化疗临床研究
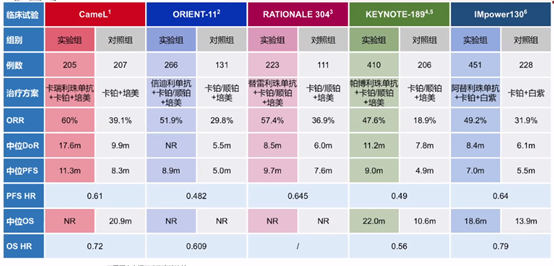
晚期鳞状NSCLC一线免疫联合化疗临床研究
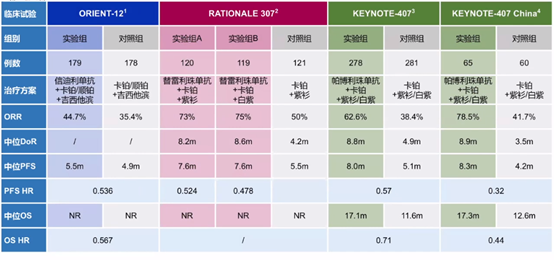
GEMSTONE-302研究
2020 ESMO ASIA大会上,周彩存教授公布了III期GEMSTONE-302研究结果,该研究旨在评估sugemalimab(一种新型PD-L1单抗,CS1001)联合化疗用于晚期NSCLC一线治疗的疗效和安全性。结果显示,研究者评估的sugemalimab+化疗和安慰剂+化疗的中位PFS分别为7.82个月和4.90个月(HR=0.50,P<0.0001),BICR评估的中位PFS分别为8.90个月和4.93个月(HR=0.54,P<0.0001)。sugemalimab+化疗可使鳞状和非鳞状NSCLC患者均获益。
双免疫联合治疗
基于CheckMate 227结果,2020年5月15日,纳武利尤单抗+伊匹木单抗获FDA批准用于PD-L1≥1%且无EGFR/ALK突变患者的一线治疗。
CheckMate 9LA
CheckMate-9LA旨在评估与单独化疗(最多4个周期)相比,纳武利尤单抗+伊匹木单抗+化疗(2个周期)一线用于转移性NSCLC患者的疗效。2020 ASCO大会上, CheckMate-9LA公布研究结果。2021年1月,该研究结果发表于《柳叶刀肿瘤学》杂志。结果显示,中位随访9.7个月时,与化疗相比,纳武利尤单抗+低剂量伊匹木单抗+化疗能为患者带来显著OS获益,中位OS分别为14.1个月和10.7个月(HR=0.69,P=0. 00065)。中位随访13.2个月时,联合组和化疗组的中位OS分别为15.6个月和10.9个月(HR=0.66)。无论PD-L1表达水平和肿瘤组织学类型(鳞癌或非鳞癌)如何,双免疫+2周期化疗组均显示出临床获益。
免疫+化疗、免疫+免疫、免疫+免疫+化疗相关研究探索
