阿帕替尼获批新适应证,肝细胞癌靶向治疗再添利器!
2020年12月30日,中国国家药品监督管理局(NMPA)官网发布公示,恒瑞医药创新研发的VEGFR-2酪氨酸激酶抑制剂(TKI)阿帕替尼(商品名:艾坦)正式在中国获批,其最新获批适应证为用于治疗既往接受过至少一线系统性治疗后失败或不可耐受的晚期肝细胞癌(HCC)。

关于阿帕替尼
阿帕替尼是一种血管内皮生长因子受体-2(VEGFR-2)的小分子酪氨酸激酶抑制剂。通过高度选择性竞争细胞内VEGFR-2的ATP结合位点,阻断下游信号转导,抑制酪氨酸激酶的生成从而抑制肿瘤组织新血管的生成,最终达到治疗肿瘤的目的。
关于关键性研究
阿帕替尼此次获批,是基于南京金陵医院秦叔逵教授牵头的AHELP研究。该研究由四川大学华西医院的李秋教授在2020年美国临床肿瘤学会(ASCO)年会上进行了口头报告。
该研究是一项随机、安慰剂对照、双盲、Ⅲ期研究,旨在评价以血管内皮生长因子受体2(VEGF-2)为靶点的抑制剂阿帕替尼治疗晚期肝癌的有效性和安全性。该研究纳入了中国31个地区的接受至少一种全身治疗(包括索拉非尼和奥沙利铂为主的化疗)的原发性肝癌患者,患者被随机分配(2:1)至阿帕替尼组或安慰剂组,主要研究终点是总生存(OS)。研究者分析了2014年4月1日至2017年5月3日纳入的393例患者(阿帕替尼组261例,安慰剂组132例)的数据。
研究显示,与安慰剂组相比,阿帕替尼组的中位OS显著延长(8.7个月 vs 6.8个月,HR=0.785,P=0.0476),中位无进展生存(PFS)延长(4.5个月 vs 1.9个月,HR=0.471,P<0.0001)。阿帕替尼组和安慰剂组客观反应率分别是10.7%(95% CI:7.2~15.1)和1.5%(95%CI:0.2~5.4)。
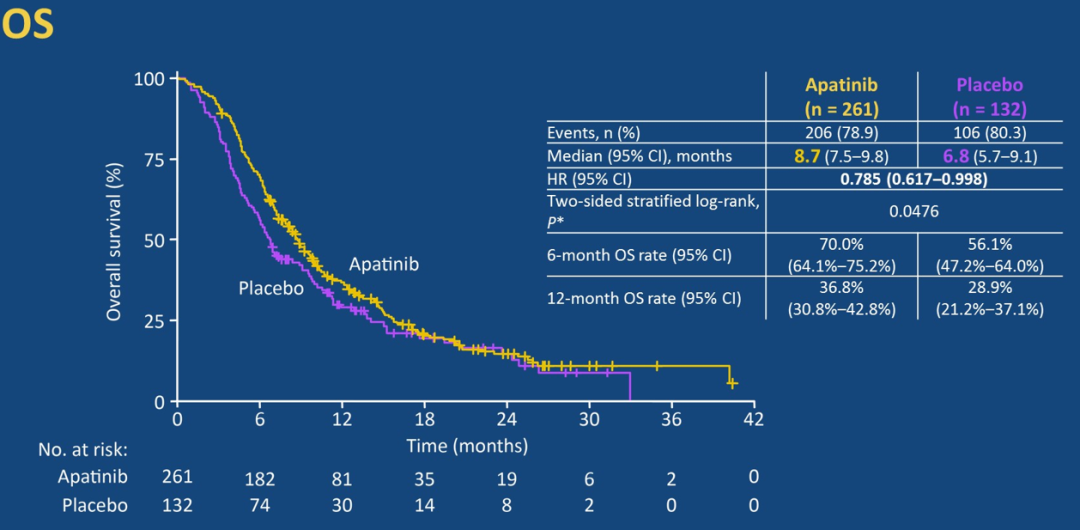
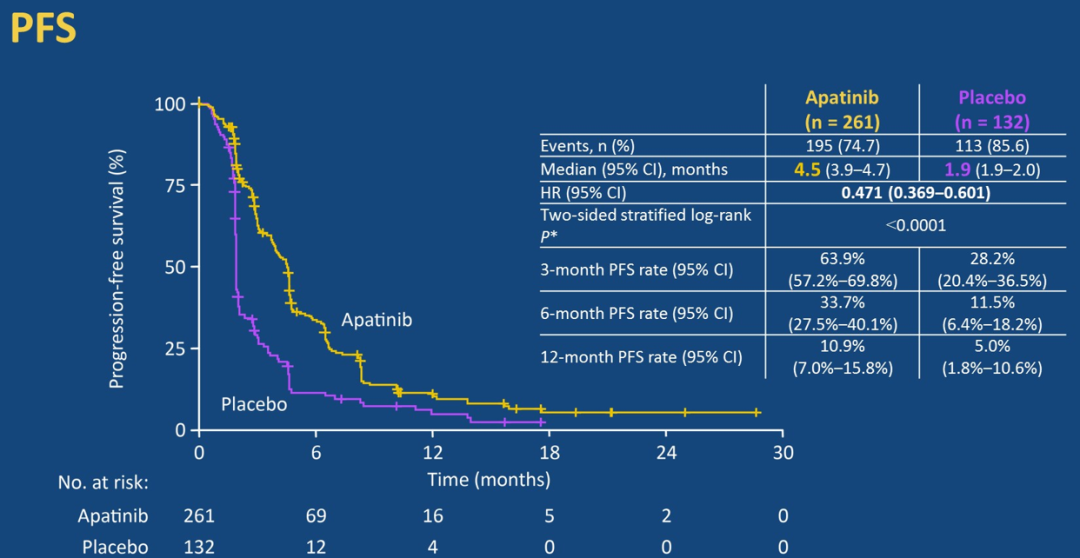
与安慰剂组相比,阿帕替尼组的中位OS和中位PFS显著延长
阿帕替尼组和安慰剂组分别有250例(97.3%)和92例(70.8%)患者出现治疗相关的不良事件(TRAEs)。3级和4级最常见TRAEs包括高血压[阿帕替尼组 71例(27.6%)vs 安慰剂组 3例(2.3%)]、手足综合征[46例(17.9%) vs 0例]、血小板减少[34例(13.2%) vs 1例(0.8%)]、中性粒细胞减少[27例(10.5%) vs 0例]。阿帕替尼组和安慰剂组分别有24例(9.3%)和13例(10.0%)患者死于不良事件,研究者认为与治疗无关。研究表明阿帕替尼能显著延长中国晚期肝癌患者的OS和PFS,且耐受性和安全性均较好。