免疫-靶向联合方案治疗肾癌数据更新 延长随访 风采依旧!
肾癌是泌尿系统肿瘤里比较常见的类型,这类肿瘤的治疗一直寻求突破,但长期以来都是多靶点抗血管生成的靶向药物互相PK,直到免疫治疗药物的出现,这个领域出现了新的面孔。
发布在柳叶刀杂志的一项研究报道了阿西替尼联合PD-1的K药与舒尼替尼的临床研究。终于将晚期肾癌的治疗掀开了新的一页。
研究背景
免疫检查点抑制剂的出现,给很多癌症的治疗带来了新的方向和思路。肾癌也是如此。
但目前晚期肾癌的一线治疗为多靶点抗血管生成药物舒尼替尼。为此将PD-1加上去之后情况会如何呢?
今天给大家分享的就是这样的一项研究。
KEYNOTE-426是一项大型的3期临床试验。该研究于2016年10月启动,在全世界16个国家共129个研究中心开展。研究总共纳入了861位先前未接受过治疗的肾透明细胞癌患者。
这些受试者随机分为两组,一组(432位患者)接收K药联合阿西替尼的治疗方案,每3周静脉滴注一次K药派姆单抗,每次200毫克,总共35个周期(约2年),同时每天口服两次阿西替尼,每次5毫克。
使用PD-1的K药出现毒性反应时,暂停使用,当不良事件降至1级或0级后可恢复K药使用;若是因为非不良事件相关的原因停用K药,比如需要进行手术,则应该在中断后3周内恢复使用。
服用阿西替尼时,在安全性达标的情况下,单次剂量而增加至7mg, 继而10mg;而当出现毒性反应时,单次剂量可降至3mg,继而2mg,2mg仍旧不耐受时,应永久性停用。
另一组患者(429例)接受单纯舒尼替尼治疗方案,每天口服一次,每次50毫克。每6周为1个周期,连用4周后,停用2周。
出现毒性反应时,单次用药剂量可减至37.5mg,继而25mg。主要终点是意向性治疗人群的总生存期OS和无进展生存期PFS。
治疗结果,K药联合阿西替尼优势明显
本次试验的中位随访时间是30.6个月。在总体生存率方面K药联合阿西替尼的治疗优势明显。

图1 两组患者的总生存期曲线
如上图所示,K药联合阿西替尼的总生存期曲线与舒尼替尼的明显拉开。两组患者的中位总生存期都没有达到。
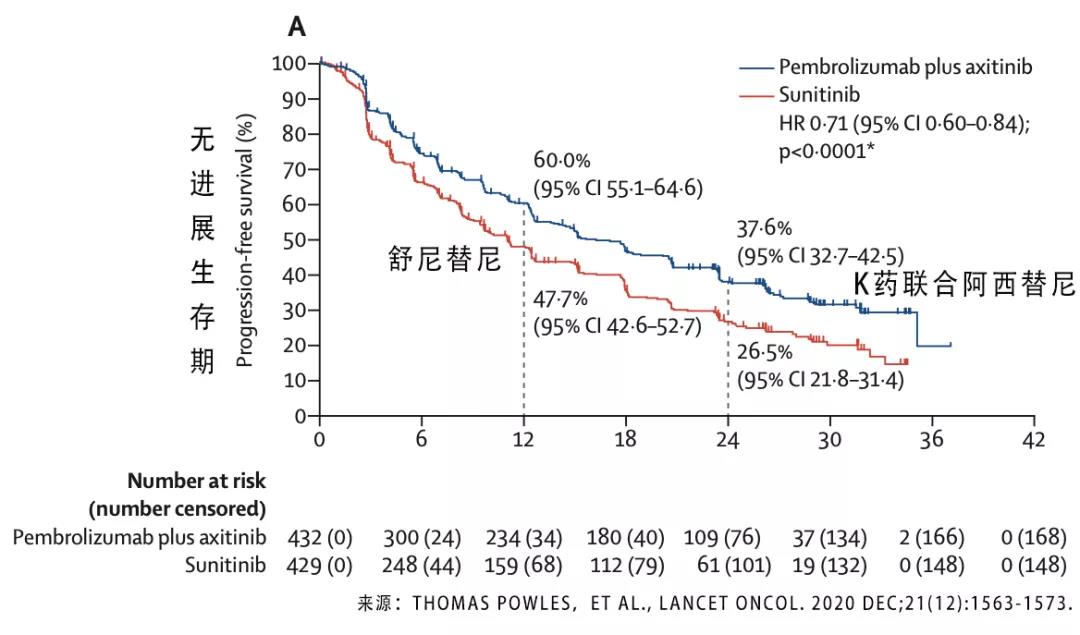
图2 两组患者的无进展生存期曲线
在无进展生存期方面,K药联合阿西替尼的中位PFS为15.4个月,而舒尼替尼单药的无进展生存期为11.1个月。
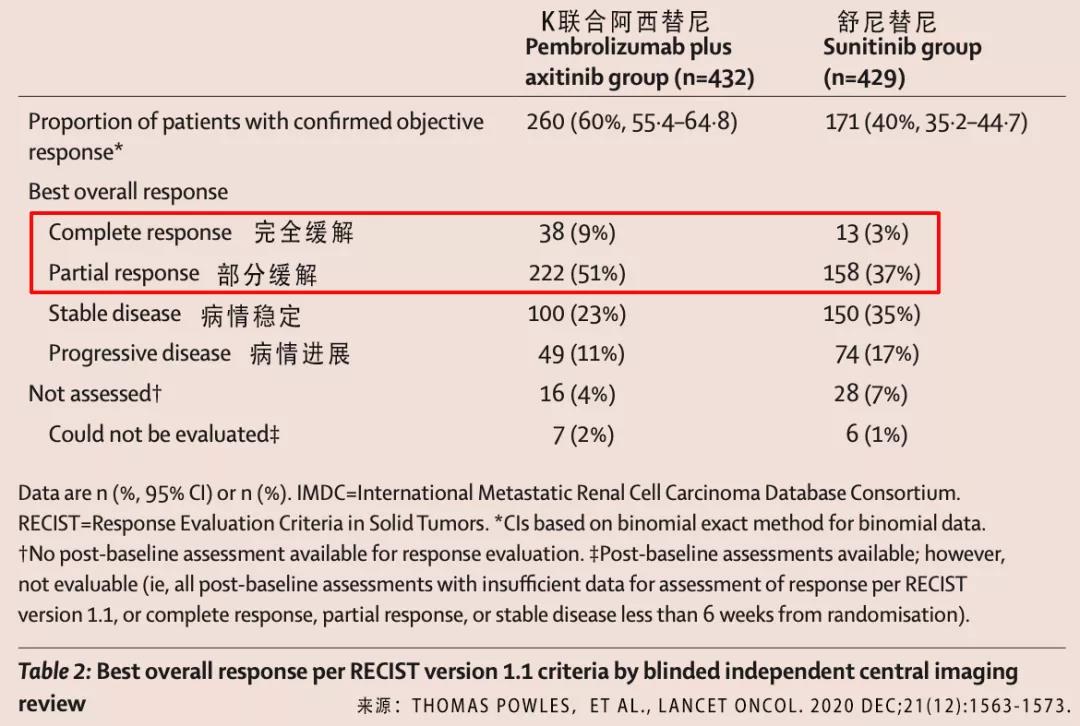
图3 两组患者的病情控制情况
此外,我们再看总具体的治疗应答率。我们看到临床完全缓解和部分缓解的比例,K药联合阿西替尼都比单独舒尼替尼要好。
从治疗不良事件来看。两组用药的患者最为常见的不良事件主要是高血压、腹泻等。总体可以耐受,并可控。
结语显
通过这一个研究可以看出,K药联合阿西替尼用于晚期肾癌应该是一个时间上的问题。这种用药组合以较低的不良反应发生概率,更好的治疗效果。有望可以给晚期肾癌患者带来更好的获益。
相信凭借这一数据,晚期肾癌有望在在一线使用PD-1,通过免疫治疗药物,抗血管生成的药物组合起来,如果再后面加上一些局部放疗,有可能给患者带来比较好的生存获益。
一旦发生了临床完全缓解、部分缓解的患者,则有可能会有一个非常长的生存期。当然具体的需要等后面的随访数据。
致敬,肿瘤治疗领域里的每一个突破和进步!
参考文献
1. Rini BI, Plimack ER, Stus V, et al. Pembrolizumab plus Axitinib versus Sunitinib for Advanced Renal-Cell Carcinoma. N Engl J Med. 2019 Mar 21;380(12):1116-1127. doi: 10.1056/NEJMoa1816714. Epub 2019 Feb 16.
2. Powles T, Plimack ER, Soulières, D, et al. Pembrolizumab plus axitinib versus sunitinib monotherapy as first-line treatment of advanced renal cell carcinoma(KEYNOTE-426): extended follow-up from a randomised, open-label, phase 3 trial [published online October 23, 2020]. Lancet Oncol. doi.org/10.1016/S1470-2045(20)30436-8.
3. Procopio G, Nichetti F, Verzoni E, et al. Pembrolizumab plus axitinib: another step ahead in advanced renal cell carcinoma [published online October 23, 2020]. Lancet Oncol. doi: 10.1016/S1470-2045(20)30482-4.