周彩存教授团队发表卡瑞利珠单抗联合阿帕替尼治疗晚期NSCLC II期试验结果;奥布替尼上市在即
要点提示
1.Lancet Gastroenterol Hepatol:加用FOLFIRINOX诱导化疗未改善术前白蛋白结合型紫杉醇+吉西他滨治疗胰腺癌的疗效
2.CCR:卡瑞利珠单抗联合阿帕替尼治疗晚期NSCLC有效且安全性好
3.CCR:转移性乳腺癌的疾病进展与其耐药性变化有关
4.新药:BTK抑制剂奥布替尼上市在即
01
Lancet Gastroenterol Hepatol:加用FOLFIRINOX诱导化疗未改善术前白蛋白结合型紫杉醇+吉西他滨治疗胰腺癌的疗效
12月15日,The Lancet Gastroenterology & Hepatology报道的NEOLAP-AIO-PAK-0113研究显示,作为局部晚期胰腺癌的多药诱导化疗方案,白蛋白结合型紫杉醇+吉西他滨与白蛋白结合型紫杉醇+吉西他滨序贯FOLFIRINOX的疗效及安全性相似。

局部晚期胰腺癌的最佳术前治疗尚不清楚。该项开放性、多中心、随机、Ⅱ期研究纳入ECOG评分为0或1、未经治疗的局部晚期胰腺癌(经组织学或细胞学确认)成人(18-75岁)患者,旨在比较白蛋白结合型紫杉醇+吉西他滨与白蛋白结合型紫杉醇+吉西他滨序贯FOLFIRINOX(氟尿嘧啶、亚叶酸、伊立替康和奥沙利铂)作为局部晚期胰腺癌多药诱导化疗方案的有效性和安全性。主要终点为手术转化率(surgical conversion rate)。
结果显示,130例患者随机分入白蛋白结合型紫杉醇+吉西他滨组(64例)或序贯FOLFIRINOX组(66例)。
白蛋白结合型紫杉醇+吉西他滨组和序贯FOLFIRINOX组的手术转化率分别为35.9%和43.9%(OR 0.72,95%CI 0.35-1.45;p=0.38),中位总生存(OS)分别为18.5个月和20.7个月(HR 0.86,95%CI 0.55-1.36;p=0.53)。
在诱导化疗期间,白蛋白结合型紫杉醇+吉西他滨组和序贯FOLFIRINOX组的3级或以上治疗中出现的不良事件(TEAE)发生率分别为55%和53%;未见治疗相关不良事件引起的死亡。
研究者表示,尽管大约三分之一的患者实现了肿瘤可切除性转化,但尚需其他证据来确定其是否可进一步转化为总生存的改善。
02
CCR:卡瑞利珠单抗联合阿帕替尼治疗晚期NSCLC有效且安全性好
12月15日,Clinical Cancer Research发布一篇临床试验结果,公布了卡瑞利珠单抗联合阿帕替尼治疗晚期非鳞状非小细胞肺癌(NSCLC)的生物标志物分析结果。研究表明,卡瑞利珠单抗联合阿帕替尼治疗肿瘤疗效显著且毒性可控。

该研究包含Ⅰb期和II期临床试验。自2017年3月起至2018年10月,105例接受过化疗预处理的NSCLC患者接受了阿帕替尼250mg(II期推荐剂量)和卡瑞利珠单抗治疗。
其中有1例(1.0%)完全缓解,28例(26.7%)部分缓解,48例(45.7%)病情稳定。在可评价疗效的人群中(n=94),客观缓解率(ORR)为30.9%(95%CI 21.7-41.2)。中位无进展生存期为5.7个月(95%CI 4.5-8.8),中位OS为15.5个月(95%CI,10.9-24.5)。
基于基因组信息,此联合治疗方案对所有PD-L1和肿瘤突变负荷(TMB)亚组都有效。其中,对于STK11/KEAP1基因突变来说,突变型和野生型患者的ORR分别为42.9%和28.1%,1年生存率分别为85.1%和53.1%。尚未观察到预料之外的不良事件。
研究者最终认为,卡瑞利珠单抗联合阿帕替尼治疗已经接受过化疗预处理的晚期NSCLC患者疗效显著且毒性可控。此外,研究还提示存在STK11/KEAP1基因突变的患者可能会从中获益更多,这一点将在III期试验中进行验证(NCT04203485)。
03
CCR:转移性乳腺癌的疾病进展与其耐药性变化有关
2020年12月15日,Clinical Cancer Research在线发表一篇关于循环肿瘤DNA(ctDNA)检测的回顾性队列研究,研究使用ctDNA来检测进展期转移性乳腺癌的耐药性变化。研究结果显示,通过连续ctDNA检测证实其耐药性改变确实与疾病进展有关。另外,研究者认为纵向ctDNA评估有望追踪肿瘤基因组的变化进展。

研究共纳入了86例正在进展期的转移性乳腺癌(MBC)患者,均采集了2次以上的连续ctDNA检测样本,所采集的样本统一使用Guardant360二代测序(NGS)技术进行了分析。第二次样本采集是基于首次样本进行了初步NGS分析,确定发生了进展(PN1)。其中有27例患者的二次NGS分析仍提示有临床进展(PN2),对其继续采集连续ctDNA样本。
根据ctDNA检测,研究分析了位点的变异情况、突变等位基因频率(MAF),变异位点的数量(NOA)以及病变部位的大致位点。另外,研究找了63例无进展的患者作为对照进行相同的检测。ctDNA检测结果显示,和对照组相比,进展组的MAF(p=0.0042)和NOA(p<0.0001)均较高。
研究者最终认为,转移性乳腺癌的进展或与耐药性改变及MAF和NOA升高有关。此外,纵向ctDNA评估有望追踪肿瘤基因组的变化进展。
04
新药:BTK抑制剂奥布替尼上市在即
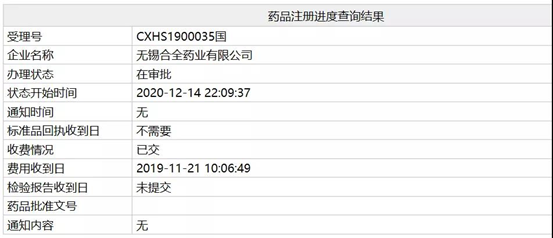
近日,诺诚健华奥布替尼片(orelabrutinib)在国内的注册申请进入“在审批”阶段,有望于近期获得批准,用于单药治疗既往至少接受过一种治疗的慢性淋巴细胞白血病/小淋巴细胞淋巴瘤(CLL/SLL)以及既往至少接受过一种治疗的套细胞淋巴瘤(MCL),成为继伊布替尼、泽布替尼后国内第三个上市的BTK抑制剂。
参考资料:
[1]Kunzmann Volker,Siveke JT,Algül H,et al.Nab-paclitaxel plus gemcitabine versus nab-paclitaxel plus gemcitabine followed by FOLFIRINOX induction chemotherapy in locally advanced pancreatic cancer(NEOLAP-AIO-PAK-0113):a multicentre,randomised,phase 2 trial[J].Lancet Gastroenterol Hepatol.Published:December 15,2020.
DOI:https://doi.org/10.1016/S2468-1253(20)30330-7
[2]Caicun Zhou,Yina Wang,Jun Zhao,Gongyan Chen,Zhihua Liu,Kangsheng Gu,Meijuan Huang,Jianxing He,Jianhua Chen,Zhiyong Ma,Jifeng Feng,Jianhua Shi,Xinmin Yu,Ying Cheng,Yu Yao,Yuan Chen,Renhua Guo,Xiaoyan Lin,Zhe-Hai Wang,Guanghui Gao,Quan Ren Wang,Weixia Li,Xinfeng Yang,Lihong Wu,Jun Zhang and shengxiang ren.Efficacy and biomarker analysis of camrelizumab in combination with apatinib in patients with advanced non-squamous NSCLC previously treated with chemotherapy.Clin Cancer Res December 15 2020.
DOI:10.1158/1078-0432.CCR-20-3136
[3]Saya Jacob,Andrew A.Davis,Lorenzo Gerratana,Marko Velimirovic,Ami N Shah,Firas Wehbe,Neelima Katam,Qiang Zhang,Lisa Flaum,Kalliopi P Siziopikou,Leonidas C.Platanias,William Gradishar,Amir Behdad,Aditya Bardia and Massimo Cristofanilli.The use of serial circulating tumor DNA(ctDNA)to detect resistance alterations in progressive metastatic breast cancer.Clin Cancer Res December 15 2020.DOI:10.1158/1078-0432.CCR-20-1566
[4]https://mp.weixin.qq.com/s/CqDDTw3rPTsMrK6kZ5YNhA