60%以上的乳腺癌 一线治疗这样用药生存期更长
中国女性健康的“头号致命物”——乳腺癌的发病率正以每年4%的速度递增。激素受体阳性(HR+)/HER2阴性(HER-)是最常见的转移性乳腺癌亚型,约占所有转移性乳腺癌的65%。
相较于其他亚型乳腺癌,HR+/HER2-预后较好,长期辅助内分泌治疗已经让更多患者实现长期“带瘤生存”。
内分泌治疗主要通过抑制雌激素生成,阻断雌激素与肿瘤细胞结合来发挥抗肿瘤作用。
在确诊为乳腺癌后,首先要进行分子分型,即检测ER、PR和HER2这三个指标,如果ER或PR是阳性,可以使用内分泌治疗。
根据NCCN和CSCO乳腺癌诊治指南,内分泌治疗已经成为绝经前和绝经后HR+/HER2- 转移性乳腺癌患者的优选策略。
近年来,一些创新治疗方案,如内分泌联合CDK4/6抑制剂、mTOR抑制剂和PI3K抑制剂等,显著改善了这类患者的预后。
鉴于此,内分泌为基础的序贯方案得到了国际指南推荐。然而,在真实世界的临床实践中,化疗和内分泌治疗仍然是乳腺癌基本的治疗方法。
化疗为基础的方案仍广泛用于一线治疗,尤其是侵袭性肿瘤和负荷较高肿瘤。
这可能是因为既往缺少对HR+/HER2-乳腺腺癌患者内分泌治疗和化疗疗效的直接比较数据。
数据来了!一项大型回顾性分析数据比较了真实世界中HR+/HER2- 转移性乳腺癌患者一线内分泌治疗与化疗的疗效。
研究证实了与单独化疗方案相比,内分泌治疗和化疗序贯内分泌治疗显示出更好的中位PFS的临床获益。
该研究收录了2000年1月1日至2018年12月30日期间共416例就诊于辽宁省肿瘤医院/研究所的HR+/HER2- 转移性乳腺癌患者。
研究将患者分为3组:单纯内分泌治疗组(n=248)、单纯化疗组(n=94)和化疗序贯内分泌治疗组(n=74)。主要终点是无进展生存期(PFS)(图1)
· 化疗组:卡培他滨、多西他赛、吉西他滨、紫杉醇、白蛋白紫杉醇单药,或紫杉醇/多西他赛/吉西他滨联合卡培他滨、紫杉醇/多西他赛联合蒽环类药物.
· 内分泌治疗方案包括:来曲唑,阿那曲唑,依西美坦,氟维司群,他莫昔芬,来曲唑联合派柏西利。

图1 研究设计
研究结果
主要研究终点中位PFS:单纯内分泌治疗组为13.9个月;化疗序贯内分泌治疗为14.2个月;而单纯化疗组的中位PFS仅为8.1个月。

图2 研究主要终点PFS对比
数据解读:在主要研究终点PFS方面,相比于单纯化疗的治疗方案,单纯内分泌治疗组和化疗序贯内分泌治疗组PFS显著提高了5个多月。
这一数据说明了内分泌治疗的显著优势,而内分泌序贯化疗的治疗方案似乎能达到更加的临床获益。
亚组分析结果
患者绝经状态 (图3)
· 绝经后患者中位PFS:单纯内分泌治疗15.1个月;化疗序贯内分泌治疗13.6个月;均优于单纯化疗8.0个月。
· 绝经前患者中位PFS:化疗序贯内分泌治疗16.6个月显著优于单纯内分泌治疗10.1个月和单纯化疗9.1个月。

图3 患者绝经状态亚组中位PFS
数据解读:研究纳入的患者中,约70%的患者处于绝经后状态(单纯内分泌治疗组为76.6%,单纯化疗组为75.5%,vs. 化疗序贯内分泌治疗组为68.9%)。因此,绝经后状态患者的中位PFS对最终结果更具意义,充分显示内分泌治疗及序贯治疗的显著疗效。
肺转移亚组(图4)
· 肺转移组中位PFS:内分泌组13.1个月、化疗序贯内分泌组15.4个月显著优于化疗组6.9个月。
· 非肺转移组中位PFS:内分泌组14.4个月、化疗序贯内分泌组13.7个月同样显著优于化疗组8.7个月。

图4 肺转移亚组中位PFS
肝转移亚组(图5)
肝转移组中位PFS,三组间中位PFS均无统计学意义。
非肝转移组中位PFS:内分泌组15.2个月和化疗序贯内分泌组14.2个月均显著优于化疗组8.1个月。
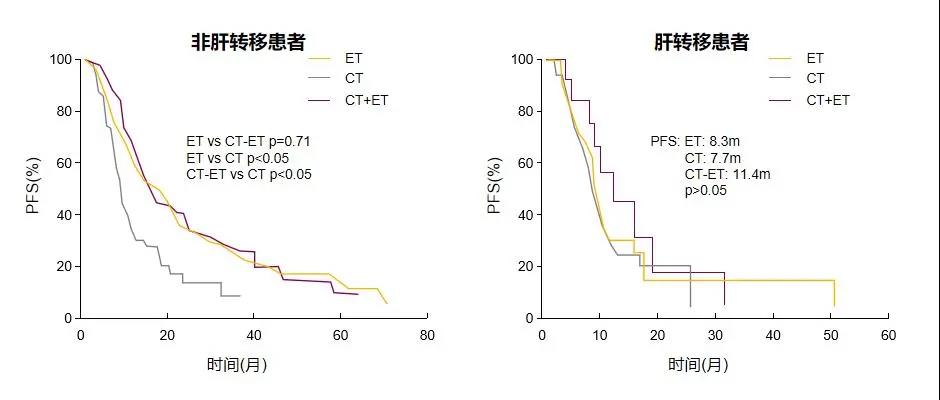
图5 肝转移亚组中位PFS
数据解读:肺转移和肝转移亚组分析中,存在统计学意义的研究结果均显示内分泌治疗和序贯治疗方案均显著优于单纯化疗。
这显示出,无论患者是否存在肺转移和肝转移,相比内分泌治疗和序贯治疗,单纯化疗治疗方案都是欠佳的。
安全性分析
在临床中,治疗方案的安全性尤为重要。与单纯内分泌治疗相比,3/4级血液学毒性在单纯化疗和序贯治疗中更为常见,应用化疗方案的患者耐受性更差一些。
小结:这项全面的回顾性分析清晰的展示了化疗和内分泌治疗对HR+/HER2-转移性乳腺癌患者疗效。
结果很明显,无论是整体的PFS还是绝经状态、肺转移和肝转移亚组分析,相比于单纯化疗作为一线治疗的方案,内分泌治疗和化疗序贯内分泌治疗能够显示出更佳的临床获益。
这一分析结果将为激素受体阳性转移性乳腺癌患者一线治疗的最佳方案选择提供更多指导证据。
声明:本资料中所涉及的信息仅供参考,请遵循医生或其他医疗卫生专业人士的
参考文献
[1]Junnnan Xu and Tao Sun.Retrospective analysis of first-line progression free survival compared endocrine therapy and chemotherapy inpatients with HR+/HER2-metastatic breast cancer. 2019 San Antonio Breast Cancer Symposium; December 10-14, 2019.