少见突变晚期NSCLC接受免疫治疗的疗效和安全性如何?
非小细胞肺癌(NSCLC)的管理依赖于组织学亚型和分子分型,在Ⅳ期肺腺癌中通常会评估患者是否存在驱动基因改变,例如EGFR、ALK、ROS1、BRAF、MET、HER2等靶点的改变,对于符合条件的患者给予靶向药物治疗。近年来以PD-1/PD-L1单抗为代表的免疫治疗发展迅速,已经改写了驱动基因阴性,尤其是EGFR、ALK阴性晚期NSCLC的治疗模式,为患者带来了更好的生存获益。对于BRAF、HER2、MET、RET等少见靶点,此类患者接受免疫治疗的疗效和安全性尚不明确。为此,来自法国的专家学者开展了名为IMAD2的研究,探索了BRAF、HER2、MET突变或RET重排晚期NSCLC接受免疫治疗的疗效和安全性。
IMAD2(GFPC 01-2018)研究是由法国肺癌组织(GFPC)开展的一项回顾性多中心研究,研究的主要目标是评估BRAF、HER2、MET突变或RET重排晚期NSCLC接受免疫治疗的疗效,包括客观缓解率(ORR),缓解持续时间(DOR)、无进展生存期(PFS)和总生存期(OS),次要目标是安全性。
研究共纳入来自法国21个中心的107例患者,患者基线情况:37%从不吸烟;54%为男性;93%为腺癌;44例患者伴有BRAF突变(V600突变26例),23例患者伴有HER2突变,30例患者伴有MET突变,9例患者有RET重排;45例(42%)患者的PD-L1表达水平已知,其中11例PD-L1阴性,34例PD-L1表达阳性,包括25例PD-L1≥50%的患者;在接受免疫治疗前,所有患者的中位治疗线数为1。

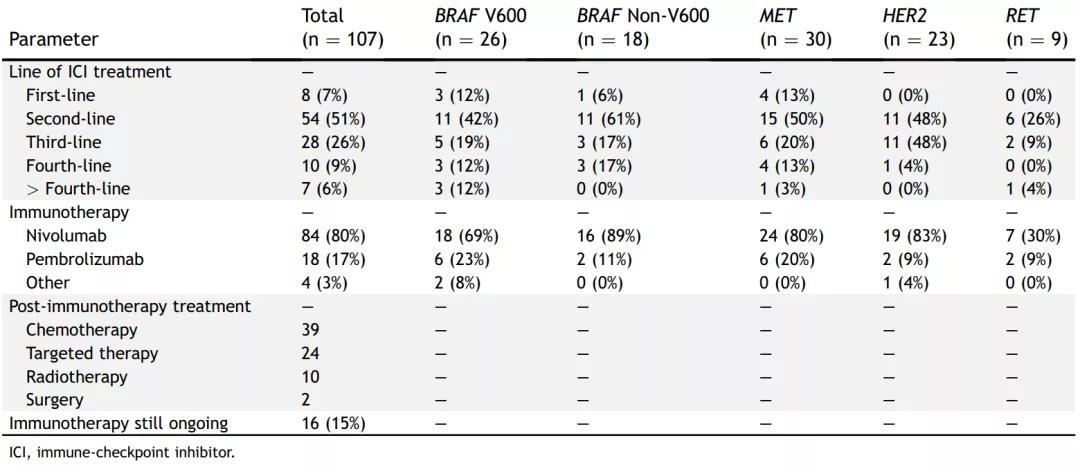
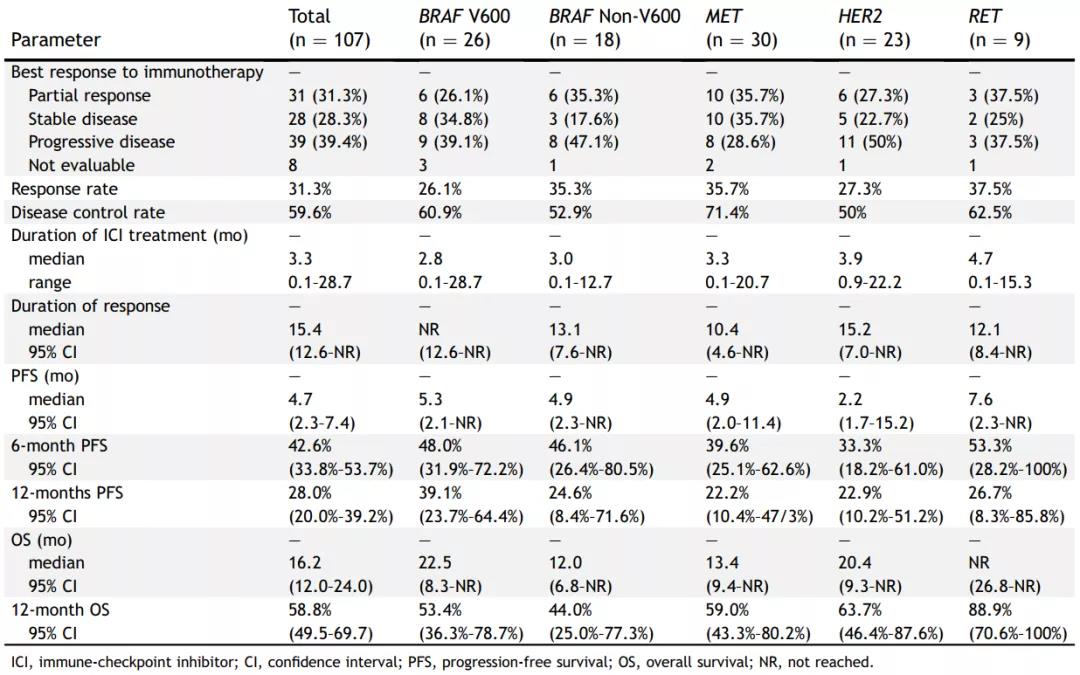
在全体人群中,患者接受免疫治疗的中位DOR为15.4个月,中位PFS为4.7个月,中位OS为16.2个月。根据分子分型,BRAF-V600突变、BRAF非V600突变、HER2突变、MET突变、RET重排NSCLC接受免疫治疗的ORR分别为26%、35%、27%、36%和38%。其他详细数据见下表。
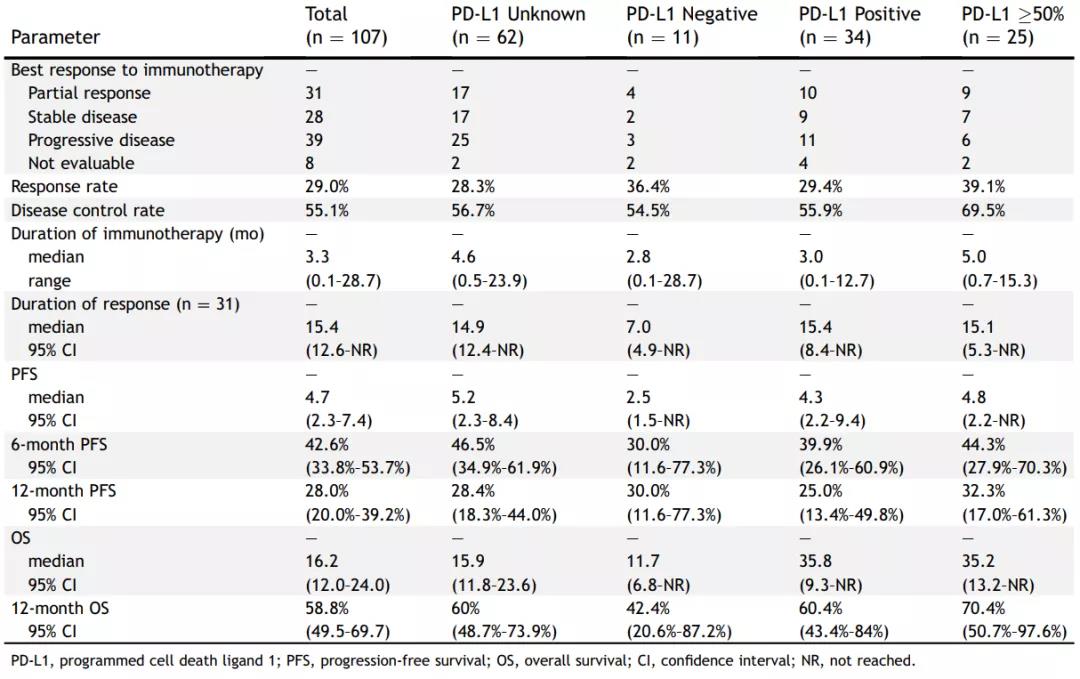
根据患者的PD-L1表达情况进行分析,PD-L1表达阴性患者的中位PFS和中位OS分别为3.0个月和11.7个月;PD-L1表达阳性患者的中位PFS和中位OS分别为4.3个月和35.8个月。
安全性方面,28例(26%)患者报道了不良事件,其中11例(10%)出现了3~5级免疫介导的不良事件(结肠炎5例;肺炎2例;垂体炎、肾炎、肝炎和贫血各1例)。
本项来自真实世界的回顾性多中心研究结果表明,BRAF、HER2、MET突变或RET重排NSCLC患者接受免疫治疗的疗效与既往随机对照临床试验中未经选择的NSCLC患者接受免疫治疗的疗效相似,未来需要进行大规模的前瞻性研究来明确在此部分少见突变人群中应用免疫治疗。
参考文献
Guisier F,Dubos-Arvis C,Viñas F,et al.Efficacy and Safety of Anti-PD-1 Immunotherapy in Patients With Advanced NSCLC With BRAF,HER2,or MET Mutations or RET Translocation:GFPC 01-2018[J].J Thorac Oncol,2020,15(4):628-636.