打破价格高 耗时长等种种局限 黄河教授 经济适用型 CAR-T再证安全有效
近年来,嵌合抗原受体T细胞CAR-T(Chimeric Antigen Receptor T-Cell)免疫疗法在获得长足发展的同时,CAR-T细胞治疗在B细胞血液系统肿瘤中已经显现出可观疗效。但当下,研究成果如何应用于临床实际为患者生存及预后带来获益?这是摆在研究者和血液医生面前的一道棘手难题。
目前,自体CAR-T细胞疗法的临床应用仍面临着诸多挑战。一方面,由于自体CAR-T细胞制备时间长、成本高,还可能存在制备失败的风险从而影响了应用可及性;另一方面,单靶点CAR-T细胞治疗中抗原丢失/下调可能导致治疗失败。那么,如何克服这些阻碍,解决应用难题?为此,医学界特邀浙江大学医学院附属第一医院黄河教授与大家一起深度探讨CAR-T细胞治疗的应用未来。
扫描二维码,听黄河教授,讲观点争锋!

CAR-T应用困难重重,血液医生如何破局?
2020年12月6日(太平洋时间),黄河教授在美国血液学会年会(ASH 2020)中发表了关于一项CRISPR/Cas9工程改造的通用CAR-T细胞产品(CTA101)用于复发/难治性B细胞急性淋巴细胞白血病(ALL)的安全性和有效性的口头报告。

图1会议现场
“
“通用型CAR-T意味着即时可用。对于具有适应证的患者,通用型CAR-T细胞产品如同‘药品’一样随取随用。经量产化的通用型CAR-T产品不仅降低了成本,也降低了患者接受CAR-T治疗的‘门槛’,能惠及更多患者。基于现阶段CAR-T治疗中诸多未被满足的临床需求,通用型的CAR-T或将成为今后发展的重要方向。”黄河教授告诉医学界。
”
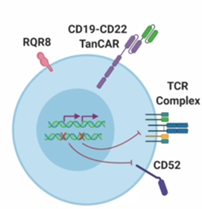
图2 CTA101设计
基于CD19和CD22在ALL中的高表达,黄河教授团队设计了双靶点通用型CAR-T细胞产品:通过CRISPR/Cas9技术敲除了TRAC和CD52基因从而降低宿主介导的免疫排斥,并利用二代慢病毒转导进行CD19/CD22 CAR-T细胞制备,同时还为其装上了一个自杀基因。

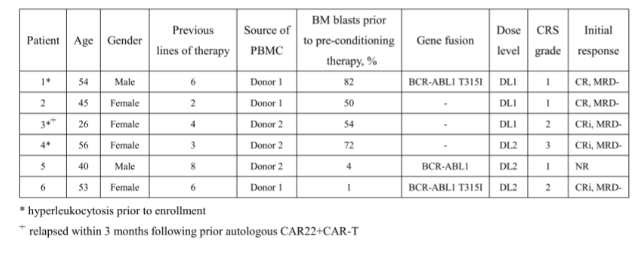
在本次研究中,接受CTA101治疗的患者均未发生剂量限制反应(DLTs)移植物抗宿主反应(GvHD)、免疫效应细胞相关神经毒性综合征(ICANS)及死亡及其他四级不良事件(AE),而与治疗相关的细胞因子风暴(CRS)经单次妥珠单抗(tocilizumab)和糖皮质激素治疗后在一周内顺利恢复。
表1患者特征及疗效

从概念到临床,从第一步到下一步
考虑到通用型CAR-T细胞疗法的优势一定程度上弥补了自体CAR-T细胞产品的诸多不足。近年来,中美国家关于通用型CAR-T产品的临床研究结果相继在国际大会上报道,而产品的临床可行性和可及性是大家始终关注的焦点。
“
“通用型CAR-T从概念设想到临床探索,我们已经迈出了第一步。从现在获得的临床数据来看,我们证实了通用型CAR-T的可行性,接下来,我们需要不断优化方案,提升治疗效果。”黄河教授补充道,“在通用型CAR-T的治疗应用中,预处理是我们首先面对的一大难题,预处理方案太弱会导致CAR-T细胞被排斥。使用CD52单克隆抗体进行预处理能够更好地避免GVDH,但同时也导致了机体免疫抑制的发生。如何权衡和调整预处理方案仍需我们进一步探讨。如何制定无需使用CD52单抗的预处理方案?如何设计出可及性更强的CAR-T新产品?这将是大家探索的方向。我相信,在不久的将来,通用型的CAR-T细胞产品将克服应用难题,真正走进临床实践,改善ALL患者预后,提升治疗疗效。”
”
克服靶点逃逸,双靶、多靶成为治疗更优选
一项新型治疗手段的诞生,眼下的疗效固然重要,但从临床实际应用考虑,如何维持长期疗效是临床医生与研究人员更为关注的焦点。靶点逃逸作为影响CAR-T治疗长期疗效的一大挑战,往往也是困扰研究者们的难题。如何解决CAR-T治疗靶点逃逸问题,提高疗效、降低疾病复发是值得我们深入思考的问题。

终极治疗or桥接治疗?仍需因“病”制宜
随着CAR-T逐渐成为万众瞩目的治疗热点,关于CAR-T在治疗中的地位一直是具有争议的话题。到底CAR-T细胞治疗未来将成为终极手段还是桥接治疗选择,目前尚未有定论。
“
对此,黄河教授告诉医学界:“CAR-T细胞治疗在不同的疾病的疗效有所差异,在ALL中CAR-T治疗缓解率可高达90%以上,但遗憾的是半数患者后续出现复发;而在淋巴瘤患者中,尽管CAR-T治疗效果并不如在ALL中显著,但淋巴瘤经CAR-T治疗后复发率相对较低。因此,对于不同疾病,我们应采取不同CAR-T治疗策略,结合实际情况来选择序贯治疗还是与小分子化合物联合来维持CAR-T细胞在血液中的数量和活性。CAR-T疗法桥接造血干细胞移植也是可行的选择,但对于本身CAR-T治疗后复发较低的疾病类型,我们不必选择桥接移植。对于ALL患者的CAR-T治疗,根据我们开展的全国多中心的临床研究结果,患者在接受CAR-T细胞治疗达MRD阴性后桥接半相合造血干细胞移植可以取得最好的疗效,两年的生存达70%;相比之下,未接受移植的患者生存仅为30%。因此,我们建议高危ALL患者,在接受CAR-T治疗达MRD阴性后可桥接半相合的造血干细胞移植。”
“当然,随着医疗的发展与进步,未来也可能诞生更优效的治疗选择,比如CAR-T的序贯治疗或者小分子靶向药物的桥接来改善疾病的预后,延长患者的生存。”黄河教授进一步补充道。
”
CAR-T大潮席卷全球,中国研究如何实现异军突起?
新药时代来临,CAR-T研究成为国内外备受瞩目的研究热点,在今年ASH大会中,我国入选的研究有很大一部分与CAR-T治疗相关,中国研究如何在CAR-T研究“量产化”时代中实现“异军突起”?

