细胞免疫疗法:盛名之下,其实难副?
细胞免疫疗法的投资并购火热
近几年,细胞免疫疗法凭借新颖的科学理论和治疗癌症患者的显著疗效,频频占据新闻头条。细胞免疫疗法以其魅力掀起了医疗领域的一场革命,不仅给患者带来了潜在的巨大临床治疗价值,而且提升了人们对疾病治疗方式的认知。从事细胞免疫疗法研发的生物技术公司如雨后春笋般涌现,数以亿计的资本蜂拥而至,在全球范围内广泛投资,期待产生显著的临床和商业获益(图表1)。
图表1. 2019年细胞治疗领域全球top10投资
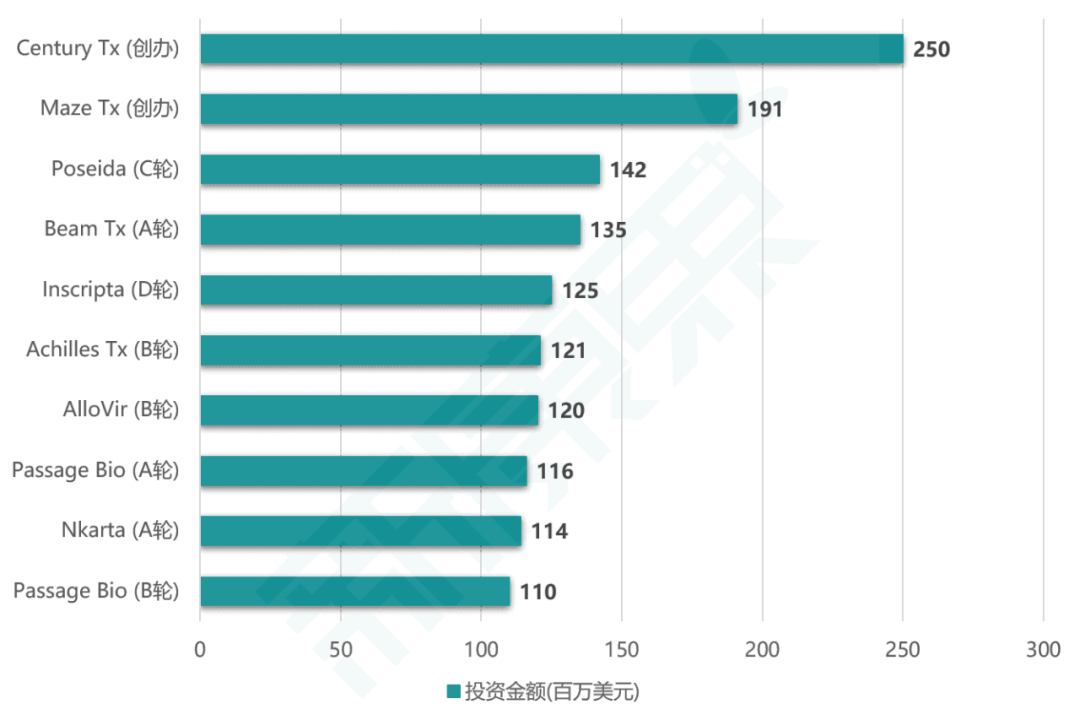
全球头部大型制药公司中,有许多都在细胞免疫疗法上押下重注。2017年8月,吉利德(Gilead)以119亿美元收购Kite Pharma(凯特)。2018年1月,新基(Celgene)以90亿美元收购了Juno Therapeutics(巨诺)。这两笔高值交易有力地体现了细胞疗法在临床疗效和改善现有治疗模式方面所受到的认可。
国外细胞免疫疗法研发概况
细胞免疫疗法(cell immunotherapy),或者说免疫细胞疗法(immune cell therapy),其基本过程为采集人体免疫细胞,体外激活以增强靶向杀伤能力,扩增后回输人体,通过调动人体免疫系统杀伤血液和组织中的癌细胞、病原体和突变细胞等(图表2)。
图表2. 细胞免疫疗法的基本过程示意

细胞免疫疗法经历了较长的发展历程,早在1982年,美国医生Grimm等在外周血单核细胞中,加入IL-2体外培养,诱导出LAK(淋巴因子激活杀伤细胞),可以杀伤对CTL(细胞毒性T淋巴细胞)、NK(自然杀伤细胞)不敏感的癌细胞。此后,TIL(肿瘤浸润淋巴细胞)、CIK(细胞因子诱导杀伤细胞)、CAR-T(抗原嵌合受体T细胞)被陆续发现。目前,细胞免疫疗法可分为非特异性和特异性两大类(图表3)。
图表3. 细胞免疫疗法主要分类
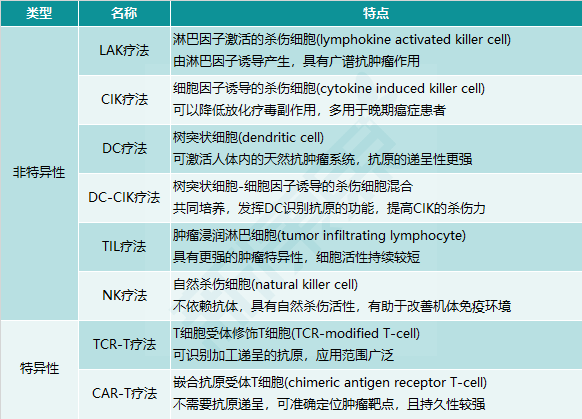
CAR-T疗法,作为最新一代的细胞免疫疗法,近几年在临床上得到了概念确证,商业价值正在显现。2017年8月,诺华上市Kymriah,用于治疗急性淋巴细胞白血病(ALL)。同年10月,吉利德旗下的KitePharma上市Yescarta,用于治疗复发或难治性大B细胞淋巴瘤。2020年7月,Kite Pharma的Tecartus获得FDA批准,用于治疗复发或难治性套细胞淋巴瘤(MCL)(图表4)。
图表4. 目前全球已获批上市的3款CAR-T产品概况(2020.11.11)
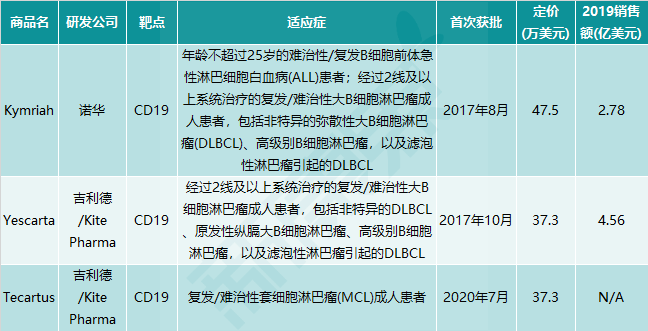
除了以上3款产品,还有多款细胞免疫疗法项目处于研发后期,即将上市。随着更多细胞免疫疗法产品的上市,很可能将极大地改变多种肿瘤的治疗标准(图表5)。
图表5. 国外处于研发后期的细胞免疫疗法
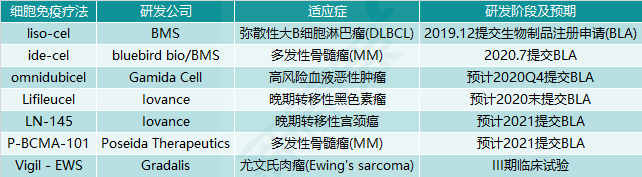
国内细胞免疫疗法研发概况
得益于政府政策扶持,在VC/PE投资的支持下,中国的细胞疗法研发欣欣向荣,大有赶超国际先进水平的趋势。2017年12月和2018年1月,先后有4款CAR-T疗法的临床试验申请(IND)被纳入优先审评,包括:传奇生物BCMA靶向CAR-T疗法LCAR-B38M、科济生物的GPC-3靶向CAR-T、北京马力诺的CD19靶向CAR-T,以及上海恒润达的CD19靶向CAR-T。传奇生物的LCAR-B38M在2019年12月被美国FDA 授予突破性疗法认定之后,又在2020年8月成为中国首个被拟纳入突破性治疗药物审评工作程序的品种。目前,中国发起的CAR-T临床试验数量已经超越美日欧成熟医药市场,居于全球首位(图表6)。
图表6. 全球细胞和基因疗法临床试验开展情况(截至2020.2.18)
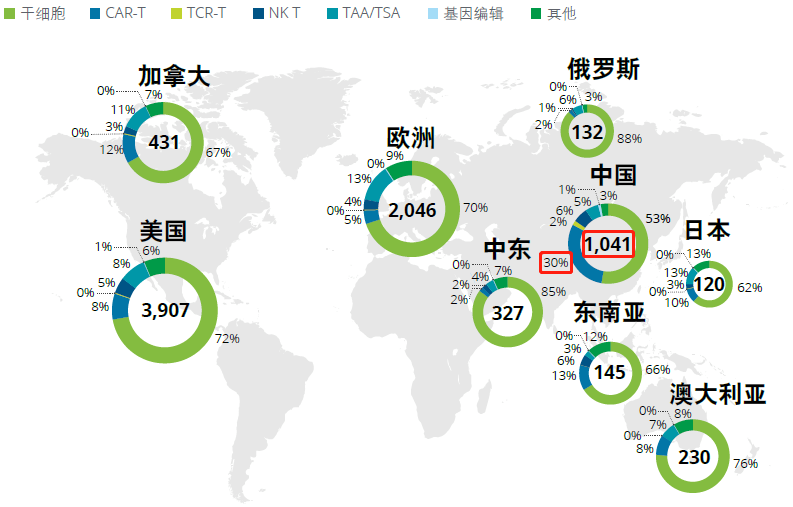
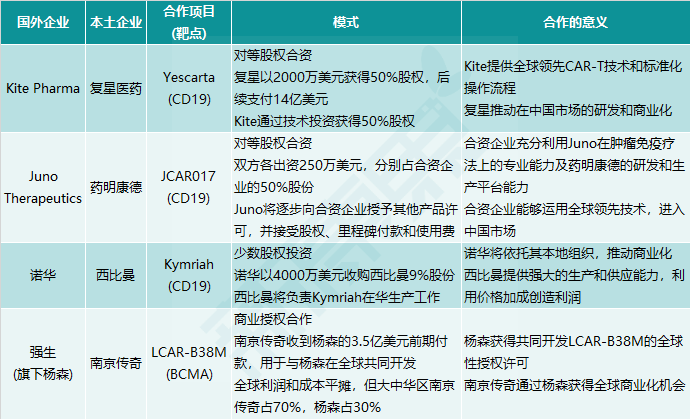
在中国市场上,除了本土生物技术公司积极进行细胞免疫疗法研发,国外企业也在加快与本土企业合作,通过合资企业、授权许可开展合作,从而获取本地化的研发、生产和商业化能力,加快产品上市速度。这种合作包括复星医药和Kite Pharma(凯特)、药明康德和Juno Therapeutics(巨诺),以及西比曼和诺华(Novartis)。南京传奇生物和强生(旗下杨森)的合作则是侧重于本土创新技术的向外授权,借助强生遍布全球的资源,实现全球商业化(图表7)。2020年3月,复星凯特的益基利仑赛注射液(即Yescarta)的中国上市申请被纳入优先审评。2020年9月,药明巨诺的CD19靶向CAR-T瑞基仑赛注射液(基于JCAR017研发的JWCAR029)被纳入突破性治疗品种,其中国上市申请被纳入优先审评。
图表7. 国外企业和本土企业关于细胞疗法的合作
叫好不叫座?
虽然细胞免疫疗法在全球掀起了研发热潮,并且得到了大量资本的青睐,但是目前已经上市的CAR-T疗法产品的销售额却差强人意。2017年上市的Kymriah和Yescarta在2019年的全球销售额分别为2.78亿美元和4.56亿美元,低于业界预期,与重磅炸弹级别产品尚有不小的差距(上文图表4)。
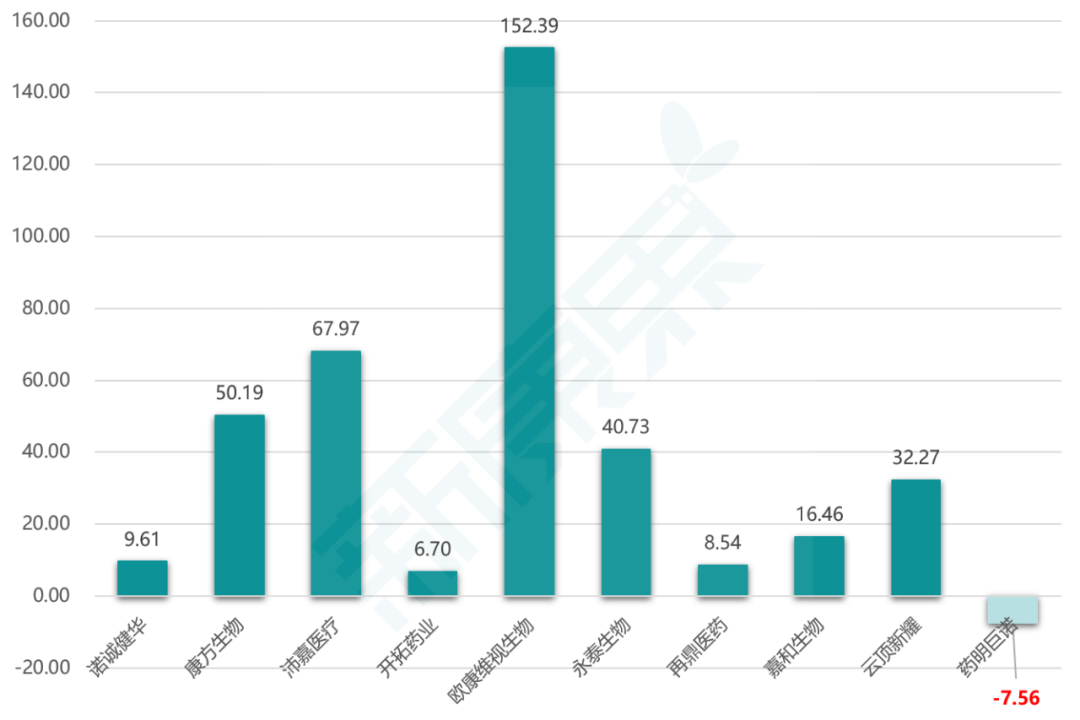
2020年11月3日,药明康德与JunoTherapeutics对等股权投资创办的药明巨诺(JW Therapeutics)在港交所挂牌上市,发行价每股23.8港元,当日以22.00港元收盘,较发行价下跌7.56%。截至目前,在2020年10家登陆港股的未盈利医药企业,仅有药明巨诺在上市首日破发(图表8)。
图表8. 2020年港股上市未盈利医药企业上市首日涨跌幅
药明巨诺反常的破发,是否表示资本市场对于细胞免疫疗法看法的转变?细胞免疫疗法是否从叫好不叫座变成了既不叫好也不叫座?细胞免疫疗法存在哪些问题,未来又会怎样?
困扰的安全性问题
CAR-T疗法的传奇始于成功治愈美国女孩艾米丽(Emily Whitehead)。2010年,5岁的艾米莉被诊断患有急性淋巴细胞白血病(ALL),随后经历了三轮化疗和两次复发。2012年4月,艾米莉加入了诺华关于CTL019(即后来的Kymriah)的临床I期试验,成为第一位接受CAR-T疗法的儿童患者。在接受治疗3周后,艾米莉的病情就得到了缓解,3个月后就已经检测不到癌细胞。此后每年检测一次,直到2020年5月仍未有复发迹象,可以认为达到了临床治愈。
成功治愈白血病给细胞免疫疗法带来了无数赞誉,但是截至目前,全球范围内公开报道的治愈病例仍然比较有限。此外,公众只注意到CTL019治愈了艾米丽,却忽视了治疗过程中的不良反应。艾米丽在接受CTL019注射后,迅速发烧,血压骤降,重度昏迷,在重症监护室使用呼吸机两周,最终通过使用IL-6抑制剂托珠单抗(tocilizumab)获得了好转。
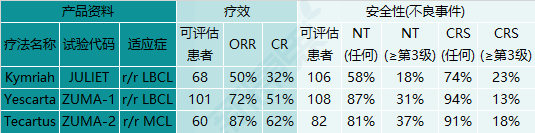
安全性问题一直困扰着细胞免疫疗法的研发和商业化。2016年,美国3名复发/难治性ALL患者在JunoTherapeutics(巨诺)关于JCAR015的II期临床试验中死亡,促使美国FDA发布了有关细胞和基因疗法产品开发和审批流程的5项综合性法规。此外,Kite Pharma的KTE-C19(即2020年获批的Tecartus)和Cellectis的UCART123都出现过患者在治疗过程中死亡的事件。目前已获批的3款CAR-T疗法在临床试验中显示了突出的疗效,但是安全性问题也比较突出(图表9)。这3款疗法的标签中都被FDA加上了黑框警告,包括细胞因子释放综合征(CRS)和神经毒性(NT),此外不良反应还有过敏反应、严重感染、延长的血细胞减少、丙球蛋白减少、继发性恶性肿瘤,以及影响驾驶和操作机器。
图表9. 获批的CAR-T疗法的疗效和安全性
制造和应用中的问题
细胞免疫疗法制造和应用过程复杂,全程需要在无菌、无毒素、无偶然污染的环境下进行,细胞的提取、分离、诱导、扩增和回输等一系列流程需要在较短时间内完成,对技术人员要求高,对存储和转移的要求严格。然而,现有质量管控多来自企业或机构,缺乏通用的管理标准。
CAR-T疗法主要涉及基因工程载体的构建和CAR-T细胞制备,但是多数企业没有成熟的工艺及质量研究平台,载体的供应成为制造环节的关键挑战。病毒载体具有高度多样性和复杂性,需要数年才能构建相关的专业知识体系,而且规模化制造非常耗时,这可能是细胞免疫疗法产品规模化快速供应的瓶颈。
细胞免疫疗法与传统药物的主要区别的一个方面是,应用场景必须是医院,而且医院需要做好充足的准备。生物制药公司需要深入评估有意使用细胞疗法的医院的现有能力,通过多种渠道(当面、线上等)提供适当的资源和培训,使患者顺利度过复杂的治疗旅程。这个治疗旅程包括收集和运送患者的细胞到生物制药公司,跟踪制造过程,接收、储存和应用治疗,最后为患者提供监测。生物制药公司或者供应商应当与尽量多的医院建立合作,从而获取更多的患者资源。
高昂的价格
围绕细胞免疫疗法的最大争论是其高昂的价格。目前已经商业化的疗法的价格分别为37.3万到47.5万美元,但是如果考虑应用和管理这些疗法的医疗成本,每位患者的花费可能增加到100万美元。生物制药公司常以细胞免疫疗法的潜在治愈属性,及其针对的临床需求,为高昂的定价进行辩护。在真实世界环境中证明细胞免疫疗法的疗效将是关键,这有利于将其纳入国家医保或商业健康险。由于细胞免疫疗法的高价,目前只在部分发达国家被纳入医保(图表10)。
图表10. 细胞免疫疗法在发达国家的医保支付政策

未来,细胞免疫疗法的高价将不可避免地影响其在中低收入国家(如中国)的商业化。生物制药公司在制定细胞免疫疗法定价模型时,应当深思熟虑地制定患者援助计划,减轻患者的经济负担,从而增加患者的就医机会。这有利于生物制药公司积累真实世界证据,从而支持细胞免疫疗法被纳入国家医保。
适应症的局限性
已获批的3款CAR-T疗法都是靶向CD19,治疗血液肿瘤,包括急性淋巴细胞白血病(ALL)、B细胞淋巴瘤和套细胞淋巴瘤(MCL)。血液肿瘤在全部肿瘤中仅占10%左右,而且已存在多种药物,如靶向PD-1/PD-L1、CD19、CD20的单抗和双抗,以及小分子BTK抑制剂等,是相对拥挤的赛道。获批的CAR-T疗法主要针对血液肿瘤复发后的后线治疗,患者数量相对一线治疗较少。
目前在研细胞免疫疗法的靶点较少,主要集中在CD19,潜在治疗血液肿瘤。实体瘤的相关靶点,如HER2、GPC3、GD2等都是肿瘤相关抗原(TAA),在正常细胞上也有表达。靶向这些靶点的细胞免疫疗法有可能存在脱靶效应,攻击正常细胞。在关于HER2靶向CAR-T治疗转移性结直肠癌的临床试验中,患者发生急性肺水肿并死于呼吸衰竭,与HER2在正常肺组织细胞上低表达相关。此外,改造后的免疫细胞如何渗透进入实体瘤的肿瘤微环境也是一大问题。
结 语
虽然细胞免疫疗法存在诸多问题,但是不应忽视其突出的疗效,以及临床治愈的潜力。相信随着科技的进展,细胞免疫疗法在突破通用性问题、解决安全性问题、拓展适应症之后,将会赢得巨大的市场潜力,并且给患者带来治愈的希望。