胃癌一线诱导化疗后免疫治疗维持治疗对比化疗
Avelumab是一种PD-L1抗体,在非小细胞肺癌、间皮瘤等多种实体肿瘤中显示出抗肿瘤活性及可耐受的安全性。在一项JAVELIN Solid Tumor trial Ⅰb期临床研究中,Avelumab维持治疗在一线化疗后无进展的晚期胃癌(GC)或胃食管交界癌(GEJC)中展现出令人鼓舞的效果。然而尚需大规模Ⅲ期临床研究进一步验证。

目的
本项Ⅲ期临床研究旨在进一步扩大研究GC/GEJC一线诱导化疗后应用Avelumab维持治疗的疗效。
患者及方案
JAVELIN Gastric 100是一项全球的、开放标签Ⅲ期试验。入组条件为未经治疗、不可切除、HER2阴性、局部晚期或存在转移的GC或GEJC患者。将接受过奥沙利铂联合氟尿嘧啶一线化疗12周后无进展的患者1:1随机分为两组,分别予Avelumab 10 mg/kg·2周维持治疗或继续化疗。主要研究终点为总生存时间(OS,从诱导化疗12周后随机分组开始算起)。
结果
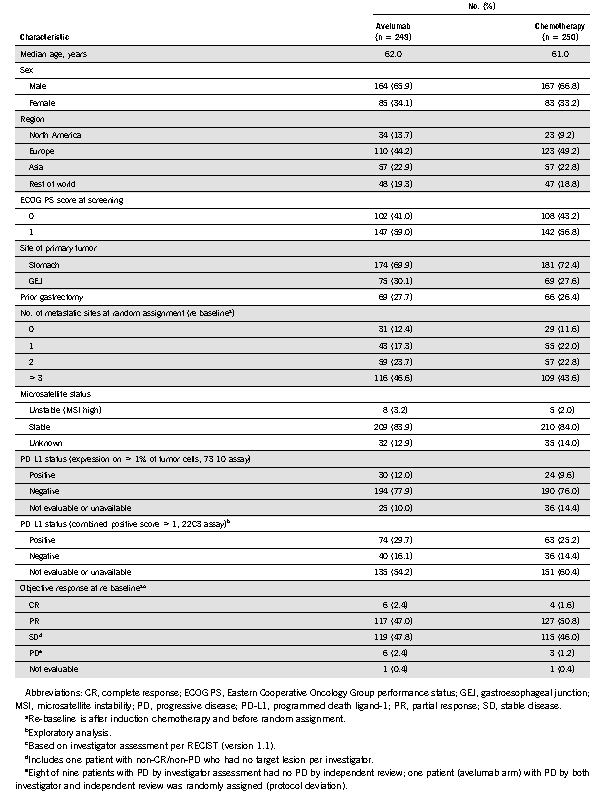
总共805位患者接受诱导化疗,其中499人随后被分别随机分配到Avelumab维持治疗组(n = 249)或继续化疗组(n = 250)(表1)。
表1 入组患者基线情况
Avelumab维持治疗组与继续化疗组的中位OS分别为10.4个月(95% CI: 9.1-12.0个月) vs 10.9个月(95% CI: 9.6-12.4个月);两组24个月OS率分别为22.1% vs 15.5%(HR=0.91; 95% CI: 0.74-1.11; P = 0.1779)(图1A)。在采用73-10 assay检测为PD-L1阳性(≥1%的肿瘤细胞)的患者中(n = 54),Avelumab维持治疗组与继续化疗组的中位OS分别为16.2个月(95% CI: 8.2个月-未达到) vs 17.7个月(95% CI: 9.6个月-未达到),OS的HR 为1.13(95% CI: 0.57-2.23; P = 0.6352)(图1B)。在采用22C3 assay检测为PD-L1阳性(联合阳性评分≥1)的患者中(n = 137),Avelumab维持治疗组与继续化疗组的中位OS分别为14.9个月(95% CI: 8.7-17.3个月) vs 11.6个月(95% CI: 8,4-12.6个月),HR为0.72(95% CI: 0.49-1.05)(图1C)。
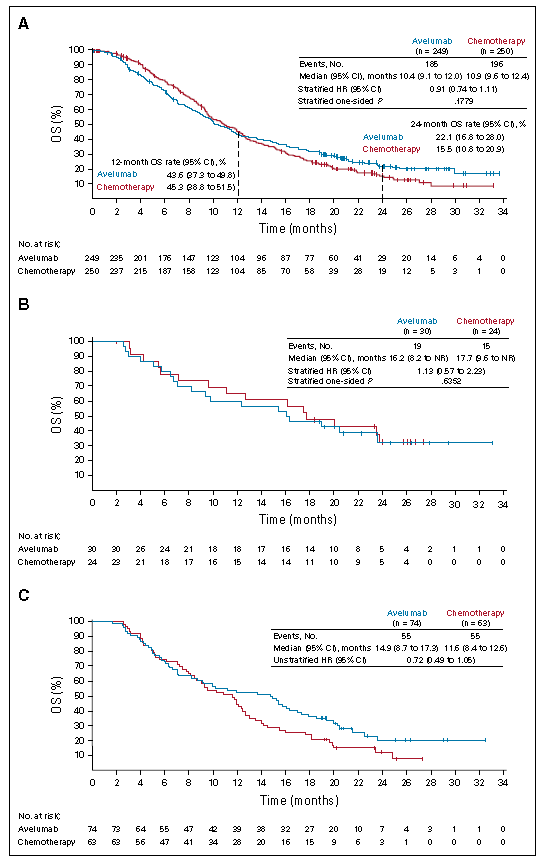
图1 各组患者OS情况
全部入组患者(A)、采用73-10 assay检测为PD-L1阳性(≥1%的肿瘤细胞)患者(B)及采用22C3 assay 检测为PD-L1性(联合阳性评分≥1)患者的OS(从诱导化疗12周后随机分组开始算起。)HR, hazard ratio; NR, not reached。
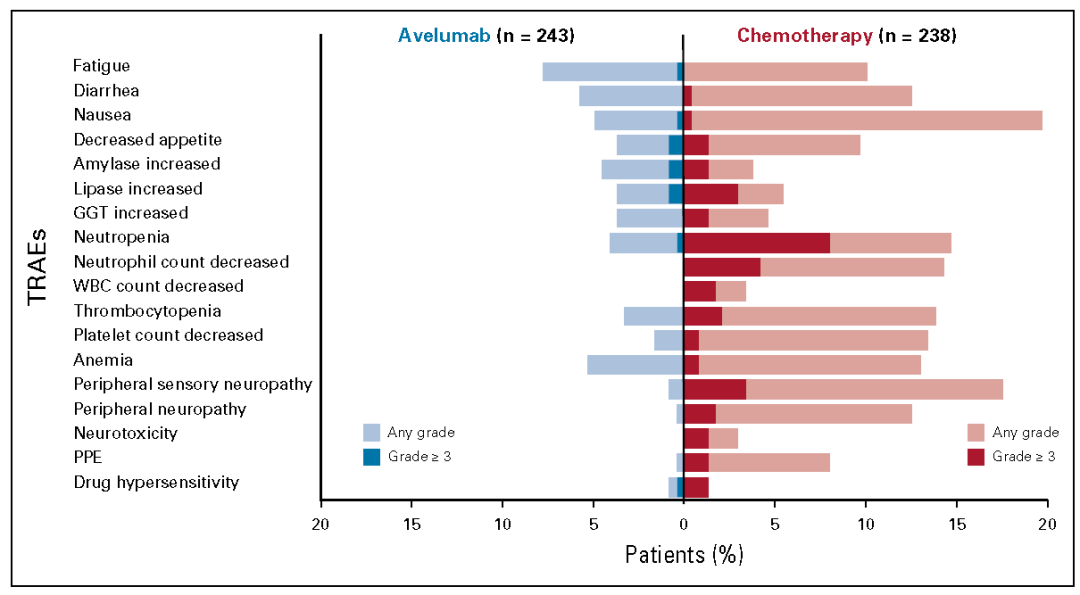
Avelumab和化疗的治疗相关不良事件(TRAEs)分别为149例(61.3%)和184例(77.3%),其中3级及以上不良事件分别为31例(12.8%)和78例(32.8%)(图2)。
 /p>
/p>
图2 各组治疗相关不良事件(TRAEs)分析
随机分组后在各组中任何级别的、发生率≥10%或≥3级、发生率≥1%的TRAEs。GGT, g-glutamyltransferase; PPE, palmar-plantar erythrodysesthesia syndrome
结论
在全部或明确为PD-L1阳性的晚期GC或GEJC患者中,Avelumab维持治疗对比继续化疗OS未见显著获益。然而,Avelumab维持治疗的TRAEs较继续化疗轻,并显示出反应时间延长等临床优势。
参考文献
Phase III Trial of Avelumab Maintenance After First-Line Induction Chemotherapy Versus Continuation of Chemotherapy in Patients With Gastric Cancers: Results From JAVELIN Gastric 100. J Clin Oncol. 2020 Nov 16; doi: 10.1200/JCO.20.00892.