遇到免疫相关不良反应还只会用激素?一文帮你“全通关”!
免疫药物治疗引起的总体不良反应发生率较化疗低,但是可引起“特殊”的免疫相关性不良反应(irAEs),这些irAEs多数为轻度。轻度irAEs(G1-2)和大部分G3-4 irAEs经过早期激素治疗后可控制良好,部分患者可再次接受免疫检查点抑制剂(ICIs)治疗,但仍有一小部分irAEs临床表现严重或不能通过激素有效控制,患者后续可能因irAEs未控、激素使用继发的不良反应或原发肿瘤进展等危及生命。这就是所谓的危重型或难治性irAEs。
目前危重型或难治性irAEs的治疗目前存在许多问题:危重型irAEs的处理原则较少且笼统;难治性irAEs的处理原则缺乏共识并且定义不清楚,没有将“难治性irAEs”这一临床确实存在的情况作为一种特殊的irAEs进行阐述和推荐。而现实是——只有克服危重型或难治性irAEs才能确实提高irAEs的管理成功率。
碰到危重型或难治性irAEs怎么办?激素抵抗/无效怎么办?医学界肿瘤频道特邀武汉大学人民医院章必成教授,教你危重型或难治性irAEs“通关全策略”!
要点提示:
危重型或难治性irAEs的机制
危重型或难治性irAEs的处理原则
危重型或难治性irAEs的处理现状(包括危重型或难治性皮肤毒性、内分泌毒性、肝脏毒性、胰腺炎、腹泻/结肠炎、肺毒性、神经毒性、血小板减少、心脏毒性等)
危重型或难治性irAEs的机制
为什么会发生危重型或难治性irAEs?低级别或普通irAEs如何发展为危重型或难治性irAEs?随着对危重型或难治性irAEs机制的不断深入了解,可概括如下:免疫耐受失衡;肿瘤释放抗原,发生交叉抗原呈递;细胞因子;脱靶效应;微生物的抗炎和促炎的动态调节等。
且不同脏器发生irAEs的机制可能不同:
中枢神经系统irAEs可能分为淋巴浸润丰富型、抗体介导型(如anti-Hu相关性脑炎)或无菌性炎症;
皮肤irAEs,比如斑状丘疹淋巴浸润丰富,苔藓样/牛皮藓表现出混合浸润的特点,而大疱性反应由抗体介导;
免疫相关肾炎或肌肉骨骼系统irAEs可能由淋巴细胞驱动、补体介导、抗体介导或无菌性炎症引起(如pauci免疫性肾小球肾炎);
免疫相关性肠炎的发生可能更多地与TNF-ɑ异常产生有关。
(答案在文末公布哦~)
危重型或难治性irAEs的处理原则
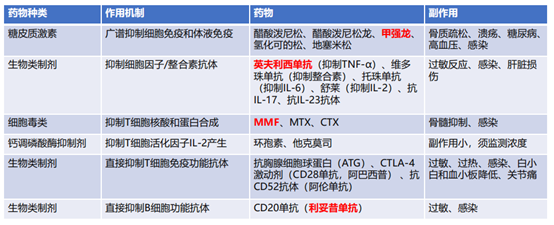
推荐糖皮质激素(以下简称激素)作为大多数irAEs的一线治疗;对于≥G3 irAEs患者,尤其是影响到心脏、肺、肝脏、结肠和神经肌肉系统的irAEs,建议进行免疫组织病理学检测,同时展开针对irAEs发病机制的系统分析,为后续的irAEs靶向治疗提供初步指导;同时,irAEs应强调MDT管理。
在激素无效的情况(≧3天症状仍持续)下可以考虑:升级治疗(激素加量);免疫调节剂:丙种球蛋白(5天);免疫抑制剂:英夫利昔单抗(5mg/kg,第1、2、6周)、麦考酚酯(1g,2次/日)、他克莫司以及其他药物:IL-6抗体(托珠单抗)、CTLA-4激动剂(阿巴西普)、抗CD52抗体(阿伦单抗)、CD20单抗(利妥昔单抗)、整合素、血浆置换、抗胸腺细胞免疫球蛋白(ATG)等。
并且在临床治疗中应该尽量避免反复使用大剂量激素。但以下情况可以考虑使用:
严重的心脏毒性;
严重的神经毒性:格林巴利综合征;免疫相关性脑炎;横断性脊髓炎;
严重的复合/多重毒性。
同时,临床医生应该关注大剂量使用激素继发的血糖升高、细菌和病毒等感染,建议在免疫抑制开始前进行结核和病毒性肝炎检测,必要时采取适当的抗菌、抗病毒等预防措施。
危重型或难治性irAEs的处理现状
▌ 危重型或难治性皮肤毒性:
1.根据现有指南/共识,斑丘疹/皮疹、瘙痒及反应性皮肤毛细血管增生症(RCCEP)分为3个级别,无G4毒性,未考虑难治性irAEs的情况。
2.危重型皮疹定义为大疱性皮炎、Stevens-Johnson综合征(SJS)/中毒性表皮坏死松解症(SJS/TEN)和伴嗜酸粒细胞增多和系统症状的药疹(DRESS),多为G3-4,并可同时出现。如果患者发生此种irAEs应永久停用ICIs,并接受泼尼松/甲强龙1-2mg/kg/d的治疗。
3.在真实世界中,银屑病、血管炎伴紫癜性皮疹等均可呈危重型或难治性。激素是首选;硫唑嘌呤、霉酚酸酯、甲氨蝶呤、四环素类抗生素、达普松和烟酰胺可以作为激素替代药物。对急性期严重银屑病,可以考虑英夫利昔单抗、IL-1阻断剂、IL-23、IL-17和IL-12单抗,合并关节疼痛时考虑使用激素。皮肤血管炎推荐用CD20单抗。
▌ 危重型或难治性内分泌毒性:
对甲状腺、肾上腺、垂体和胰腺等炎症以及胰腺受累引发的高血糖,均未推荐使用激素,G4毒性均未涉及停药,恢复至G1后可再次挑战ICIs。胰岛、肾上腺功能无法完全恢复,需终生使用替代治疗。Ipilimumab治疗者需高度警惕垂体炎。对腮腺炎和唾液腺炎,尚无相应的处理意见。
▌ 危重型或难治性肝脏毒性
1.各指南/共识分级标准不一。欧洲肿瘤内科学会(ESMO)、美国国家综合癌症网络(NCCN)、美国临床肿瘤学会(ASCO)指南未将胆红素升高纳入分级标准之内;癌症免疫治疗学会(SITC)的G4毒性标准较低;中国临床肿瘤学会(CSCO)指南相对全面,并要求在irAEs缓解不满意时行病毒性肝炎检查。推荐激素、麦考酚酯和他克莫司相继使用。疗效不佳时,观察窗口期为2-3d。ATG可作为激素无效时的推荐治疗,但不推荐或谨慎推荐使用英夫利昔单抗。
2.重视谷草转氨酶(aspartate aminotransferase,AST)/谷丙转氨酶(alanineaminotransferase,ALT)比值变化,可能反映是否存在肝脏以外的损伤。当胆酶分离往往提示肝功能极度恶化、危及生命,但是在irAEs的范畴内是否具有相同的临床意义尚不清楚。已有IL-6单抗、CD20单抗、英夫利昔单抗成功治疗免疫相关性肝炎的案例。
▌ 危重型或难治性胰腺炎:
只有NCCN、ASCO指南将胰腺毒性作为一项孤立的毒性列出,建议如果患者出现G2毒性即停止ICIs并予激素治疗;如出现G3-4毒性,如淀粉酶/脂肪酶升高至>3倍正常值上限,和/或放射学异常,和/或中度腹痛或呕吐,及血液动力学不稳定,血糖变化等,建议激素及专科治疗,疗效差者可考虑麦考酚酯。关于其他治疗尚无相应报告和推荐,但特异性免疫抑制治疗值得探索。
▌ 危重型或难治性腹泻/结肠炎:
1.CSCO指南指出G3-4腹泻无需等待肠镜即可开始激素,如48h激素无效考虑加用英夫利昔单抗;如果仍无效,可考虑&α;4&β;7整合素拮抗剂维多珠单抗,少有建议麦考酚酯。
ESMO指南不排斥止泻药,其他指南对止泻药未做相关建议。
2.对于严重肠炎,英夫利昔单抗+激素可考虑作为一线选择,对于长期使用激素效差的难治性腹泻/结肠炎需要尽快肠镜,首先排除感染,如巨细胞病毒(CMV)和难辨梭杆菌等继发感染。对于难治性腹泻/结肠炎尤其英夫利昔单抗效不佳时,可以尝试使用IL-6抑制剂、环孢霉素、那他珠单抗、IL-1抑制剂、IL-17单抗、IL-23单抗及IL-2单抗等。
▌ 危重型或难治性肺毒性:
针对G3及以上肺炎,可经验性使用抗生素,并同时给予静脉激素治疗。但临床上仍有10-15%患者对激素不敏感,治疗2d无好转加用免疫抑制剂,如英夫利昔单抗、麦考酚酸或环磷酰胺等;也可使用免疫球蛋白、IL-6抑制剂等,必要时给予ICU支持。推荐常规进行支气管镜检查,不仅可以纠正经验治疗的偏差,而且有望查清可能存在的病原菌。
▌ 危重型或难治性神经毒性:
1.重症肌无力:建议使用甲强龙1-2mg/kg/d;避免使用可能加重症状的药物(如&β;-受体阻滞剂、含镁离子药物、喹诺酮类、氨基糖苷类及大环内酯类抗生素等);效果不佳时,免疫球蛋白0.4g/kg/d或血浆置换,5d。
2.格兰巴雷综合症:免疫球蛋白0.4g/kg/d,或者血浆置换,5d;试验性应用甲强龙2-4mg/kg/d;也有推荐使用1g/d,5d,与免疫球蛋白或血浆置换联合应用;也有推荐先行免疫球蛋白或血浆置换,激素逐渐增量。
3.无菌性脑炎:甲强龙(必要时大剂量);免疫球蛋白;CD20单抗;血浆置换;经验性抗病毒及抗生素治疗。
总体上,建议激素与免疫球蛋白或血浆置换联用,可反复使用,即21d一次,3-4次。指南除了对无菌性脑膜炎有CD20单抗推荐外,其余均未推荐免疫抑制剂。但在临床实践中,亚急性和慢性炎症性脱髓鞘性多发性神经根神经炎、重症肌无力、脑炎、无菌性脑膜炎等均有从免疫抑制剂(IL-1受体抑制剂、IL-6受体抑制剂和CD20单抗)中获益的成功报道;脑炎和无菌性脑膜炎可应用IL-1受体抑制剂和CD20单抗。
▌ 危重型或难治性血小板减少:
ESMO、NCCN、ASCO指南未涉及免疫性血小板减少症,SITC提及病名但无处理建议,只有CSCO指南有较详细的描述:G3以上毒性时暂停ICIs,予泼尼松1-2mg/kg/d口服,如果无缓解或者恶化,继续使用泼尼松,联合免疫球蛋白1g/kg,并根据需要重复使用;可考虑使用CD20单抗、血小板生成素受体激动剂艾曲波帕。
▌ 危重型或难治性心脏毒性
1.G3-4心肌毒性需立即请心内科会诊,完善心电图、心肌标志物、炎性标志物、心脏彩超和/或心肌增强MRI检查,心电监护。药物治疗方面推荐使用甲强龙,1g/d,3-5d;激素治疗24h无改善时加用ATG、英夫利昔单抗等。可考虑使用抗病毒治疗、免疫球蛋白或透析等。但要警惕:英夫利昔单抗与心衰有关,中-重度心衰者禁用。
2.心律失常、房室传导阻滞者死亡率最高,其中36%患者可出现完全性房室传导阻滞(60%死亡),21%患者出现心律失常时肌钙蛋白/肌酸激酶并未明显升高。心脏起搏器植入和心内科专科治疗对于改善预后最为重要。部分心肌炎的患者尽管在激素冲击治疗后心肌酶稳步下降,后续仍可出现恶性心律失常导致死亡,活检也证实心肌内存在未控制的炎症。免疫抑制剂可能是成功的关键。