帕博利珠单抗一线治疗结直肠癌在中国拟纳入优先审评;徐兵河教授团队研究带来转移性乳腺癌治疗新方案
要点提示
Ann Oncol:优替德隆联合卡培他滨可延长难治性转移性乳腺癌总生存
Ann Oncol:基于RNA的GemPred分层可预测从吉西他滨化疗中获益的PDAC患者
Neuro-Oncology:HFSRT联合帕博利珠单抗和贝伐珠单抗治疗复发性高级别胶质瘤患者安全且耐受性好
CCR:两性调节蛋白是抗EGFR治疗转移性结直肠癌预后的预测指标
JAMA Surg:前哨淋巴结活检可用于对子宫内膜癌进行外科分期
新药:帕博利珠单抗一线治疗结直肠癌在中国拟纳入优先审评
新药:舒格利单抗一线治疗非小细胞肺癌上市申请获NMPA受理
1
Ann Oncol:优替德隆联合卡培他滨可延长难治性转移性乳腺癌总生存
11月11日,Annals of Oncology在线发布一篇优替德隆联合卡培他滨与单独使用卡培他滨治疗难治性转移性乳腺癌(MBC)的III期试验总体生存结果的文章。该研究结果提示优替德隆联用卡培他滨可作为治疗MBC患者的一种新的有效治疗方案。本文第一作者为中国医学科学院肿瘤医院徐兵河教授。

共有405名患者被随机分为两组,分别接受优替德隆联合卡培他滨或单用卡培他滨,每21天为一周期。在最终总生存(OS)分析中,优替德隆联合卡培他滨组的中位随访时间为19.6个月,而单独使用卡培他滨组的中位随访时间为15.4个月。
结果显示:
在意向治疗人群中,在数据截止点发生了313例死亡。联合治疗组270名患者中有203名死亡,单药治疗组135名患者中有110名死亡。
联合治疗组中位OS为19.8个月,单药治疗组为16.0个月(HR 0.75,95%CI 0.59-0.94,P=0.0142)。
两组治疗的安全性没有显著差异。安全性结果在发生率、严重性和特异性方面与此前报道的相似。
优替德隆只引起轻微的骨髓抑制,没有明显的肝脏毒性。虽然周围神经病变的不良反应很常见,但调整剂量后,通常是可控和可逆的。
对于多线治疗失败、对蒽环类和紫杉类药物耐药的MBC患者,与单独使用卡培他滨相比,优替德隆联用卡培他滨可显著延长OS。这些结果支持优替德隆联用卡培他滨作为治疗MBC患者的一种新的治疗方案。
2
Ann Oncol:基于RNA的GemPred分层可预测从吉西他滨化疗中获益的PDAC患者
日前,Annals of Oncology在线发布一项研究证实基于RNA的GemPred分层可预测从吉西他滨化疗中获益的胰腺导管腺癌(PDAC)患者。

该研究对来源于PDAC患者的临床前模型(原代细胞培养和患者来源的异种移植)化疗敏感性和全基因组RNA谱进行分析。在单中心队列(切除PDAC样本67例)中检测基于RNA的GemPred分层并在多中心队列(切除PDAC样本378例)中进行验证。在单中心队列和多中心队列中,分别有43(65%)和203(55%)名患者接受了吉西他滨辅助化疗。
吉西他滨化疗敏感PDAC定义为GemPred+。与GemPred-患者相比,GemPred+患者OS较高(P=0.046和P=0.00216)。在两个队列中,未接受吉西他滨化疗的患者,其GemPred分层与OS无关。在接受吉西他滨化疗的患者中,GemPred+患者的OS显著高于GemPred-患者[91.3个月(95%CI 61.2-未达到) vs 33个月(95%CI 24-35.2);HR 0.403(95%CI 0.221-0.735,p=0.00216)]。吉西他滨与GemPred+分层交互作用显著(p=0.0245)。
研究表明,基于RNA的GemPred分层可预测从吉西他滨化疗中获益的PDAC患者。
3
JAMA Surg:前哨淋巴结活检可用于对子宫内膜癌进行外科分期
11月11日,JAMA Surgery发布一篇探讨前哨淋巴结活检(SLNB)对中、高级子宫内膜癌(EC)患者SLNB的诊断准确性、临床表现特点及发病率的前瞻性多中心队列研究。研究结果显示,SLNB在淋巴结转移风险最大的高级EC患者中,具有与淋巴结切除术相似的诊断准确性和预后能力。

本研究共纳入156例患者(中位年龄65.5,范围40-86岁;中位体重指数27.5,范围17.6-49.3),其中126例为高级别EC。所有患者均接受SLNB和盆腔淋巴结清扫术(PLND)治疗,101例(80%)高级别EC患者同时接受腹主动脉旁淋巴结清扫术(PALND)治疗。
前哨淋巴结的检出率分别为97.4%(95%CI 93.6%-99.3%)、87.5%(95%CI 83.3%-91.0%)和77.6%(95%CI 70.2%-83.8%)。
在27例(17%)淋巴结转移患者中,SLNB算法正确识别26例,敏感性为96%(95%CI 81%-100%),假阴性率为4%(95%CI 0%-19%),阴性预测值为99%(95%CI 96%-100%)。仅有1例患者(0.6%)被SLNB算法误识。
26%(7/27)的淋巴结转移患者存在在PLND边界外有前哨淋巴结转移,或需要免疫组织化学来诊断的情况。
在这项前瞻性队列研究中,SLNB对于淋巴结转移风险增加的高级别EC患者有可接受的诊断准确性,并且与淋巴清扫相比,提高了淋巴结阳性病例的检出率。研究结果表明,SLNB可用于对EC进行外科分期。
4
Neuro-Oncology:HFSRT联合帕博利珠单抗和贝伐珠单抗治疗复发性高级别胶质瘤患者安全且耐受性好
日前,Neuro-Oncology在线发布一项临床I期研究证实,低分割立体定向放疗(HFSRT)联合帕博利珠单抗和贝伐珠单抗治疗复发性高级别胶质瘤患安全且耐受性好。

放疗可能与PD-1/PD-L1抑制剂具有协同作用。该研究纳入32名复发性胶质母细胞瘤或间变性星形细胞瘤患者,所有患者接受帕博利珠单抗(100/200mg,每三周1次)、HFSRT(总剂量30Gy,5次分割)和贝伐珠单抗(10 mg/kg,每两周1次)。
结果显示,最常见的治疗相关不良事件(TRAE)为蛋白尿(40.6%)、疲劳(25%)、丙氨酸转氨酶升高(25%)和高血压(25%)。1例患者因出现3级天冬氨酸转氨酶升高而停药。
在先前未接受过贝伐珠单抗的患者中,20名患者(83%)达完全缓解(CR)或部分缓解(PR)。中位OS和无进展生存期(PFS)分别为13.45个月(95%CI 9.46-18.46)和7.92个月(95%CI 6.31-12.45)。
在贝伐珠单抗耐药队列中,5例患者(62%)达PR。中位OS为9.3个月(95%CI 8.97-18.86),中位PFS为6.54个月(95%CI 5.95-18.86)。大多数患者(20/26,77%)肿瘤细胞或肿瘤微环境PD-L1表达<1%。
研究表明,HFSRT联合帕博利珠单抗和贝伐珠单抗治疗复发性高级别胶质瘤患者安全且耐受良好。
5
CCR:两性调节蛋白是抗EGFR治疗转移性结直肠癌预后的预测指标
11月11日,CCR发布一篇关于抗EGFR治疗转移性结直肠癌的疗效预测指标的文章。研究结果表明,两性调节蛋白(AREG)高表达与抗EGFR治疗的疗效密切相关,是mCRC预后的良好标志。

该研究团队评估了参与随机对照试验FIRE-1、CIOX和FIRE-3的mCRC肿瘤组织中配体mRNA的表达、RAS、BRAF、PIK3CA突变和EGFR的表达。采用Kaplan-Meier方法,包括单因素和多因素Cox回归分析,评估患者的OS和PFS。
在688例患者中,有343例(大于中位数)和172例(大于第三四分位数)患者检测到AREG高表达。
与两个低表达的阈值相比,AREG高表达与OS(26.2个月 vs 21.5个月,HR=0.80,95%CI 0.68-0.94,P=0.007)、PFS(10.0个月 vs 8.1个月,HR=0.74,95%CI 0.63-0.86,P=0.001)和ORR(63.1% vs 51.6%,P=0.004)显著增高相关。在多因素Cox回归分析中,影响仍明显(OS:P=0.01,PFS:P=0.002)。
在RAS基因野生型mCRC患者中,与贝伐单抗疗效相比,西妥昔单抗(OS:P=0.02,PFS:P=0.04)的疗效与AREG mRNA高表达显著相关。
AREG mRNA高表达是mCRC预后的良好标志,与抗EGFR治疗的疗效密切相关。
6
新药:帕博利珠单抗一线治疗结直肠癌在中国拟纳入优先审评
11月12日,中国国家药监局药品审评中心(CDE)位点最新公示,PD-1抑制剂帕博利珠单抗注射液以“符合附条件批准的药品”拟纳入优先审评,拟定适应症为结直肠癌一线治疗。根据CDE官网信息,帕博利珠单抗此前在中国递交的6项新药上市申请均曾正式纳入优先审评。
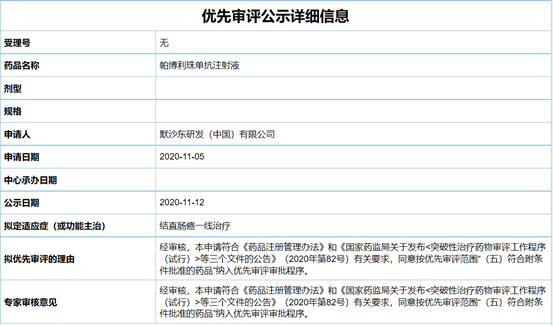
此前,该产品已在中国获批多个适应证,涉及癌种有黑色素瘤、鳞状/非鳞状非小细胞肺癌(NSCLC)、PD-L1表达阳性NSCLC,以及食管鳞状细胞癌。另外,帕博利珠单抗用于特定复发性头颈部鳞状细胞癌(HNSCC)患者一线单药治疗的新药上市申请也已于今年7月被纳入优先审评,目前该申请正在审评审批中。
此次帕博利珠单抗在中国拟纳入优先审评,拟定适应证为结直肠癌一线治疗。具体为一线治疗不可切除或转移性微卫星不稳定性高(MSI-H)或错配修复缺陷(dMMR)结直肠癌患者。
7
新药:舒格利单抗一线治疗非小细胞肺癌上市申请获NMPA受理
11月12日,基石药业宣布,中国国家药品监督管理局(NMPA)已受理舒格利单抗(CS1001,抗PD-L1单抗)的新药上市申请(NDA),用于联合化疗一线治疗晚期鳞状和非鳞状NSCLC患者。这是基石药业在全球范围内递交的舒格利单抗的首个NDA。基石药业今年在全球范围内已递交6个NDA,中国大陆地区占其中3个,目前已有4个NDA在受理中。
此次NDA的受理是基于一项III期临床研究结果,即舒格利单抗联合化疗用于一线治疗鳞状和非鳞状NSCLC患者的CS1001-302研究。详细的临床试验数据将于ESMO ASIA会议11月21日的Proffered Paper环节(Late-Breaking Abstract)进行口头报告。
参考文献:
1.B.Xu,T.Sun,Q.Zhang,P.Zhang,Z.Yuan,Z.Jiang,X.Wang,S.Cui,Y.Teng,X.-C.Hu,J.Yang,H.Pan,Z.Tong,H.Li,Q.Yao,Y.Wang,Y.Yin,P.Sun,H.Zheng,J.Cheng,J.Lu,B.Zhang,C.Geng,J.Liu,K.Shen,S.Yu,H.Li,L.Tang,R.Qiu.Efficacy of utidelone plus capecitabine versus capecitabine for heavily pretreated,anthracycline-and taxane-refractory metastatic breast cancer:final analysis of overall survival in a phase 3 randomised controlled trial.Annals of Oncology.Available online 11 November 2020.https://doi.org/10.1016/j.annonc.2020.10.600.
2.NicolleO R,Gayet O,Duconseil P,et al.A transcriptomic signature to predict adjuvant gemcitabine sensitivity in pancreatic adenocarcinoma.Annals of Oncology.2020;11.
3.Cusimano MC,Vicus D,Pulman K,et al.Assessment of Sentinel Lymph Node Biopsy vs Lymphadenectomy for Intermediate-and High-Grade Endometrial Cancer Staging.JAMA Surg.Published online November 11,2020.
doi:10.1001/jamasurg.2020.5060
4.Sahebjam S,Forsyth PA,Tran ND,et al.Hypofractionated Stereotactic Re-Irradiation with Pembrolizumab and Bevacizumab in Patients with Recurrent High Grade Gliomas:Results from a Phase 1 Study[published online ahead of print,2020 Nov 11].Neuro Oncol.2020;noaa260..https://doi.org/10.1093/neuonc/noaa260.
5.Arndt Stahler,Sebastian Stintzing,Dominik P.Modest,Ingrid Ricard,Clemens Giessen-Jung,Christine Kapaun,Boryana Ivanova,Florian Kaiser,Ludwig Fischer von Weikersthal,Nicolas Moosmann,Andreas Schalhorn,Martina Stauch,Alexander Kiani,Swantje Held,Thomas Decker,Markus Moehler,Jens Neumann,Thomas Kirchner,Andreas Jung and Volker Heinemann.Amphiregulin Expression Is a Predictive Biomarker for EGFR Inhibition in Metastatic Colorectal Cancer:Combined Analysis of Three Randomized Trials.Clin Cancer Res November 11 2020.
DOI:10.1158/1078-0432.CCR-20-2748
6.https://mp.weixin.qq.com/s/JAl7uF_khovhnfOZPos8QQ
7.https://www.wuximediatech.com/content/post/detail.html?sn=401c2afb54a84211913a7e32ec1f002a&from=wechat