一文读懂最新慢性淋巴细胞白血病诊疗
CLL是西方世界最常见的白血病,每年发病率达4.2/10万。对于年龄>80岁的人群,每年发病率增加至30/10万以上。CLL患者诊断时的中位年龄为72,据报道,约10%的CLL患者年龄小于55岁。由于CLL存在遗传易感性,CLL患者家庭成员的患病风险增加6-9倍。
诊断标准
CLL的诊断要求外周血形态成熟的单克隆B淋巴细胞≥5×109/L,流式符合CLL表型。
外周血CLL样细胞不足5×109/L且无淋巴结肿大、器官肿大或其他髓外病灶时,诊断为单克隆B淋巴细胞增多症(MBL)。
外周血CLL样细胞不足5×109/L,而淋巴结、脾脏或其他髓外部位受累时,诊断为小淋巴细胞淋巴瘤(SLL),需要注意的是,SLL和CLL是同一种疾病,两者的区别主要在于临床表现:CLL主要表现为外周血和骨髓浸润为主;而SLL则主要以淋巴结、脾脏等淋巴器官肿大等淋巴瘤表现为主。
疾病分期

启动治疗时机
1.无治疗指征,推荐观察等待:
既往研究表明,对于无治疗指征患者化疗并不能带来生存优势。这部分患者的标准治疗是观察等待(watch-and-wait)策略(1A)。在第1年,每3-12个月进行一次血细胞计数和临床检查,此后所有患者应每3个月随访一次。
由于缺乏临床证据,对于局限性、早期SLL无法给出循证治疗建议,但一致认为SLL的处理与CLL相似,SLL患者中仅考虑在特定局部对症状性淋巴结病进行局部放疗。
推荐意见:
无治疗指征CLL患者的标准治疗是观察等待策略(1A)。
2.有下述治疗指征之一,启动治疗:
存在进行性骨髓功能衰竭的证据,表现为发生贫血和/或血小板减少或贫血恶化。血红蛋白(Hb)<100 g/L或血小板计数<100×109/L为治疗适应证。但需要指出的是,在一些患者中,血小板可能会在很长一段时间内保持<100×109/L的稳定状态,此时并不需要治疗干预;
显著(即左肋缘下≥6 cm)或进行性或症状性脾肿大;
显著(即最长直径≥10 cm)或进行性或症状性淋巴结病;
进行性淋巴细胞增多症,2个月内增加≥50%,或淋巴细胞倍增时间(LDT)<6个月。LDT可以通过在2-3个月的观察期内,每隔两周测定绝对淋巴细胞计数(ALCs)的线性回归外推获得;初始血液淋巴细胞计数<30×109/L的患者可能需更长的观察期来确定LDT。应排除CLL以外,导致淋巴细胞增多的因素(如感染、使用激素),尤其是当LDT作为启动治疗的唯一标准时;
自身免疫并发症,包括对皮质类固醇反应不佳的贫血或血小板减少症;
症状性或功能性结外受累(如皮肤、肾脏、肺、脊柱);
疾病相关症状定义为以下任何一种情况:
过去6个月内不明原因体重减轻≥10%;
严重疲乏[即欧洲肿瘤协作组体能状态(ECOG-PS)≥2;无法工作或进行日常活动];
发热≥38.0℃持续≥2周,且无感染证据;
盗汗≥1个月,且无感染证据。
应排除导致这些症状的其他因素(例如继发性肿瘤、感染、睡眠障碍、焦虑、绝经),特别是当任何上述症状是启动治疗的唯一标准时。
一线治疗
CLL一线治疗有不同可用的治疗策略(图1),包括Bruton酪氨酸激酶抑制剂(BTKi)如伊布替尼持续治疗直至疾病进展或以化疗为基石与CD20抗体进行时间限制性治疗。此外,美国食品药品监督管理局(FDA)和欧洲药品管理局(EMA)最近批准维奈托克+奥滨尤妥珠单抗用于CLL的一线治疗也成为一种替代治疗选择。治疗决策应包括评估IGHV和TP53状态及患者相关因素,如用药情况、合并症、经济情况和治疗依从性。
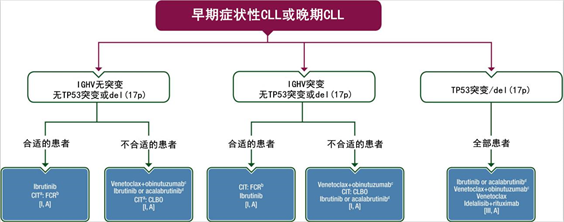
图1 CLL的一线治疗(a 只有在有理由反对靶向治疗或无法使用靶向治疗时,才使用CIT作为替代治疗;b 在65岁以上患者中也可考虑BR;c 可用情况下使用;d 如果批准且可用)
在III期随机试验中,与固定时间的抗CD20单抗为主的免疫化疗(CIT)[FCR(利妥昔单抗+氟达拉滨+环磷酰胺)、苯达莫司汀+利妥昔单抗(BR)、苯丁酸氮芥+奥滨尤妥珠单抗]相比,伊布替尼单药治疗或与CD20单抗联用的无进展生存期(PFS)更长(1A)。然而,尚未确定伊布替尼的最佳治疗持续时间。
对于有合并症的患者,与CIT相比,维奈托克+奥滨尤妥珠单抗联合治疗(如可用)作为首选治疗(1A)。
CIT仍被认为是适合IGHV突变CLL患者的一线治疗(2B),在咨询患者时,应考虑CIT诱发继发性肿瘤、白血病/骨髓增生异常综合征(MDS)和感染的长期风险。
对于接受CIT治疗的年轻适合CLL患者,应接受FCR治疗(1A)。对于>65岁的健康患者,由于FCR的感染和继发髓系肿瘤可能增加,应考虑BR(图1)(1A)。
TP53突变或del(17p)患者应接受BTKis作为一线治疗(3A)。
磷酸肌醇3激酶(PI3K)抑制剂艾代拉里斯+利妥昔单抗可用于不适合接受任何其他治疗的患者(3A)。
复发和难治性CLL的治疗
与一线治疗一样,复发后治疗仅适用于有症状的患者(图2),复发但无症状的CLL患者可以在不治疗的情况下长期接受随访。若接受靶向治疗时,疾病仍快速进展,建议立即调整治疗方案。
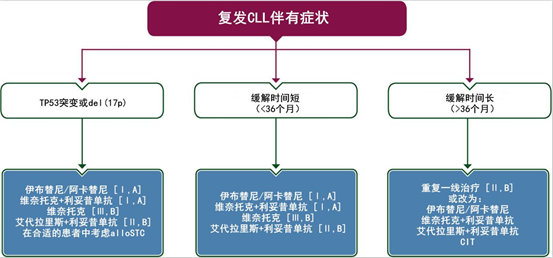
图2 复发CLL的治疗
如果持续治疗后3年内,出现症状性复发或对治疗无应答,无论一线治疗的类型如何(CIT或新型治疗),均应改变治疗方案:
应选择以下两种治疗选择之一(1A):
维奈托克+利妥昔单抗治疗24个月;
伊布替尼或阿卡替尼或其他BTK抑制剂持续治疗。
备选方案包括:
PI3K抑制剂艾代拉里斯联合利妥昔单抗(2B);
CIT,除非发现TP53突变或del(17p)且无其他可用的抑制剂或细胞疗法治疗选择;既往BR的缓解应持续至少3年以证明再次给药的合理性(2B)。由于毒性发生率和继发性髓系肿瘤风险增加,不建议重复给予FCR(5B)。
对于上述治疗方式的选择,应与患者讨论以下几个方面:
治疗持续时间(无终止vs.固定持续时间);
给药途径(口服vs静脉);
依从性(口服vs静脉);
证据(目前,伊布替尼一线治疗后启动维奈托克二线治疗的数据更多);
并发症风险(尤其是存在特定合并症时:伊布替尼或其他BTKi的出血和心脏合并症/维奈托克的肾功能受损和中性粒细胞减少症);
既往治疗的反应和副作用;
对于既往CIT后BCRi治疗期间发生的进展,则首选基于维奈妥昔单抗的治疗,换用其他CIT或BCRi不能诱导持久缓解(3B)。
如果既往时间限制性治疗后达到长期缓解(>3年),患者可再次接受相同的治疗方案,但证据有限(2B)。
造血干细胞移植和细胞治疗
自体干细胞移植(autoSCT)对CLL无效(1A),以下情况应考虑同种异体干细胞移植(alloSCT):
TP53突变或del(17p)的CIT难治性患者,但对新型抑制剂治疗应答完全。如果移植风险较低,应与患者讨论AlloSCT这一治愈性选择;
CIT和新型抑制剂治疗难治的患者,即使是非复发死亡风险较高的患者[造血细胞移植合并症指数(HCT-CI)评分≥3)](3B);
治疗后缓解且克隆与CLL相关的Richter转化患者。
对于以上三组人群,在临床试验中使用嵌合抗原受体T(CAR-T)细胞或双特异性T细胞衔接器(BiTE)抗体治疗可能是alloSCT的替代方法(5B)。但CAR-T细胞治疗CLL的经验较少,至少在两个方面与alloSCT有很大区别:
较低的非复发死亡率,可能存在急性毒性反应(细胞因子释放综合征;CAR-T细胞相关性脑病综合征),使得这种方法可用于有一些合并症的患者;
长期治疗潜力尚不确定
参考文献
1.Eichhorst B,Robak T,Montserrat E,Ghia P,Niemann CU,Kater AP,Gregor M,Cymbalista F,Buske C,Hillmen P,Hallek M,Mey U;ESMO Guidelines Committee.Electronic address:clinicalguidelines esmo.org.Chronic lymphocytic leukaemia:ESMO Clinical Practice Guidelines for diagnosis,treatment and follow-up†.Ann Oncol.2020 Oct 19:S0923-7534(20)42469-X.
2.刘澎.复旦大学附属中山医院慢性淋巴细胞白血病/小淋巴细胞淋巴瘤诊疗规范(v1.2018)[J].中国临床医学,2018,25(1):157-160.