IO治疗时代CRC外科手术标准需要重新定义 肝曲结肠癌穿透性侵犯十二指肠1例
结直肠癌是我国最为常见的恶性肿瘤之一,手术治疗是其最为重要的方法之一。医脉通肿瘤科邀请中山大学肿瘤防治中心陈功教授团队创立专栏——肠话短说,向每位读者传递最新的研究进展、最前沿的诊疗思路、最实用的临床经验。本期病例分享中,陈功教授分享了1例结肠肝曲癌并侵犯十二指肠患者的治疗过程。
病历简介
1
基本情况
男性,51,结肠肝曲癌并侵犯十二指肠。
2
既往检查治疗史
2020-02-21 胃镜提示:十二指肠降段肿物。病理(十二指肠降段)病变符合低分化腺癌。
2020-02-21 肠镜提示:结肠肝区癌?(距离肛门60cm)直肠多发小息肉。病理提示(结肠)符合低分化腺癌。
2020-02-27 PET/CT提示:
升结肠-横结肠(肝曲)管壁不均匀增厚,糖代谢增高,符合结肠腺癌。十二指肠管壁增厚、呈类结节状,糖代谢增高,符合十二指肠腺癌。
结肠病灶临近腹膜数个结节,部分糖代谢增高,考虑转移。余腹盆腔腹膜增厚并积液糖代谢未见异常。
右肺上叶前段、后段类结节灶,糖代谢未见异常,考虑炎性。
2020-03-06 基因检测:MSI-HMSH6突变,MSH2突变,NRAS野生型,KRAS野生型,HER2突变。公司事后计算TMB为35,但由于检测 PANEL的基因数目少,可能存在偏差。
2020-02-29,2020-03-22 行奥沙利铂+卡培他滨化疗2周期。
2020-04-15 复查腹部CT提示:结肠肝曲肠壁增厚,考虑结肠癌,周围脂肪间隙模糊并见多发淋巴结,增厚肠壁左侧囊片状低密度区,考虑肠壁穿孔伴包裏可能。
否认糖尿病,高血压病史;否认药物过敏病史。已婚己育,2男。否认手术病史。姐姐肠肿瘤,具体不详,父亲肝癌病史。
查体:LN-,心肺-,腹软,肝脾-,右侧上腹肋缘下5cm处可及腹块,边界不清,腹水-,肛査入指7cm未及异常。
于 2020-05-09、2020-05-25、2020-06-08、2020-06-22 予 FOLFIRI+PD-1抗体联合治疗4疗程,过程顺利。第1疗程治疗后出现发热,Tmax38.3℃,可自行退热,持续一周后好转。双下肢出现1度皮疹伴瘙痒,可自行消退。后2疗程治疗过程顺利耐受可。
2020-07-09 CT 提示:
胸部:(1)双肺各叶散在絮状淡薄密度增高影,滲出灶?(2)双肺上叶多发小结节,双肺各叶可疑多发细小结节影。
腹、盆腔:(1)结肠癌复査,现结肠肝曲肠壁增厚及软组织肿块,范围较前缩小,周围脂肪间隙较前清晰;(2)肠系膜淋巴结较前缩小,胆囊壁稍增厚;(3)膀胱壁稍増厚。
现患者偶诉乏力,胃纳尚可,大便约1次/日,近期体重无明显増减。
3
治疗计划
2020-07-09 外院 CT 显示肝曲肿物与十二指肠已经无黏连;建议继续治疗满6周期,然后评估胃镜、肠镜及腹盆 CT,拟手术。
4
诊断
结肠肝曲癌侵犯十二指肠并腹腔、淋巴结转移IV期,MSI-H。
陈功教授病例回顾与点评
该患者2020年2月份确诊肝曲结肠癌,穿透性侵犯十二指肠。结肠镜和胃镜均在相应部位看到肿瘤,病理活检均为腺癌,IHC提示MSH2和MSH6蛋白表达缺失。当地医院给予初始化疗CAPOX两个疗程,未见明确疗效。NGS基因检测确认为dMMR/MSI-H结肠癌,TMB 35。在我院接受FOLFIRI+国产PD-1单抗共6周期,CT显示原发肿瘤明显退缩,与十二指肠粘连已经几乎完全分离。胃镜检查显示,十二指肠未见异常,结肠镜检查,仍然可见肝曲结肠肿物,但内镜活检均未见肿瘤细胞。患者主观拒绝继续治疗。
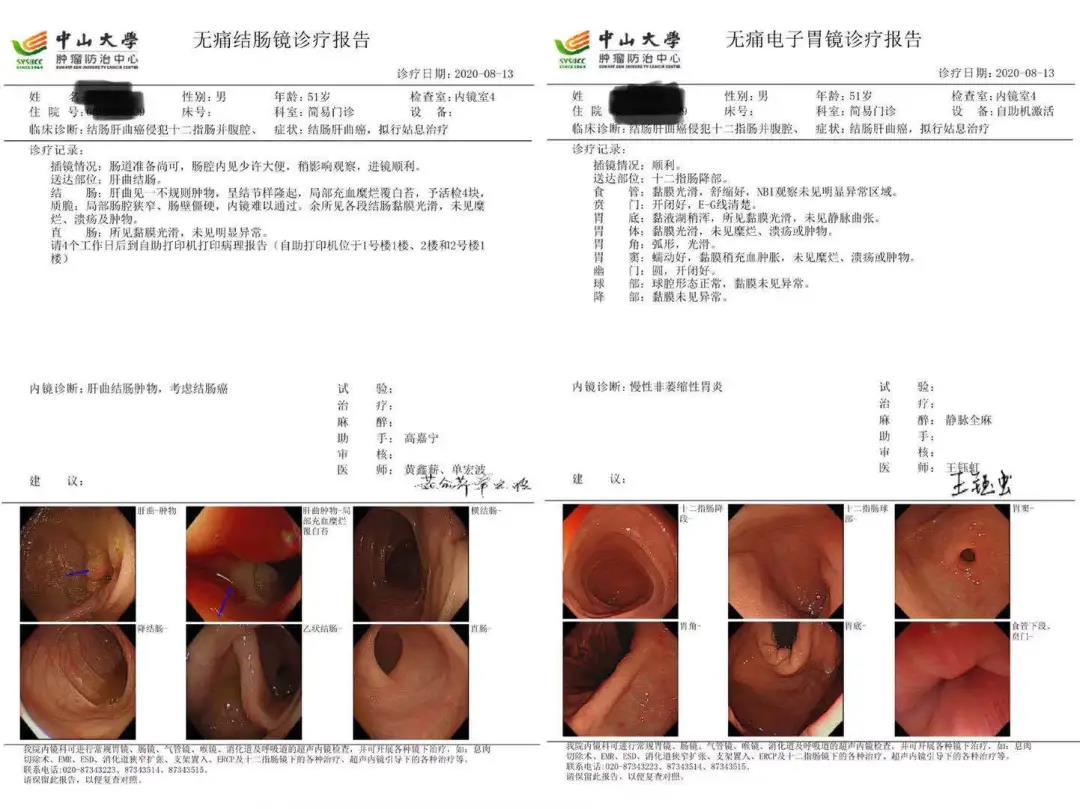
摆在外科医生面前的问题来了:还要不要手术?
我们选择了手术,一方面,难以确认该患者是否真的达到了CR;另一方面,外科需要积累更多的类似病例来重新确立手术/不手术的标准。
手术当天,我和丁培荣主任在手术前进行了广泛、充分的探讨,手术中仍然可以发现原发肿瘤部位与十二指肠浆膜面成轻度粘连,但电凝钩很容易就可以分开。外科切除标本如下:
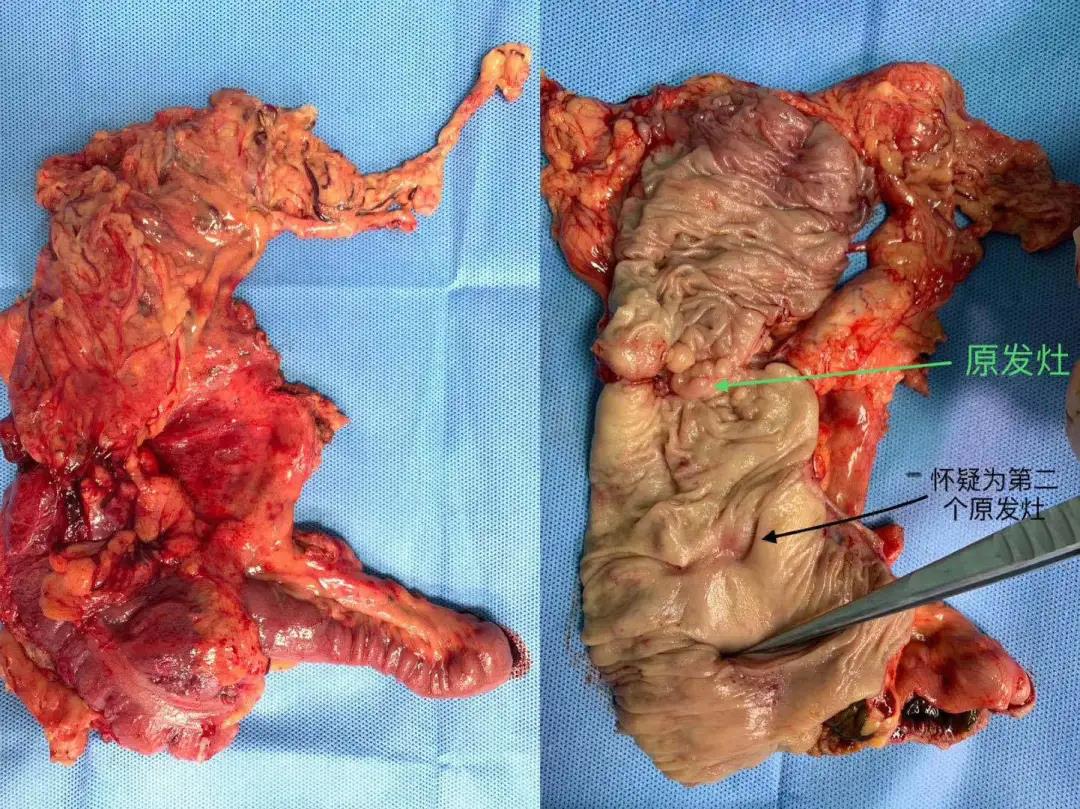
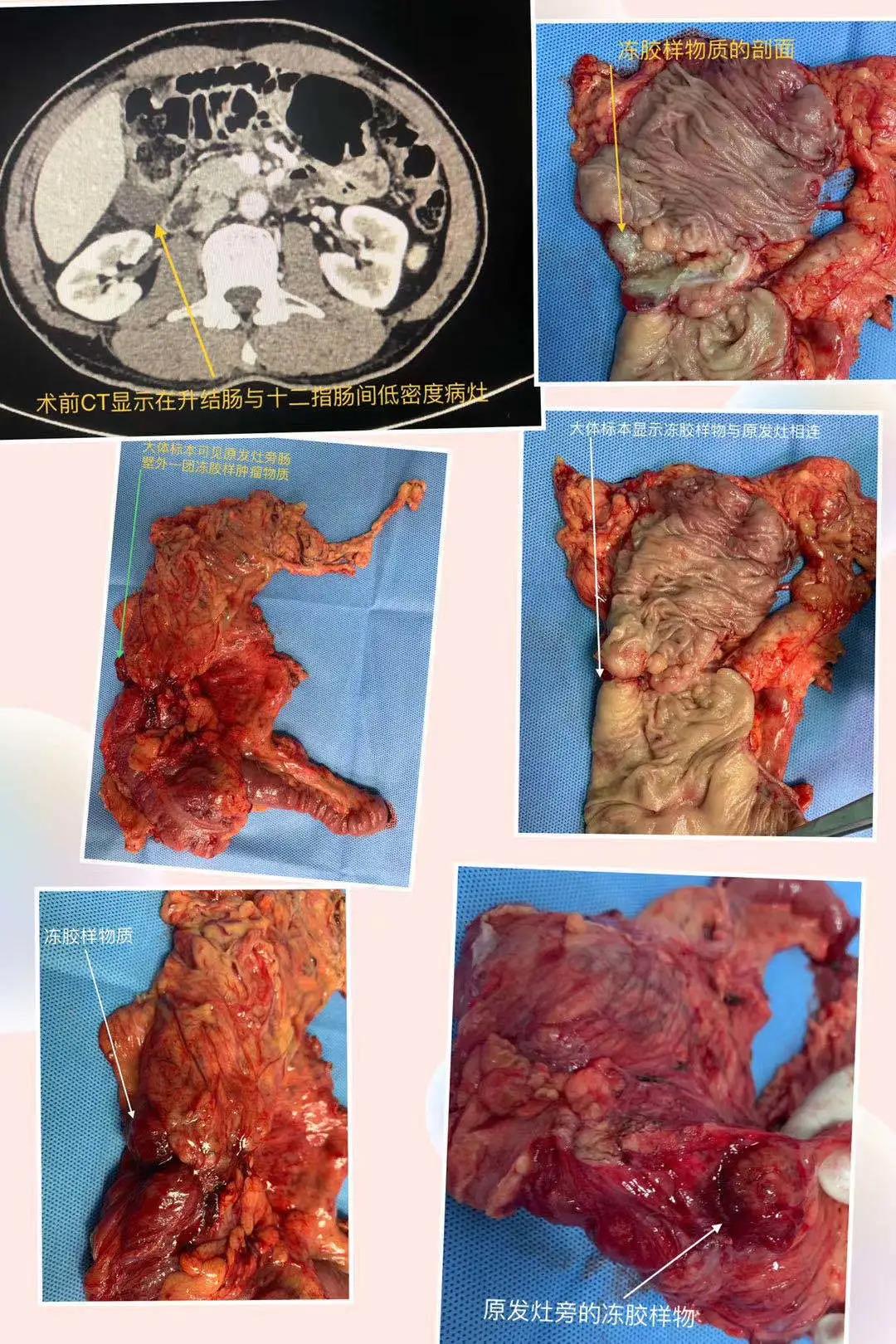
最终病理诊断结果揭晓,肿瘤完全消失,达到了pCR。基于既往一些类似患者的手术经验,手术时我就认为pCR是大概率事件。随着越来越多的病例积累,我们更加加深了外科层面的判断经验。

很显然,这位患者是幸运的,因为他有这样特殊的基因表型MSI-H,通过有奇效的免疫治疗,患者豁免了传统上需要做的胰十二指肠切除术(Whipple术),现在的问题是,这些患者未来也许完全可以不再需要手术。
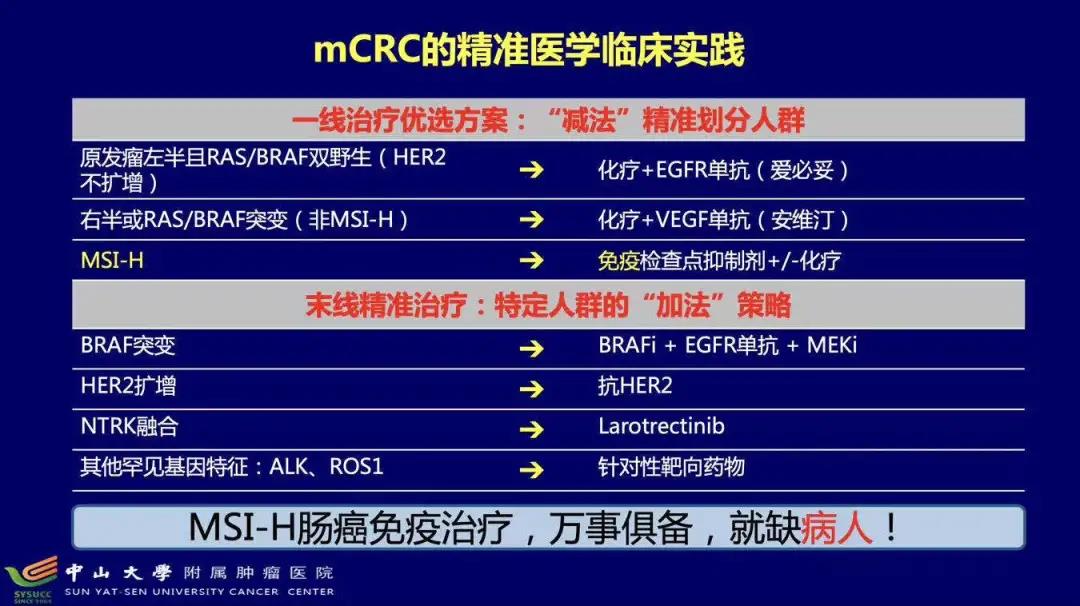
总而言之,对于MSI-H肠癌的免疫治疗(不管早期还是晚期),万事俱备,就缺病人了!病人从哪里来?各位同仁应切记所有肠癌患者均应首先筛选MSI状态,尤其是那些巨块型T4b期肿瘤患者。