口头报告专场 乳腺癌重磅研究盘点!
早期乳腺癌
IMpassion031研究:阿替利珠单抗+化疗新辅助治疗为高危早期TNBC带来新希望!
背景:I-III期三阴性乳腺癌(TNBC)占新诊断早期乳腺癌的10%~20%。早期TNBC患者优选的新辅助方案包括以紫杉烷类+蒽环类为基础的治疗方案。
IMpassion130研究显示,与单独白蛋白结合型紫杉醇相比,阿替利珠单抗+白蛋白结合型紫杉醇可为PD-L1阳性转移性TNBC患者带来无进展生存期(PFS)获益和有临床意义的总生存期(OS)获益。
IMpassion031是在高危原发性侵袭性早期TNBC患者中开展的一项全球、多中心、随机双盲、安慰剂对照III期临床研究,旨在评估阿替利珠单抗或安慰剂+白蛋白结合型紫杉醇新辅助治疗序贯阿替利珠单抗或安慰剂+剂量密集多柔比星+环磷酰胺的疗效和安全性。本次ESMO大会首次公布了IMpassion031的研究结果。
方法:入组患者为年龄≥18,既往未经治疗、中心证实的侵袭性II-III期早期TNBC,肿瘤大小> 2 cm。入组患者按1:1比例随机分配接受6剂阿替利珠单抗(840 mg)或安慰剂(q2w)+白蛋白结合型紫杉醇(125 mg/m2qw),序贯4剂阿替利珠单抗(840 mg)或安慰剂(q2w)+ 多柔比星(60 mg/m2)+ 环磷酰胺(600 mg/m2 q2w),随后接受手术治疗。手术后评估所有患者的病理学完全缓解(pCR;ypT0/isN0)。根据诊断分期(II vs III)和肿瘤浸润免疫细胞中PD-L1的表达(IC;≥1%vs < 1%)进行分层。共同主要终点是ITT或PD-L1 +(PD-L1 IC≥1%)患者的pCR。次要终点包括无事件生存期(EFS)和安全性。
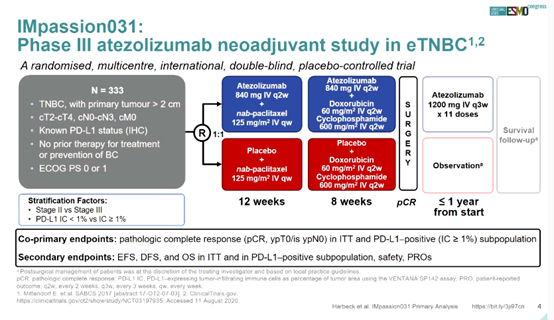
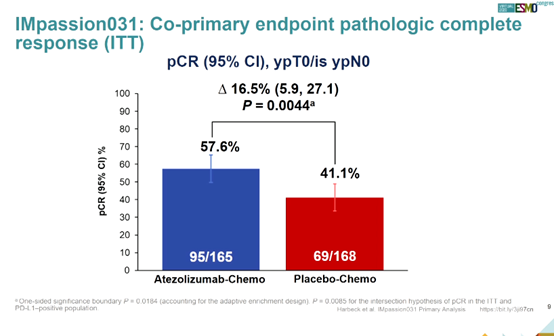
结果:333例患者被分配至阿替利珠单抗+化疗组(n = 165)或安慰剂+化疗组(n = 168)。数据截止至2020年4月3日,阿替利珠单抗-化疗组的中位随访时间为20.6个月,安慰剂-化疗组为19.8个月。阿替利珠单抗-化疗组和安慰剂-化疗组分别有57.6%和41.1%患者观察到pCR(单侧P = 0.0044[显著性边界,0.0184])。
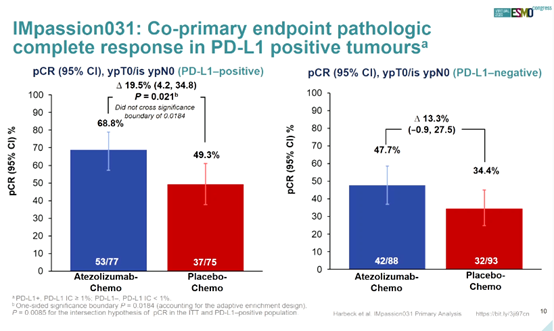
在PD-L1+患者(n = 152)中,两组分别有68.8%和49.3%患者观察到pCR(单侧P = 0.021;不显著)。
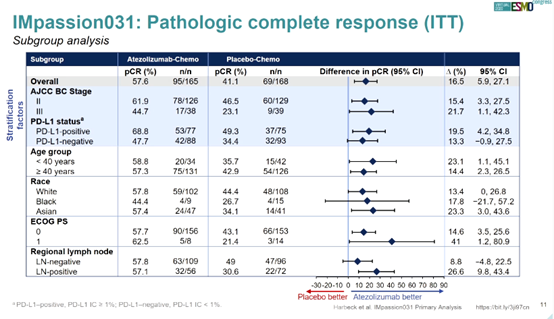
亚组分析结果见下图
ITT人群中,两组的中位EFS(HR=0.76)、中位DFS(HR=0.74)、中位OS(HR=0.69)均未达到。在新辅助治疗阶段,两组分别有22.6%和15.6%患者发生治疗相关严重不良事件,两组各有1例患者发生不相关的5级不良事件。
结论:无论PD-L1表达状态如何,阿替利珠单抗+化疗新辅助治疗为II-III期TNBC患者带来了有临床意义的pCR获益,pCR率提高了16.5%,且具有可接受的安全性。
转移性乳腺癌
FLIPPER研究:帕博西尼+氟维司群一线治疗HR+/HER2-晚期乳腺癌添新证!
背景:PALOMA-2研究证实,帕博西尼联合来曲唑可作为HR+/HER2-转移性乳腺癌的一线标准治疗方案。PALOMA-3研究证实,帕博西尼联合氟维司群可作为内分泌治疗进展后HR+/HER2-转移性乳腺癌的标准治疗方案。FALCON研究显示,氟维司群用于一线治疗时,疗效优于芳香化酶抑制剂。PARSIFAL研究显示,帕博西尼+来曲唑对比帕博西尼+氟维司群用于内分泌敏感转移性乳腺癌时,疗效相当。
帕博西尼联合氟维司群一线治疗是否可改善内分泌敏感晚期乳腺癌患者的临床结局,值得进一步探索。为此,FLIPPER研究纳入绝经后初诊HR+/HER2-转移性乳腺癌或完成≥5年辅助内分泌治疗后复发 > 12个月的患者,探索了帕博西尼+氟维司群用于内分泌敏感转移性乳腺癌一线治疗的疗效和安全性。
方法:这是一项双盲II期研究,患者以1:1比例随机分配至氟维司群(500 mg)/帕博西尼组(F/P)和氟维司群/安慰剂(F/PL)组。分层因素包括:内脏vs非内脏、复发性疾病vs初诊转移性疾病。主要终点为1年PFS率(研究者根据RECIST 1.1评估),次要终点包括中位PFS、OS、客观缓解率(ORR)和安全性等。
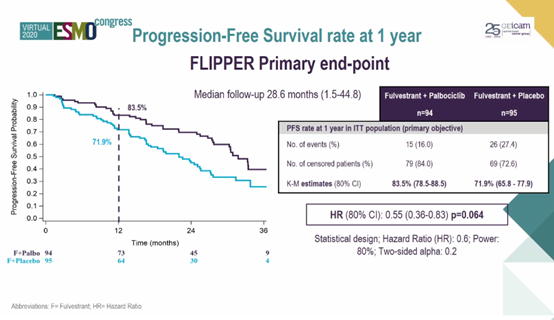
结果:2016年2月至2019年1月期间,入组的189例患者随机分组,F/P组和F/PL组分别有94例和95例患者。中位年龄为64,45.5%患者为初诊转移性患者,60.3%患者累及内脏。研究达到了预设的主要终点:中位随访28.6个月时,F/P和F/PL组1年PFS率分别为83.5%和71.9%(HR=0.55,P=0.064)。
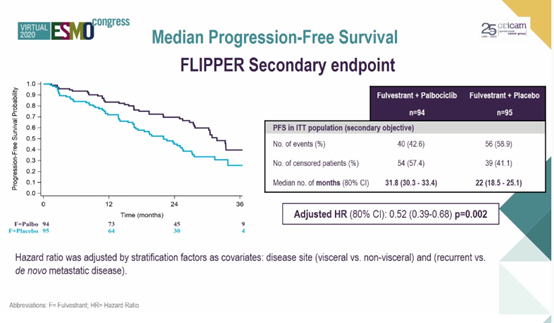
两组的中位PFS分别为31.8个月和22.0个月(HR=0.52,P = 0.002)。
PFS亚组分析结果见下图
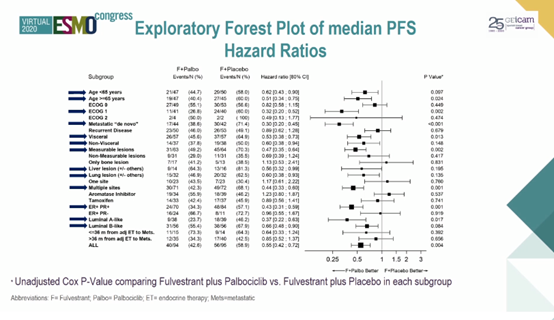
在内脏转移和初诊转移性疾病患者中,氟维司群+帕博西尼联合治疗可带来明显PFS获益。
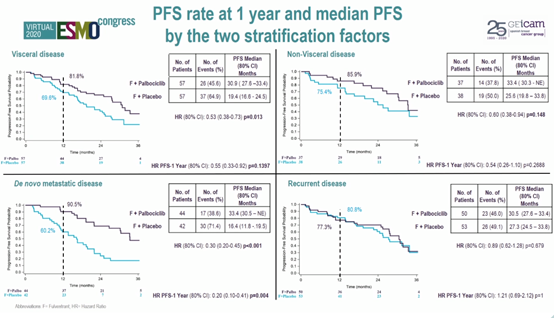
两组的ORR分别为68.3%和42.2%(P = 0.004)。
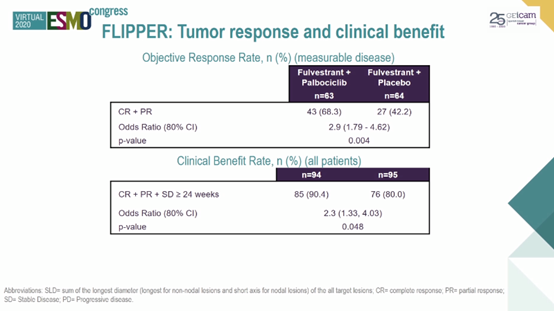
F/P和F/PL组最常见的3/4级非血液学不良事件分别为腹泻(3.2% vs 2.1%)和疲乏(12.8% vs 5.3%)。3/4级血液学不良事件分别为中性粒细胞减少(64.9% vs 0%)、白细胞减少(26.6% vs 0%)和淋巴细胞减少(14.9% vs 2.1%)。未报告发热性中性粒细胞减少病例或治疗相关死亡。OS数据尚未成熟。
结论:与氟维司群+安慰剂相比,氟维司群+帕博西尼一线治疗显著提高了HR+/HER2-内分泌敏感晚期乳腺癌患者的1年PFS率,同时也改善了中位PFS和ORR。
ASCENT研究:新型ADC药物治疗经治mTNBC
背景:在既往接受过治疗的转移性三阴性乳腺癌(mTNBC)患者中,标准治疗化疗的ORR较低,中位PFS较短。SG(TRODELVY™)是一种新型抗体药物偶联物(ADC),由抗Trop-2抗体通过独特可水解连接物与伊立替康的活性代谢产物SN-38(通过连接物允许SN-38在细胞内和肿瘤微环境中释放)偶联组成。I/II期IMMU-132-01研究显示,SG在mTNBC患者中的ORR为33%,中位PFS为5.5个月,且具有可管理的安全性,该研究结果使SG获得美国FDA加速批准用于mTNBC。随后开展了III期ASCENT研究以进一步验证该结果。

方法:在ASCENT研究(NCT02574455)中,既往接受≥2线化疗后出现复发/难治性疾病的mTNBC患者以1:1比例随机分配接受SG(10 mg/kg IV,第1天和第8天,每21天一个周期)或TPC单药治疗(卡培他滨、艾日布林、长春瑞滨或吉西他滨),直至疾病进展或出现不可接受的毒性。主要终点为脑转移阴性人群(BMneg)的PFS。关键次要终点包括OS、ORR和安全性。
结果:在入组的529例患者中,468例为BMneg(中位年龄为54,中位既往治疗线数为4)。与TPC(n = 233)相比,SG(n = 235)显著改善了中位PFS,两组的中位PFS分别为5.6个月和1.7个月(HR=0.41;P < 0.0001)。
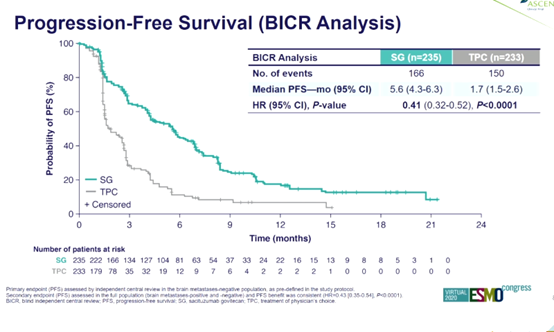
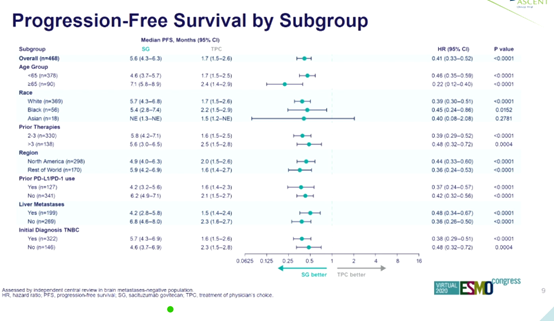
亚组分析显示了与总人群一致的PFS获益。
中位OS也得到显著改善,两组的中位OS分别为12.1个月和6.7个月(HR=0.48;P < 0.0001)。
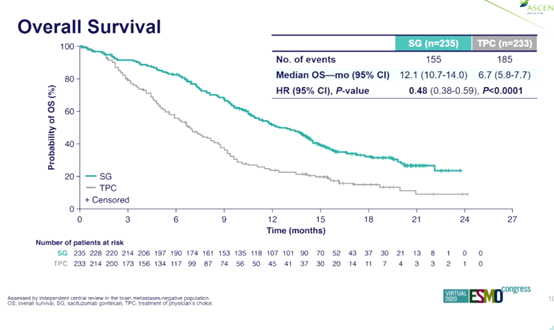
SG的ORR为35%,TPC为5%(P < 0.0001)。两组的临床获益率(CBR)分别为45%和9%(P < 0.0001),两组的中位缓解持续时间(DOR)分别为6.3个月和3.6个月。
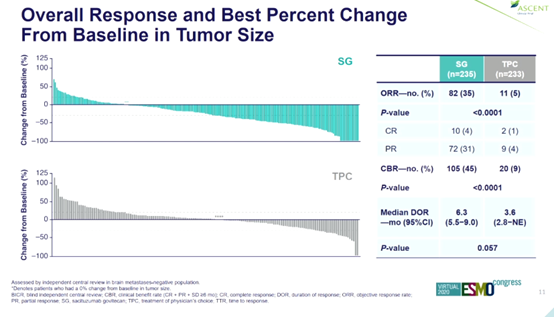
在安全性人群(接受≥1剂研究药物的患者;n = 482)中,SG(n = 258)和TPC(n = 224)的关键治疗相关≥3级不良事件为中性粒细胞减少(51% vs 33%)、腹泻(10.5% vs < 1%)、贫血(8% vs 5%)和发热性中性粒细胞减少(6% vs 2%)。SG组未见> 3级神经病变或间质性肺病,也未见治疗相关死亡事件。
结论:ASCENT研究是关于ADC药物用于经治mTNBC患者的首项III期临床研究,SG对比标准化疗显著改善了PFS和OS。SG或可考虑作为经治mTNBC患者的新治疗选择。
nextMONARCH研究:阿贝西利+内分泌治疗显著改善经治HR+/HER2-乳腺癌OS!
背景:HR+/HER2-转移性乳腺癌约占转移性乳腺癌的70%。CDK4/6抑制剂+内分泌治疗(ET)已逐渐成为HR+/HER2-转移性乳腺癌的标准方案之一。阿贝西利(Abemaciclib)是一种口服、连续给药的细胞周期蛋白依赖性激酶4/6(CDK 4/6)抑制剂。III期MONARCH2和MONARCH3研究显示,阿贝西利+内分泌治疗可显著改善HR+/HER2-转移性乳腺癌患者的PFS。
nextMONARCH研究初步分析中,PFS和ORR结果显示出阿贝西利在经治HR+/HER2-转移性乳腺癌患者中稳健的单药活性,而联用他莫昔芬后PFS无显著改善。本次大会报告了最终24个月OS结果。
方法:nextMONARCH是一项多中心、随机、开放标签II期研究,旨在评估阿贝西利或联合他莫昔芬用于内分泌治疗和化疗期间或之后疾病进展的经治HR+/HER2-转移性乳腺癌的疗效和安全性。患者以1:1:1比例随机分配至阿贝西利(150mg)+ 他莫昔芬(20 mg)组(A+T)或阿贝西利(150 mg)组(A-150)或阿贝西利(200 mg)+预防性洛哌丁胺组(A-200)。末例患者入组治疗后24个月时进行最终OS分析。OS是预设的次要终点。
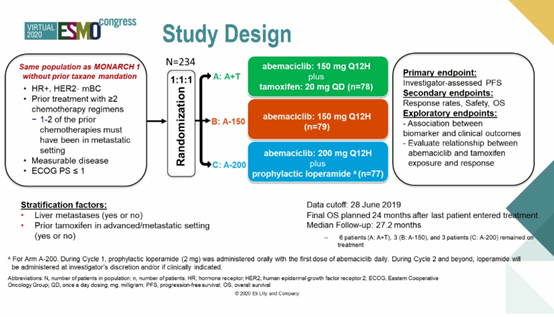
结果:2019年6月28日数据截止日期时,入组的234例患者中有12例仍在接受研究治疗。中位随访时间为27.2个月。A + T组的中位OS为24.2个月,A-150组为20.8个月,A-200组为17.0个月(A + T vs A-150:HR=0.620,P= 0.034;A-150 vs A-200:HR=0.96,P= 0.832)。
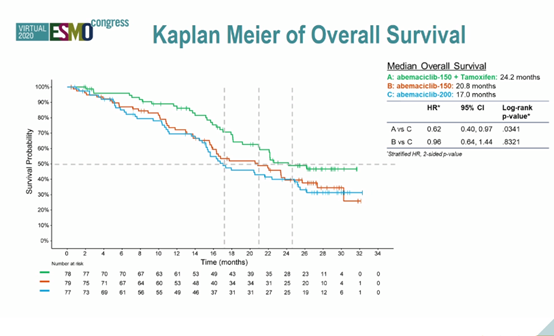
OS亚组分析结果见下图
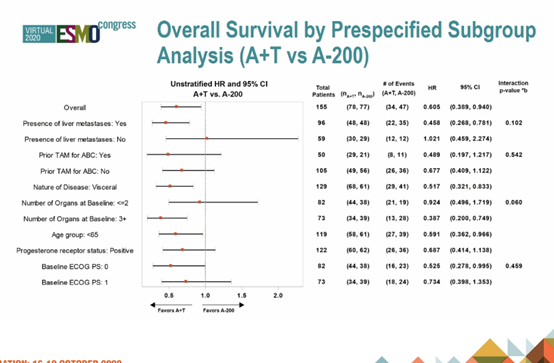
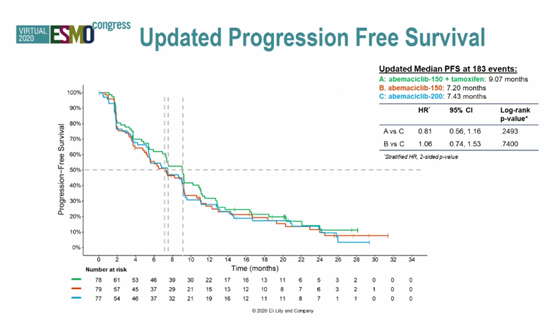
24个月分析时,PFS更新结果显示,三组的中位PFS分别为9.07个月、7.2个月和7.43个月(A + T vs A-150:HR=0.81,P= 0.249;A-150 vs A-200:HR=1.06,P= 0.74)。
阿贝西利组有≥25%患者发生常见治疗后出现的不良事件(TEAE),包括腹泻(61.1%)、中性粒细胞减少症(49.6%)、贫血(40.6%)、恶心(36.3%)、白细胞减少症(30.8%)、疲乏(29.9%)和腹痛(27.4%)。
结论:与阿贝西利单药相比,阿贝西利+他莫昔芬可显著改善经治HR+/HER2-晚期乳腺癌的OS,PFS结果与初步分析结果一致。未观察到新的不良事件。
参考文献:
1. LBA11 - IMpassion031: Results from a phase III study of neoadjuvant(neoadj) atezolizumab + chemotherapy in early triple-negative breast cancer(TNBC)
2. LBA19 - GEICAM/2014-12(FLIPPER) study: First analysis from a randomized phase II trial of fulvestrant(F)/palbociclib(P) versus(vs) F/placebo(PL) as first-line therapy in postmenopausal women with HR(hormone receptor)+/HER2– endocrine sensitive advanced breast cancer(ABC)
3. LBA17 - ASCENT: A randomized phase III study of sacituzumab govitecan(SG) vs treatment of physician’s choice(TPC) in patients(pts) with previously treated metastatic triple-negative breast cancer(mTNBC)
4. 273O - nextMONARCH: Final overall survival analysis of abemaciclib monotherapy or in combination with tamoxifen in patients with HR+, HER2- metastatic breast cancer