PD-1持续用药优于一年用药; “诺奖风向标”拉斯克奖停发; 2020医保更新又有新消息
抗癌大事件
【2020年ESMO大会结束!超多重要进展全汇总】
2020年9月19日至9月21日,为期3天的2020年欧洲肿瘤内科学会(ESMO)年会圆满结束,众多期待已久的重磅临床研究公布了结果,为2020年及后续的抗癌治疗方案开展迎来了重大更新。
咚咚特别汇总了ESMO会议中重要的八大进展,看看有没有涉及你关注的问题:ESMO汇总: PD-1耐药、四代EGFR、PARP药物, 八大重磅进展
【受新冠疫情影响,“诺奖风向标”拉斯克奖停发】
今年,本应在9月初公布的拉斯克奖宣布停发,而停发原因根据其官方位点称,是由于美国以及全球的新冠肺炎疫情大流行。
拉斯克奖是医学领域最为重磅的奖项,加之它通常在诺贝尔奖前近一个月颁发,在医学届被称为“诺贝尔奖风向标”。我国科学家屠呦呦于2011荣获拉斯克奖,2015年荣获诺贝尔奖。
【研究者们发现:高强度运动更有利于健康!】
近日,在著名医学期刊《自然·医学》杂志上,发表了一篇关于人类运动量与死亡风险的数据研究。
这项数据共纳入超过10万人,结果显示:任何强度的运动都有益于健康,每天高强度运动相比低强度运动而言(消耗同样的能量),死亡风险降低30%以上。也就是说,在运动过程中,高强度运动占比越多,我们就越健康。
【2020国家医保目录更新初审药物通过清单发布!数个重磅抗癌药名列其中】
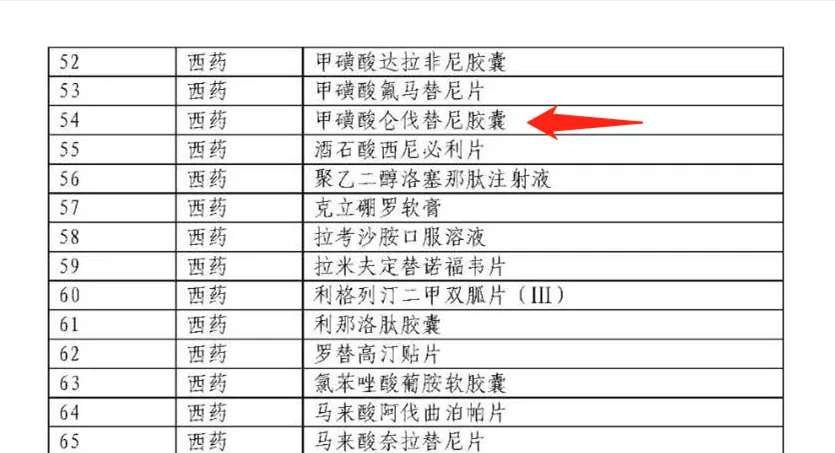
2020年9月18日,国家医保局正式发布《2020年国家医保药品目录调整通过形式审查的申报药品名单》目录,意味着一批新的抗癌药物即将开启2020年医保谈判。
值得注意的是,数个重磅靶向药物(如仑伐替尼等)及数个PD-1、PD-L1药物均名列其中。
癌讯新前沿
【双效分子“D18”增强PD-1抗体疗效】
为了增强PD-1抗体的治疗效果,研究者一直在尝试各种组合疗法。近日发表在《科学·转化医学》上的一项研究发现一种小分子药物D18能够增强PD-1抗肿瘤效果[1]。
研究者分析了对PD-1抗体响应和不响应的黑色素瘤患者肿瘤的基因表达谱,发现高表达KDM5A(一种组蛋白去甲基化酶)的患者具有更好的PD-1抗体疗效。进一步他们还筛选出能够同时增强KDM5A和TLR(一种天然免疫受体)活性的小分子D18,在多种小鼠肿瘤模型中增强PD-1抗体的疗效。
【PD-1免疫检查点抑制剂持续用药优于一年用药】
近年来,免疫治疗特别是PD-1/PD-L1抑制剂取得了突飞猛进的发展,但是免疫治疗十分昂贵,很多家庭无法持续负担相关的费用。能不能缩短免疫治疗时间,这也是一直以来医生和患者都想问的问题。
JCO杂志上一项Checkmate153研究[2]共招募了1428例晚期非小细胞肺癌患者,并应用nivolumab治疗。其中,有252名被随机分配为持续治疗(n=127)和1年固定时间治疗(n=125)。
随访13.5个月后,研究结果显示,持续治疗组比1年固定时间治疗组无进展生存期人群的中位数较长(24.7个月vs9.4个月),持续治疗患者的总体生存期更长。通过该研究发现,持续使用nivolumab超过1年可以改善预后。
【免疫学评分可以更精准预测结肠癌患者的疾病进展风险】
近年来的研究发现, 肿瘤内免疫细胞浸润,可以作为很好的参考指标用于提示结直肠癌的发展规律, 因而被视为潜在的预后指标。免疫学评分测试原理就是通过免疫组化量化测定肿瘤和浸润边缘的总T细胞(CD3+)和细胞毒性T细胞(CD8+)的分布密度,并换算成患者的免疫学评分。
近期一项研究发现,在第1组(加拿大/美国)和第2组(欧洲/亚洲)的763名患者中,免疫学评分越高,复发风险越低[3]。低、中、高免疫学评分患者3年无复发率分别为56.9%、65.9%和76.4%。
这项研究表明,免疫学评分高与III期结肠癌患者的生存期延长显著相关。同时,免疫学评分可进一步提升预后评估,就复发风险而言,免疫评分高的患者从化疗中获益最多。
【有了干扰素信号,PD-1/CTLA-4疗法对黑色素瘤才有效】
近日,在《癌症细胞》上发表了的一项利用测序技术对黑色素瘤患者的肿瘤细胞及免疫检查点抑制疗法效果的研究[4]。这项研究将101名黑色素瘤患者分为未接受治疗组以及接受PD-1或PD-1/CTLA-4联合治疗组,并将他们的肿瘤细胞的转录组进行测序分析。
测序结果显示有了T细胞对肿瘤的浸润以及干扰素信号,患者对于PD-1或PD-1/CTLA-4联合治疗表现出很好的临床反应。因此,T细胞的抗肿瘤活性以及肿瘤细胞内干扰素信号的活跃度是免疫检查点抑制疗法效果好坏的决定性因素。
【肿瘤周围的胶原为癌症治疗的PD-1/PD-L1疗法增加阻碍】
肿瘤细胞外基质常常与抗药性与免疫抑制的现象有关。近日,一项针对肺癌中胶原含量与PD-1/PD-L1抑制效果关系的研究发表在《自然通讯》杂志上[5]。
这项研究发现在小鼠和人的肺癌细胞周围,胶原水平的上升与总体CD8 T细胞数量的下降、耗竭CD8 T细胞数量的上升成正相关。当把肿瘤周围的胶原含量降低后,T细胞对肿瘤的浸润增加,耗竭T细胞的数量减少,肿瘤对于PD-L1的抗性也消失了。这个研究告诉我们,胶原也可以作为降低免疫治疗抗性的潜在靶点。
【新证据:PD-L1阴性的肺癌患者,依然受益于免疫治疗】
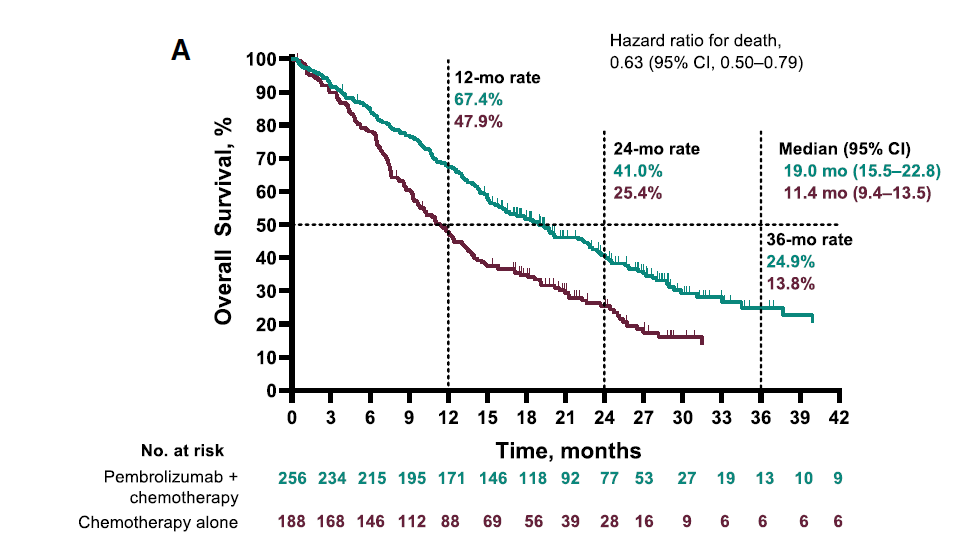
目前,免疫治疗+化疗已经成为非小细胞肺癌一线治疗的标准方案,包括PD-L1阳性和阴性的患者。研究人员汇总了KEYNOTE-021、KEYNOTE-189和KEYNOTE-407三个重要临床试验中PD-L1表达阴性(小于1%)患者的临床数据[6]:一共444位患者,256位接受K药+化疗的联合治疗方案,188位接受单独化疗。
数据分析显示:联合治疗组的中位总生存期是19.0月,而单独化疗组只有11.4月,联合治疗降低了37%的死亡风险。
参考文献:
[1]. Wang, L. et al. Enhancing KDM5A and TLR activity improves the response toimmune checkpoint blockade. Sci TranslMed 12,doi:10.1126/scitranslmed.aax2282(2020).
[2]. Waterhouse, D. M. et al. Continuous Versus 1-YearFixed-Duration Nivolumab in Previously Treated Advanced Non-Small-Cell LungCancer: CheckMate 153. J Clin Oncol,JCO2000131, doi:10.1200/JCO.20.00131(2020).
[3]. Mlecnik, B. et al. Multicenter InternationalSociety for Immunotherapy of Cancer Study of the Consensus Immunoscore for thePrediction of Survival and Response to Chemotherapy in Stage III Colon Cancer. J Clin Oncol, JCO1903205, doi:10.1200/JCO.19.03205(2020).
[4]. Grasso, C. S. et al. Conserved Interferon-γ SignalingDrives Clinical Response to Immune Checkpoint Blockade Therapy in Melanoma. Cancer Cell,doi:10.1016/j.ccell.2020.08.005(2020).
[5]. Peng, D. H. et al. Collagen promotes anti-PD-1/PD-L1resistance in cancer through LAIR1-dependent CD8+ T cell exhaustion. Nature Communications 11, doi:10.1038/s41467-020-18298-8(2020).
[6]. Hossein Borghaei, et al. Pembrolizumab PlusChemotherapy Versus Chemotherapy Alone in Patients With Advanced Non–Small CellLung Cancer Without Tumor PD-L1 Expression: A Pooled Analysis of 3 RandomizedControlled Trials. Cancer. DOI: 10.1002/cncr.33142