肿瘤免疫治疗的十大挑战
近年来,肿瘤免疫治疗(CIT)的治疗进展迅速,反映出人体免疫系统与肿瘤相互作用的重要性。尽管CIT在广泛的人类肿瘤中得到了成功的应用,但只有少数晚期肿瘤患者通过这些治疗得到了持久的免疫应答和生存。发表在今年Immunity上的一篇文章,列举了目前CIT面临的十大挑战。应对这些挑战需要基础科研人员和临床医师的共同努力,加速了解肿瘤与免疫系统之间的复杂关系,从而为肿瘤患者开发更好的治疗方案。
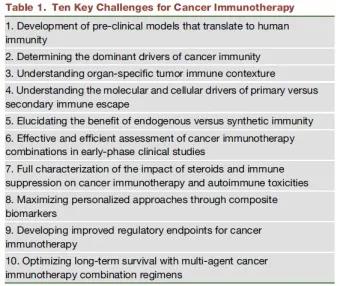
挑战一 转化为人体免疫的临床前模型的研发
临床前常用模型的一个问题是这些模型依赖于癌细胞系的植入。植入后生长的肿瘤通常不能重现影响人体肿瘤免疫反应的肿瘤免疫背景特征。最常用的临床前模型为皮下移植物,不能反映在复杂组织和/或器官特定环境中肿瘤的发生和发展,也会影响干预后对肿瘤的免疫反应。传统的基因工程小鼠模型通过敲除抑癌基因或使用Cre-LoxP系统诱导体细胞突变,从而导致新发肿瘤。这种肿瘤诱导方法不能模拟人类肿瘤进化过程中突变的连续累积,这种模型代表了冷免疫和基因稳定的肿瘤,通常对CIT没有很好的应答。目前正在进一步完善临床前模型,包括人性化小鼠模型、基因重组小鼠模型,以改善来源于人类肿瘤干细胞前体的肿瘤、类器官和乳腺癌的免疫原性。体外人体肿瘤外植体模型对CIT尤其具有吸引力,因为它们可以通过免疫染色和实时成像的结合来观察肿瘤与免疫细胞的相互作用。
另外的挑战来自于免疫系统本身的复杂性,它依赖于肿瘤微环境(TME)中众多不同的细胞类型来发挥功能,因而不能在单一细胞类型中轻易复制。其中一些复杂性反映在免疫浸润中,人体肿瘤可以排列在肿瘤免疫连续体上,并根据免疫细胞相对于肿瘤的空间定位和间质区分划分为炎性、免疫沙漠型或免疫排斥型。
炎性肿瘤中免疫细胞密切贴近肿瘤细胞,免疫排斥型肿瘤中免疫细胞嵌入周围肿瘤间质、远离肿瘤细胞,免疫沙漠型肿瘤无肿瘤浸润淋巴细胞(TILs)。反向转化,是从临床研究中获取科学见解并将其应用到临床前模型中,这有助于进一步描述存在的一些特殊缺陷。它致力于开发更多转化模型,如果成功的话,可以提高该领域对新药及其靶点生物学基础的理解,应用这些模型可能有助于潜在地帮助避免3期临床试验的失败。
挑战二 肿瘤免疫的主动驱导
肿瘤细胞或肿瘤浸润免疫细胞上PD-L1高表达,和/或高比例TIL的肿瘤,被定义为炎性(inflamed)肿瘤。除PD-L1以外的炎性肿瘤的生物标志物,包括IFN&γ;信号、B细胞和由MSI或高肿瘤突变负荷(TMB)定义的基因组不稳定性(图1)。
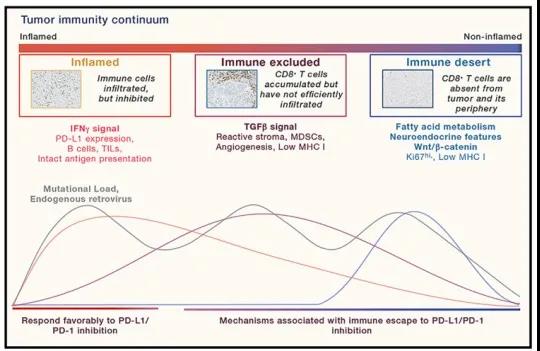
免疫排斥型肿瘤是指有免疫抑制TME的肿瘤,其表现为明显嵌入肿瘤基质微环境中的T细胞,具有高TGF&β;信号、髓样炎症和血管生成。该类肿瘤往往对CPI反应不佳。反向转化研究已经证明了TGF&β;信号通路在促进排斥表型中的重要作用,抑制TGF&β;信号通路可导致表型转换为对临床前EMT6乳腺癌模型中aPDL1+aTGF&β;的联合反应有利的炎性肿瘤。与细胞因子(如IL-8和IL-6)在TME中的高表达相关的髓系炎症在感染性和免疫排斥性肿瘤中也普遍存在。单细胞RNA测序技术的进步将进一步帮助阐明人类肿瘤髓系细胞群体的表型描述,帮助更好地识别旨在解决这些细胞介导的免疫抑制的组合。
免疫沙漠型肿瘤在组织学上表现为缺乏免疫浸润、抗原呈递(低级别MHC-I)的肿瘤和高肿瘤细胞增殖,如儿童恶性肿瘤、激素受体阳性乳腺癌、前列腺癌、胶质母细胞瘤和小细胞肺癌(SCLC)。除SCLC外,这些疾病在基因组稳定,TMB较低,对单药治疗CPI反应不佳。免疫沙漠表型与多种不同的机制有关。包括WNT/&β;-catenin信号、TIL减少、PI3K-AKT/FGFR3信号突变等。
在图2中,我们展示并大致分类了每种肿瘤中的大致表型发生率,并将其置于肿瘤免疫连续体中,因为它们与TMB相关。
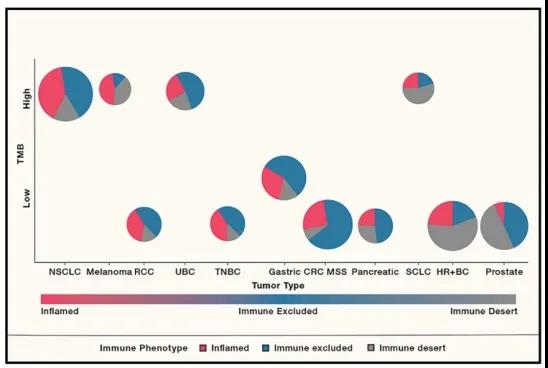
总体的临床挑战仍然是确定炎性肿瘤或高抗原负荷肿瘤的阈值,以及确定与特定表型相关的特异性驱动因素。炎性肿瘤TMB的临界值可能与非炎性肿瘤中TMB的临界值不同。联合疗法的临床转化需要确定合适的患者群体,以将沙漠型或排斥型肿瘤转化为炎性肿瘤。采用除(IHC)CD8检测外的复杂生物标记(如TGF&β;、髓系生物学或WNT/&β;-catenin或改变的肿瘤代谢)有可能开发新的基因标签。
挑战三 了解器官特异性肿瘤免疫环境
促进肿瘤生长的主导力量包括肿瘤细胞的内在特性和肿瘤所在的器官。在转移性尿路上皮癌中,转移到肝脏的肿瘤更有可能对治疗耐药,而转移到淋巴结的肿瘤更可能对CPI产生完全应答。因此,部位是与抗肿瘤免疫应答相关方式的一个重要组成部分。
在肿瘤免疫学中,特别是与抗肿瘤反应相关,需要更多地考虑不同组织中的免疫组分和要素。例如,肝脏通过各种机制与诱导免疫耐受有关。髓源性抑制细胞、Kupffer细胞和肝树突状细胞主要促进活化的免疫抑制通路网络,抑制CD8+和CD4+效应T细胞的激活。对肝转移的反应证明了这些耐受性机制在肿瘤中的相关性。有肝转移的黑色素瘤或NSCLC患者对pembrolizumab的应答降低,无进展生存期(PFS)较短,这与边缘CD8+T细胞浸润减少有关,导致免疫系统无法有效迁移到癌细胞、识别癌细胞和杀伤癌细胞。肝脏也是一个高度血管化的器官,由MDSCs和肝星状细胞构成肝脏的结构。这些与肝脏中的癌相关成纤维细胞一起,为常驻T细胞有效激活并杀死肿瘤细胞提供了一个高阈值。
肝细胞癌是通过由丙型肝炎或乙型肝炎感染导致肝硬化,引起慢性肝病的一种疾病,联合血管内皮生长因子(VEGF)靶向治疗,目前已显示出对CPI的良好反应。VEGF-靶向治疗在逆转不可切除的肾细胞癌中的髓系炎症中的作用,除了使肿瘤血管系统正常化外,还假设有与这些疗法可以产生协同。这些联合疗法是否能有效治疗其他部位肿瘤的肝转移,还有待观察。
目前的临床治疗模式通常不包括器官特异性治疗方法。器官特异性免疫不局限于肝脏。抗肿瘤免疫应答在骨微环境中也特别有限,可能是由于独特的基质相互作用(如胶原蛋白)、存在的细胞因子(如TGF&β;)和MDSC的增加。此外,淋巴结、肺和皮肤等部位通常可能是更有利的抗肿瘤免疫部位,这可能是由于这些特定器官中存在相对较高的免疫细胞。最近的数据显示可以采取器官特异性治疗方法,并且联合治疗的其他研究可以阐明免疫机制匹配治疗患者的具体益处。
挑战四 了解原发和继发免疫逃逸的分子和细胞驱动因素
临床上很大一部分患者对CPI治疗没有反应,而一些临床应答多年的患者最终仍可能经历肿瘤的进展。前者被称为“原发性免疫逃逸”,后者被称为“继发性免疫逃逸”。虽然这两种不同的免疫逃逸所涉及的机制可以重叠,但它们不会在时间上重叠。免疫逃逸的机制可能与特定的免疫表型有关。炎性的低TMB肿瘤预先存在免疫应答,但往往因为存在髓系炎症而免疫抑制从而对单药CPI反应不佳。联合靶向VEGF以克服髓系介导的免疫抑制似乎是合乎逻辑的。炎性高TMB NSCLC肿瘤中HLA位点杂合子丢失,新抗原转录物的表观遗传抑制;MSI-H的结直肠癌Wnt-&β;-catenin信号的激活与免疫逃逸有关。
研究继发性逃逸的驱动因素更具挑战性,主要是由于在治疗开始前和治疗进展过程中缺乏系统的肿瘤组织收集。肿瘤可诱导抗原呈递机制中的基因变化,包括JAK-STAT信号的突变、&β;2微球蛋白的丢失、MHC表达的下调、免疫原性突变的丢失或抗原丢失,以克服免疫压力。
原发性免疫逃逸更容易从已存在的肿瘤标本中进行研究,并可能使这些机制更依赖于受累器官和肿瘤发生的细胞类型的生物学特性,例如胃肠道恶性肿瘤的免疫排斥。与继发性免疫逃逸不同,后者可能在免疫治疗有效后较短时间内出现,它的机制可能更多地与所使用的特定类型CIT有关,就像CD19定向CAR T治疗的情况一样。
挑战五 阐明内源性免疫与合成免疫的益处
PD-L1/PD-1抑制剂的发展使许多患者产生了高效的内源性抗肿瘤免疫应答,以消除癌细胞。这种内源性免疫反应很大程度上依赖于先前启动的CD8+T细胞,这些细胞能特异性识别癌细胞。通过抑制PD-L1/PD-1,这些免疫细胞可以被重新激活或扩增,从而识别和杀死癌细胞。
然而,并不是所有的肿瘤都具有内源性T细胞能够有效识别的适当的免疫原性抗原。合成免疫是人工地将T细胞与癌细胞结合的治疗方法,这种结合通常是基于T细胞受体与特定肽-MHC复合物的同源结合而产生的(图3)。CAR-T细胞是从病人身上分离出来的基因修饰T细胞,将一个人工结合区域引入到肿瘤相关抗原上,该抗原通常与TCR信号蛋白和T细胞共刺激蛋白相连接,然后再注入到肿瘤患者体内。
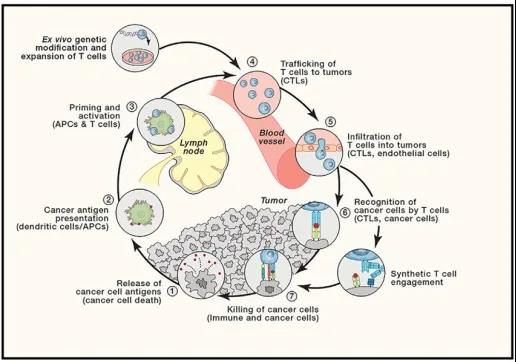
合成免疫促进肿瘤常驻和非特异性T细胞进入肿瘤的增殖。对免疫原性差的肿瘤,合成免疫产生初始的抗肿瘤免疫反应,刺激细胞因子上调,导致免疫原性癌细胞死亡,进一步激活内源性抗肿瘤免疫反应。抑制PD-L1/PD-1可减轻PD-L1对T细胞功能的任何免疫抑制作用,进一步增强合成免疫应答。
在免疫排斥和免疫沙漠型肿瘤中驱动免疫抑制的因素尚不完全清楚,并且缺乏能够在这些肿瘤患者中产生有效内源性免疫的免疫疗法。许多炎性肿瘤也存在多因子免疫抑制。将T细胞与癌细胞结合的合成疗法不仅可导致非内源性T细胞与癌细胞的结合,还可导致强有力的T细胞激活信号,从而产生强大的细胞毒性免疫反应,潜在地克服和/或压倒可能存在的免疫抑制。
将内源性免疫和合成免疫结合起来可能特别具有协同作用。在单药内源性免疫或合成免疫能治愈的情况下,可能不需要联合治疗。如高PD-L1和高TMB患者的PD-L1/PD-1靶向治疗或某些表达CD19的血液恶性肿瘤的CAR T疗法。然而,大多数肿瘤既没有表现出足够强的内源性免疫反应来根除肿瘤,也没有足够敏感的合成免疫来达到治疗效果。当一种肿瘤存在肿瘤相关抗原可以通过合成免疫方法靶向,并且存在、或可以产生内源性抗癌免疫反应,那么就出现了这两个治疗领域的交集。在这个交集上确定合成免疫和内源性免疫疗法的理想组合还需要进一步的研究。
挑战六 早期临床研究中肿瘤免疫治疗组合的有效性和高效性评估
临床上有超过1000种CIT组合,因此迫切需要尽早评估这些组合。鉴于抗肿瘤免疫涉及多个步骤,通过同时或序贯调节免疫中的不同生物步骤,合理组合以提高CIT疗效的潜力是非常广阔的。然而,令人生畏的生物学复杂性和组合的可能性,与尽快为患者提供最有效的免疫治疗的需求相悖。改善临床前和临床研究的整合,特别是改善临床前模型和/或更好地理解模型在哪里可以很好地转化将极大地有助于在待检测的患者群体匹配组合方法,同时依赖于对联合用药的作用机制的明确理解和临床证明。CIT的治疗,需要而且可能会与任何将纳入此类试验的综合生物标记策略相关联,包括药效学和预测性生物标记。迫切需要利用只有在联合后产生协同(或叠加)作用时才能检测到或改变的生物标记物。
在早期研究中,单药有效率仍然是CIT疗效初步评估的最有用终点。而联合用药,特别是包括至少一种具有单药活性的药物的联合用药,由于病人的异质性,潜在的病人选择偏差,以及缺乏随机化,在I期联合用药研究的评估是非常复杂的。此外,特殊的成像方法可以提供对不同区域、微环境和器官的免疫生物学的深入了解。从免疫学角度讲,组合不应要求每个成分都有单独的反应活性,因为某些组合成分只需能够使肿瘤对第二种组分敏感,例如疫苗与CPI的结合。
挑战七 类固醇和免疫抑制对肿瘤免疫治疗和自身免疫毒性的影响
皮质类固醇对人体免疫有直接作用,对T细胞的影响大于对B细胞的影响,最终导致循环中T细胞总数的减少。皮质类固醇通常用于治疗自身免疫性疾病,治疗移植物抗宿主病,和逆转由检查点抑制引发的自身免疫不良事件或合成免疫方法中的细胞因子释放综合征(CRS)。评估类固醇对抗肿瘤免疫的影响可能需要纳入类固醇的给药时间(如在CIT开始时或之前,对比免疫治疗开始后的几个月甚至数年)。根据目前的临床资料对类固醇对肿瘤免疫影响的最佳评估是,全身性类固醇会削弱我们试图用CIT达到的抗肿瘤免疫效应,然而,这种影响往往不能完全消除抗肿瘤免疫效应。类固醇实际削弱抗肿瘤免疫效果的程度最有可能是由给药时间(早期与晚期)、剂量、疗程和特定类固醇给药(高剂量与低剂量类固醇,连续、与间歇、与单次服用类固醇,以及类固醇的效力)和给药时抗肿瘤免疫应答强度所决定的。
合成免疫治疗与绝大多数内源性免疫反应相比,,如CAR T和T细胞结合抗体会导致高度急性毒性,最常见的表现为CRS。早期识别CRS和积极使用类固醇对预防5级事件很重要。类固醇用于治疗CRS似乎不会明显影响合成免疫所产生的疗效。然而,类固醇的使用与远期结局(如多年的持久生存)之间的关系尚不清楚。虽然了解免疫毒性的机制并优化处理这些毒性的方法是肿瘤免疫治疗学的重要组成部分,一个更重要的挑战是如何开发出更有效和特异的CIT,这些CIT能够在不产生自身免疫或免疫介导毒性的情况下消除肿瘤细胞。
挑战八 通过复合生物标记最优化个体化治疗
CIT的生物标记物开发存在挑战。与靶向治疗不同,靶向治疗通常是靶点自身的基因异常(例如Her2扩增、EGFR突变、ALK易位),后者通常被定义为二元(是或否)检测,CIT中的生物标志物通常面临关联度和连续变量的问题,PD-L1表达、TMB和肿瘤源性IFN&γ;基因标签都是如此,每种在不同适应症都有多个不同的生物标记物临界值。这通常使得在设计临床试验时,预先确定生物标志物的临界值去区分高或低值人群具有挑战。绘制受试者工作特征(ROC)曲线的统计方法可能有用。大型临床试验的设计用以确定生物标志物在3期试验的临界值,并可能有助于为肿瘤患者诊断是否从治疗中获益。对生物标志物假说用统计学的严谨性进行临床试验,即使是回顾性地进行,也可能促进治疗算法的发展。
像PD-L1的IHC检测一样,确保生物标记的一致定义和检测仍将是挑战,使药物开发人员之间的数据能一致性解释。诊断开发商正在研制能够快速转换分子和/或细胞数据的工具,所有这些工具都将使可操作的信息可行且负担得起并对患者有用。越来越多的研究使用具有预先指定分析计划的综合平台,为诊断策略提供信息,从而有可能基于这些终点注册试验,因此,使用算法来定义患者利益并使患者和治疗医生做出基于证据的决策可能成为规范。考虑到有效治疗所需要的相互作用的复杂性,这些方法可能特别适用于CIT。
挑战九 改进肿瘤免疫治疗的调控终点
PD-L1/PD-1抑制剂的传统统计和批准的监管终点是可用的,使许多此类药物能够快速和广泛的评估和批准。然而,这些终点,包括ORR、PFS和OS,并没有被设计或很好地匹配用于CIT的评估。大多数转移性肿瘤患者及其治疗医师的目标是实现CIT的持久疗效和生存率。在检查Kaplan-Meier生存曲线时,最好用“曲线尾部”来衡量这一点。然而,分析动力不足,需要长期随访,通常持续数年使得目前缺乏衡量这一益处的临床试验方法。此外,ORR评估并未考虑有效的CIT会导致延迟反应(例如,肿瘤持续生长后肿瘤退缩)或“假进展”(例如,肿瘤退缩后炎性反应导致看上去像肿瘤生长)。PFS评估同样受到上述因素的影响。因此,为确定和验证更好的CIT终点,已经进行了尝试,包括制定免疫相关反应标准、实体瘤的免疫反应评估标准(iRECIST)、imRECIST和imPFS。OS评估非常适合CIT的评估,尽管它可能需要较长时间才能完成,需要对照组接受治疗的患者死于肿瘤才能进行评估,并且受对照组与免疫治疗的交叉以及给定患者群体受益时间的差异的影响(例如,交叉OS-Kaplan-Meier曲线)。可能解决其中一些问题的其他可能的终点包括使用基于模型的治疗增长率常数估计值来预测OS效益、landmark OS、加权对数秩OS或使用基于Cox模型的时变治疗效果估计得出的OS。
挑战十 通过多药肿瘤免疫联合方案优化长期生存
开发最佳CIT方案可能需要多种疗法来调节产生抗肿瘤免疫反应所需的每个步骤。通过多管齐下的方法,一个完整的治疗方案可能包含能够杀死癌细胞、驱动对数杀伤、减轻肿瘤负担、使肿瘤对免疫治疗敏感、激活内源性抗癌免疫反应、驱动免疫细胞增殖以及提供维持驱动长期记忆反应的药物,从而延长生存曲线的尾部。这种治疗方案可以包括抗PD-L1/PD-1药物以及其他可以去除负性调节因子的药物;激活、激发和/或在没有现有强大免疫反应的患者中产生新的免疫;克服免疫排斥;增加I类MHC分子;增加T细胞存活率;和/或驱动T细胞记忆。此外,一些最强大的抗肿瘤药包括细胞毒性药物(如化疗和放疗),以及合成免疫制剂可以进行联合。这些类型的治疗方案将需要优化药物的剂量、时间(考虑到潜在的瞬时效应)和/或排序,以达到最大的效益。有些药物可能只需要在整个疗程中使用几次,或者在疗程中不经常使用。总的目标是避免重叠毒性,最大限度地发挥协同作用,并将重叠耐药性的可能性降至最低。
为了快速确定优先顺序并加快此类方案的开发,需要新的临床试验方法。这些试验“平台”包括伞式试验,篮子试验等。这些试验设计具有适应性,允许快速将新的组合、剂量和/或时间表添加到试验中,并为患者提供切换组合的灵活性。总的来说,这些临床试验设计可以促进更快和更有信心的决策,也可以使治疗方法连续地加入到一个方案中,或者相反地,连续地解构一个复杂方案的组成部分。适应性临床试验的例子包括BATTLE平台、 I-SPY试验、MORPHEUS和 FRACTION研究、QuEST1研究等。也有可能根据真实世界为临床试验开发合适的“非研究”对照组数据。这些对照组可采用与随机对照试验相同的纳入和排除标准,纳入按标准治疗的患者。
结语
为了推动CIT领域的发展,需要克服这十大挑战。在这一系列挑战中,可能仍需要进一步确定优先次序,一种观点认为可以集中于在1期临床研究中更好地评估CIT组合的重要性。从改进临床前模型,到临床生物标志物和器官特异性免疫。此外,优先考虑合成免疫和内源性免疫之间的关系至关重要的,需要将这些方法最佳地结合起来。
历史上,治疗模式的转变之间有很长的时间间隔,但这些时间间隔一直在缩小(图4A)。今天,CIT领域内有了巨大的发展,主要是利用内源性免疫或合成免疫方法(图4B)进行的孤立的工作。因此,协作方式是必需的,目前包括跨学术机构、政府机构和行业合作伙伴的合作。将CIT领域聚集在一起可以立即和直接解决公开的挑战,如了解二次免疫逃逸这一特定领域,收集和分析肿瘤进展后期的样本是必要的。

这些合作已经成功地促成了CIT对疗效评估、出版指南、不良事件管理和诊断方法的具体评估。随着这一领域在过去几年中不断发展壮大,试图将肿瘤研究的不同部分整合在一起的各种工作也在不断增多。“一致性”,一种知识的统一,但不一定是思维的统一,这个概念特别适合描述现在所需要的: 架起科学家、协作小组和思想的桥梁。激励全球CIT的研究者,不是围绕特定的解决方案,而是围绕我们需要面对、关注和解决的广泛挑战进行努力,很可能对成功开发出 “治愈疗法”大有帮助。