徐建明教授报告索凡替尼治疗晚期胰腺神经内分泌瘤患者的Ⅲ期临床研究 SANET-p研究结果
编者按:胰腺神经内分泌肿瘤(pNET)发病率迅速上升,正逐渐引起医学界关注和重视。基于索凡替尼在神经内分泌瘤患者Ⅰb/Ⅱ期研究的疗效和安全性,和记黄埔医药率先在全球范围内开展了两项针对中国NET患者的Ⅲ期临床研究——SANET-ep和SANET-p。继解放军总医院第五医学中心徐建明教授在2019年ESMO年会上口头汇报SANET-ep研究的主要结果之后,9月20日,以线上形式举行的2020年ESMO年会上,徐教授再登演讲台,口头报告SANET-p研究结果。《肿瘤瞭望》特邀徐建明教授撰文,对该研究进行介绍。
研究背景
神经内分泌肿瘤(NENs)是一类起源于胚胎的神经内分泌细胞、具有神经内分泌标记物和可以产生多肽激素的肿瘤。2012年中国学者回顾分析了1954年至2011年国内发表的所有相关文献,汇总胃肠胰神经内分泌肿瘤共11 671例,pNENs占49.8%(5807例),但pNET发病率迅速上升,正逐渐引起医学界的关注和重视。而且无论是在国内还是全球范围内,对于pNET患者的治疗存在巨大的临床需求,亟需有效的药物造福广大的患者。
研究原理
索凡替尼(Surufatinib)是由和记黄埔医药自主研发的一个全新结构的嘧啶类小分子靶向抗肿瘤新药,能有效抑制VEGFR(1、2、3)、FGFR1和CSF1R活性,从而抑制血管内皮细胞增殖、管腔形成等功能,最终通过抑制肿瘤新生血管的形成而抑制肿瘤生长。
在Ⅰ期剂量递增临床研究中接受索凡替尼治疗的18例疗效可评价的神经内分泌瘤患者中有8例患者达到PR(44.4%),其中在7例疗效可评价的PNET患者中,有3例达到PR(42.9%)。另外在神经内分泌瘤患者中进行的Ⅰb/Ⅱ扩展期研究也出现相似的疗效趋势,显示出索凡替尼在晚期NETs的初步疗效。
在安全性方面,Ⅰa期临床试验数据显示索凡替尼的药物不良反应与同类VEGFR靶向治疗药物相似,未发现新的安全性信息。这些不良反应多为轻到中度,所引起的治疗中断或减量的发生率较低,且经过对症处理均可得到减轻或恢复。
基于索凡替尼在神经内分泌瘤患者Ⅰb/Ⅱ期研究的疗效和安全性,和记黄埔率先在全球范围内开展了两项针对中国NET患者的Ⅲ期临床研究(SANET-ep和SANET-p),其中解放军总医院第五医学中心徐建明教授在2019年ESMO上口头汇报了SANET-ep研究的主要结果,研究结果表明索凡替尼能够显著延长中国晚期非胰腺NET患者的中位PFS(9.2个月 vs. 3.8个月,P<0.0001)。
研究设计
SANET-p研究是一项随机、双盲、安慰剂对照、多中心Ⅲ期临床试验,入组人群为处于疾病进展期、无法手术切除的局部晚期或远处转移的低、中级别(G1或G2)PNET患者。在该研究中,患者以2:1的比例随机接受每天口服一次300 mg索凡替尼或安慰剂治疗,28天为一个治疗周期。
研究的主要终点为研究者评估的无进展生存期(PFS),次要终点包括客观缓解率(ORR)、疾病控制率(DCR)、到达疾病缓解的时间(TTR)、缓解持续时间(DoR)、总生存期(OS)、安全性及耐受性。
研究结果
SANET-p研究中期数据分析截止时(2019年11月11日),共入组172例晚期胰腺NET患者,随机接受索凡替尼(113例)或安慰剂(59例)治疗。两组患者基线特征较为均衡,其中中级别(G2)患者所占比重较大(索凡替尼组占87.6%,安慰剂组占84.7%)。
结果显示,与安慰剂相比,索凡替尼能够显著延长研究者评估的PFS,索凡替尼和安慰剂组分别为10.9个月和3.7个月,风险比(HR)为0.491[95%可信区间(CI)为0.319~0.755],P=0.0011。
支持性分析表明,索凡替尼能够显著延长盲法孤立审查委员会(BIIRC)评估的PFS,索凡替尼和安慰剂组分别为13.9个月和4.6个月,风险比(HR)为0.339[95%可信区间(CI)为0.209~0.549],P<0.0001。
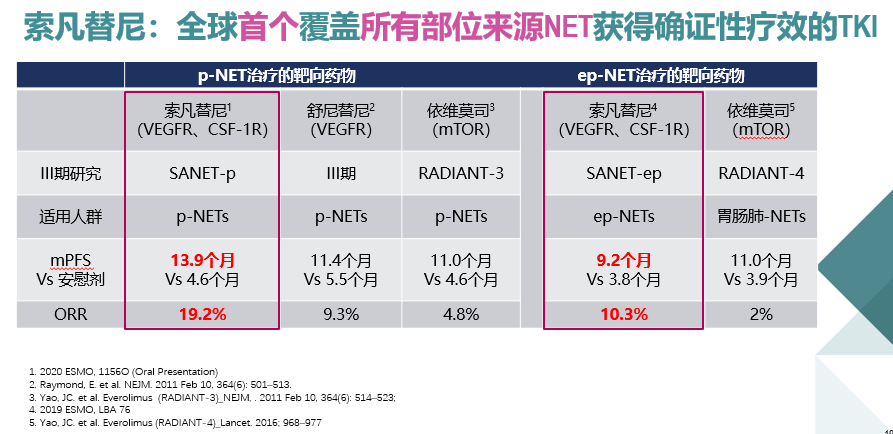
此外,索凡替尼在ORR(19.2% vs. 1.9%)、DCR(80.8% vs. 66.0%)等次要研究终点方面也优于安慰剂组。索凡替尼是迄今为止,pNET治疗的靶向药物中ORR最高(19.2%)的药物,显示出良好的pNET治疗效果。
此项研究中,索凡替尼的安全性和耐受性良好,治疗相关不良事件与既往早期临床研究一致,最常见的不良反应为蛋白尿、高血压、腹泻等。基于预先计划的中期分析中观察到的优效性,IDMC建议提前终止本研究。