NSCLC精准治疗新希望 三代EGFR TKI伏美替尼
编者按:肺癌是我国发病人群最多的癌种,受到社会各界的极大关注,也是CSCO 2020年会的重要讨论话题。随着精准治疗不断的深入,针对NSCLC的第三代EGFR TKI 甲磺酸伏美替尼历经Ⅰ期剂量爬坡研究、Ⅱa期剂量拓展研究和Ⅱb期关键注册临床研究,取得一系列良好成果并即将上市,其与吉非替尼头对头对比的一线用药III期研究正在进行,将为国内NSCLC患者带来新的希望。CSCO 2020年会之际,在石远凯教授的主持下,韩宝惠教授、刘晓晴教授回顾EGFR阳性NSCLC治疗史,关注甲磺酸伏美替尼这颗冉冉升起的新星,王孟昭教授、杨农教授、史美褀教授、刘安文教授展开深入讨论,探索更多可能。
开篇

甲磺酸伏美替尼是上海艾力斯医药科技股份有限公司研发的第三代EGFR TKI。自2016年进入临床研究以来,已完成了Ⅰ期、Ⅱa期、Ⅱb期相关研究,两项Ⅱ期临床研究的综合分析也于本次CSCO会议上公布,甲磺酸伏美替尼对总体患者的ORR达74.7%,DCR达92.8%,mPFS为9.6个月,显示了药物良好的疗效和安全性。其与吉非替尼头对头比较的一线治疗NSCLC的临床研究也已入组完毕,正在治疗和随访当中。本次会议将重点介绍甲磺酸伏美替尼相关临床研究的重要结果,提高对三代EGFR TKI的全面认识,为未来药物的合理应用打下基础。现下,甲磺酸伏美替尼已经进入了国家药监局药品审评中心上市前的审评程序,希望尽快上市,造福中国的肺癌患者。
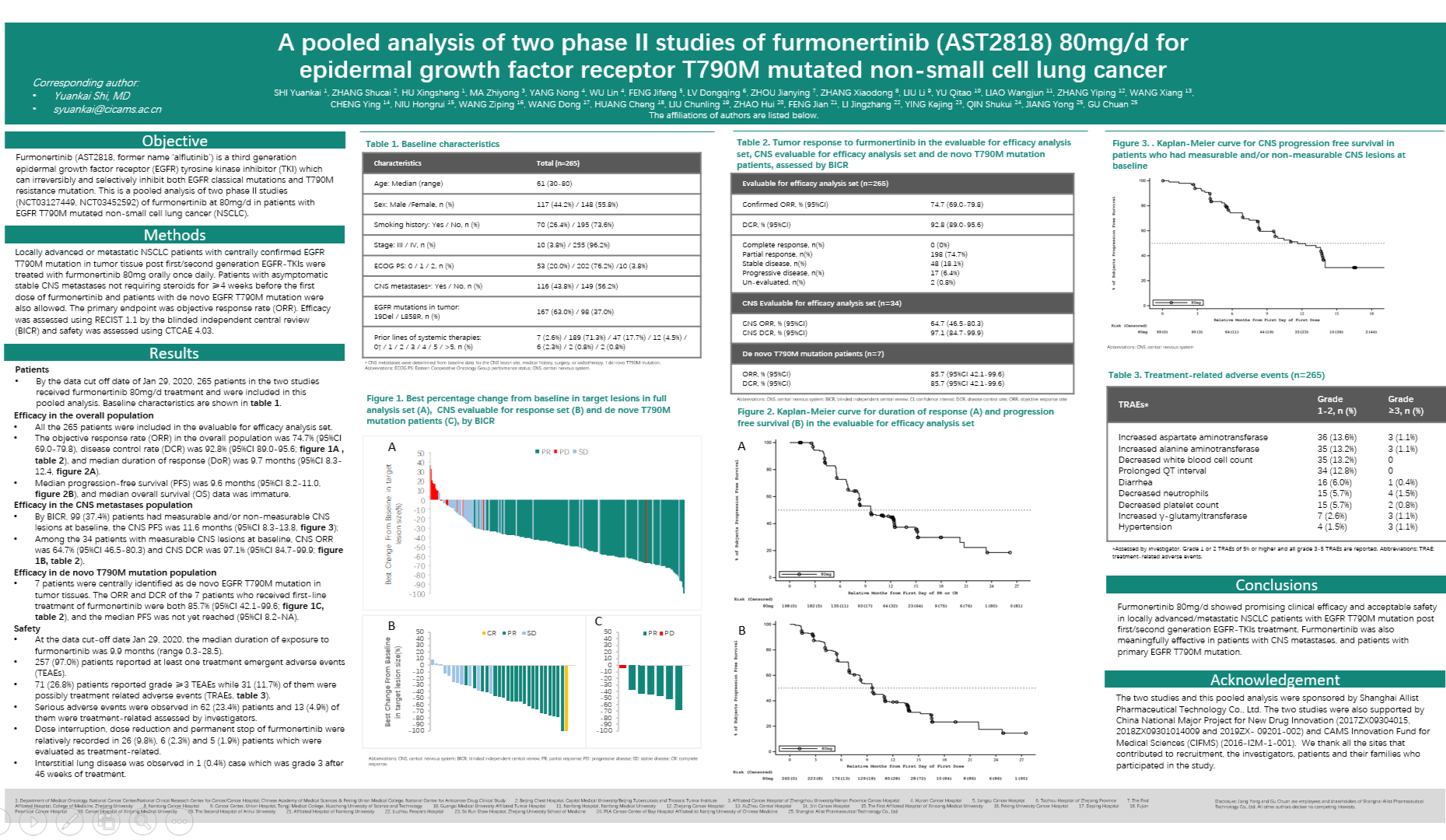
甲磺酸伏美替尼——三代EGFR TKI治疗的新选择

EGFR突变是中国NSCLC的主要驱动因素,约有近一半患者伴随EGFR突变。甲磺酸伏美替尼正是针对EGFR突变的三代TKI,具有创新的以三氟乙氧基吡啶为基础的结构,无论是药物原型AST2818还是主要代谢产物AST5902,均可通过不饱和丙烯酰胺键与EGFR不可逆结合,具有双活性,可以强效抑制EGFR敏感突变和耐药突变。同时,三氟乙氧基吡啶结构可以阻断非选择性代谢产物的产生,药物分子具备的空间位阻效应也能提高激酶谱选择性,降低脱靶效应,提高安全性。体外药效试验对此进行了充分的证实,动物研究也显示了甲磺酸伏美替尼对EGFR敏感突变和T790M耐药突变的肿瘤具有强抑制效应。
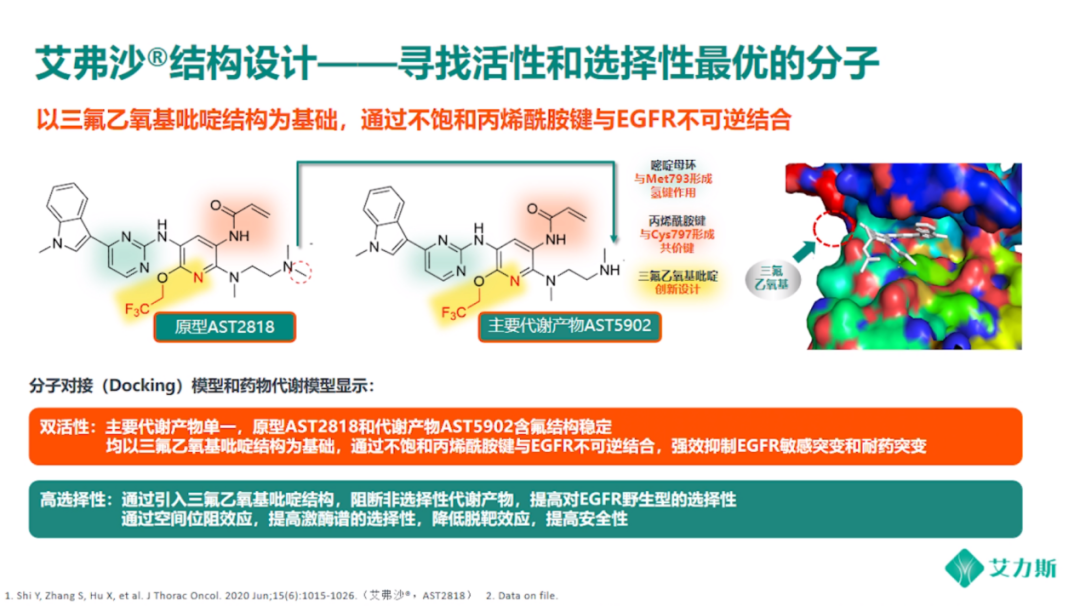
自2016年开始,甲磺酸伏美替尼开始了在NSCLC治疗的探索,在其关键临床研究设计中,纳入了ECOG 2分的患者,L858R突变、CNS转移的患者比例相对较高。其Ⅰ期剂量递增试验显示,患者用药剂量达到240mg/d时仍未观察到剂量限制毒性,且未获得最大耐受剂量,显示了良好的安全性。Ⅱa期剂量扩展研究剂量达到80mg即可取得很好的疗效,ORR达77.8%,原发T790M突变ORR可达100%,总体人群PFS为11.1个月。Ⅱb期研究以80mg/d做进一步延伸,今年ASCO公布的结果显示对T790M突变患者ORR可达74.1%,DCR 93.6%,PFS 9.6个月;并且可以有效控制CNS转移,CNS ORR 65.5%,CNS DCR 100%,CNS PFS 长达11.6个月。除了良好的效果,已经开展的Ⅰ期、Ⅱa期、Ⅱb期研究中,所有研究剂量组3级及以上药物相关不良反应约10%左右,而80mg/d剂量组各项3级及以上药物相关不良反应均小于1.5%,安全性极佳。
综上可见,甲磺酸伏美替尼作为中国原创的第三代EGFR-TKI,机制上具有双活性、高选择的特点,并且目前研究也证实了其强抑瘤,安全佳的优势,有望成为三代EGFR TKI的全新选择。
精准治疗时代EGFR突变阳性NSCLC的历史回顾

进入21世纪后,随着分子靶向治疗的发展,对肺癌的分子分型逐步清晰,现行的NCCN指南中已经详细的规定了在病理分型的基础上,根据患者基因突变类型或免疫标志物选择相应的精准治疗手段。实际上,早在1997年,研究者就已经发现了EGFR突变的潜在作用,直至2009年IPASS研究证实了一代EGFR TKI吉非替尼的疗效,才真正开创了肺癌靶向精准治疗时代,此后EGFR TKI蓬勃发展。
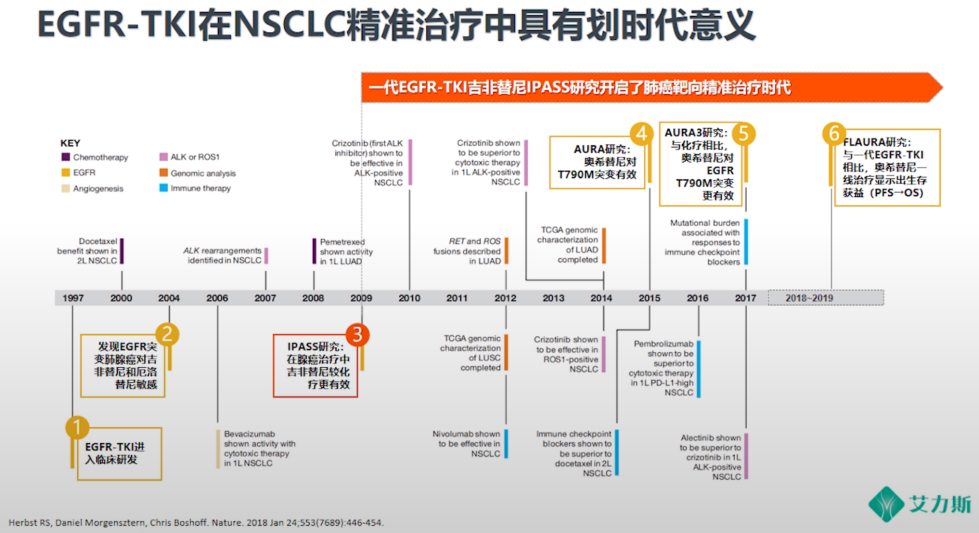
相较于欧美人群,EGFR突变是中国肺癌最常见的驱动基因,几乎占到一半,所以EGFR TKI的探索与应用至关重要。在精准治疗时代以前,对于未筛选的肺癌患者,一代EGFR TKI获益有限,PFS仅3个月左右;随着EGFR突变人群筛选的应用,精准治疗时代真正开启,一代EGFR TKI对此类人群的PFS获益提高到接近1年。
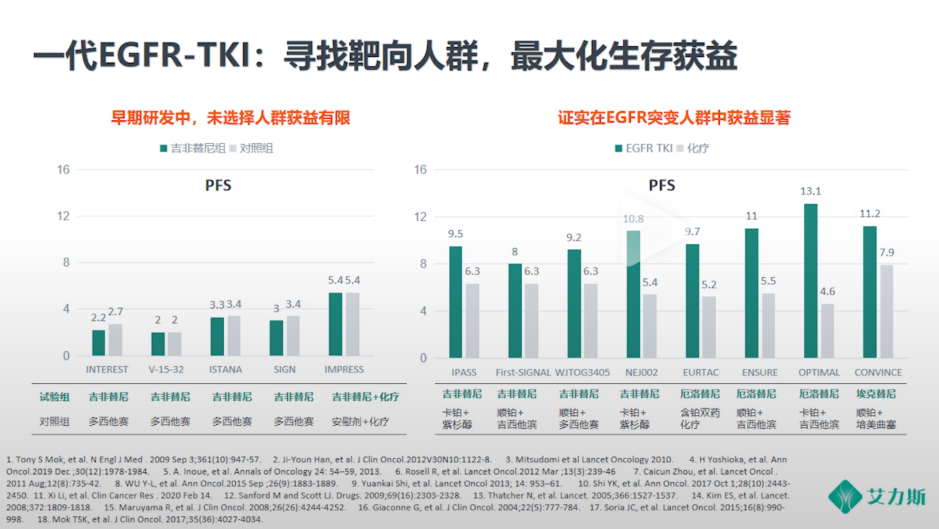
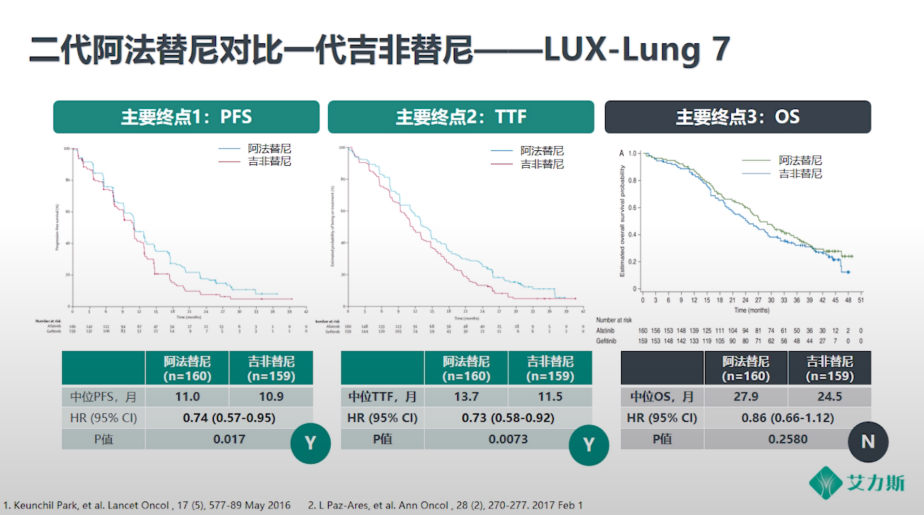
由于T790M突变造成一代EGFR TKI耐药,所以二代EGFR TKI引入了丙烯酰胺键,通过共价键与EGFR不可逆结合,相应的对T790M的抑制作用增强,但选择性较差,因此限制了其应用。LUX-Lung7研究显示,对于EGFR阳性患者,阿法替尼较吉非替尼延长了患者的mPFS(11.0个月vs 10.9个月)、mTTF(13.7个月 vs 11.5个月),但延长的绝对值有限,且OS无显著差异。ARCHER 1050研究则对另一个二代EGFR TKI达克替尼进行了探索,相较于吉非替尼,达克替尼的mPFS(14.7个月 vs 9.2个月)、OS(34.1个月 vs 27.0个月)有显著改善,然而该研究方案规定了固定次序的检验策略,OS前序终点ORR无统计学差异,所以不能认为OS具备正式的统计学意义。在二代EGFR TKI疗效改善并不明显的同时,其不良反应有明显的增加,因不良反应导致的减量更是近乎一半,并且未能有效解决耐药问题,T790M突变耐药的占比依然很高。
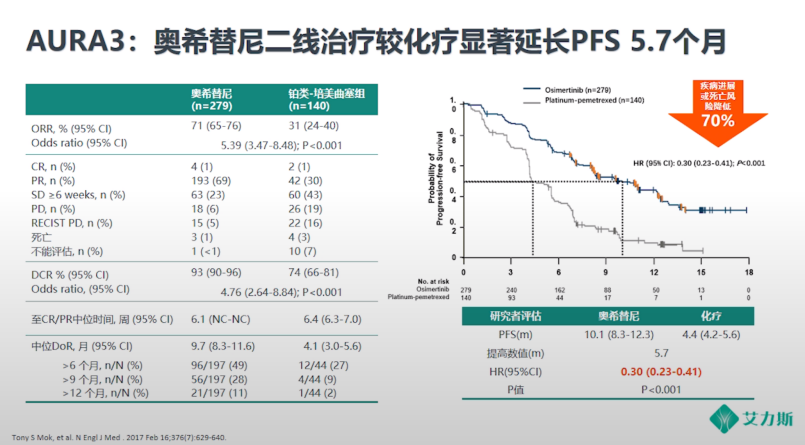
为了更好的克服耐药,三代EGFR TKI在保留不可逆结合特性的同时,将喹唑啉母环更换为嘧啶母环,增加对T790M抑制作用的同时增强了选择性。AURA3研究对一线EGFR治疗后耐药患者分别使用了奥希替尼和化疗,结果显示,奥希替尼较化疗可显著延长患者PFS(10.1个月vs 4.4个月)。针对亚裔人群使用奥希替尼二线治疗的AURA17研究PFS也达9.7个月,显示三代EGFR TKI能够更好地解决耐药问题。
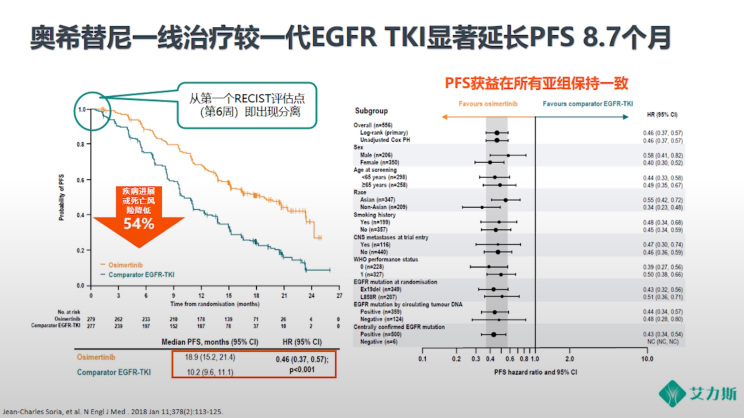
此外,FLAURA研究进一步实现了三代EGFR TKI从二线到一线的跨越。对于EGFR阳性NSCLC患者,奥希替尼较一代EGFR TKI能够显著延长PFS(18.9个月 vs 10.2个月)和OS(38.6个月vs 31.8个月),对脑转移患者也有更好的疗效,并且具有更好安全性。因此,NCCN指南、CSCO指南均将三代EGFR TKI作为EGFR突变的NSCLC一线优选用药推荐。
随着精准治疗的不断发展,针对不同类型的EGFR突变模式患者将有不同的EGFR TKI联合用药方案进行更精细化的管理。临床中不仅仅对高频突变实现了精准治疗,对于不断发现的低频突变,相应的靶向药物也在不断问世,全基因检测将为患者争取更多的治疗机会。未来的治疗将更加精益求精,最大化的延长患者总生存。