复旦大学附属中山医院刘澎教授发表伊沙佐米一线治疗NNMM的真实世界数据
含口服蛋白酶体抑制剂伊沙佐米的诱导治疗方案在针对多发性骨髓瘤(MM)的临床研究中已经展现出良好的疗效和安全性,但其在真实临床实践中的应用数据或经验仍然有限。在常规治疗中,由于多方面原因,很少有患者接受以伊沙佐米为基础的诱导治疗。为了评估伊沙佐米方案诱导治疗在真实世界中的有效性和安全性,复旦大学附属中山医院刘澎教授团队对国内14家中心应用伊沙佐米一线治疗的新诊断MM(NDMM)患者的初步疗效和安全性进行了观察分析,其结果于近日发布在《血液学年鉴》(Annals of Hematology)上。

刘澎
主任医师,教授,博士生导师
复旦大学附属中山医院血液科主任
复旦大学附属中山医院厦门医院血液科主任
上海市卫生系统优秀学科带头人
上海市肿瘤防治联盟淋巴瘤专委会主任委员
上海市抗癌协会血液肿瘤专委会副主任委员
中国医师协会血液科医师分会委员
中国抗癌协会血液肿瘤专委会委员
主持国家自然科学基金 3 项
研究背景
对于NDMM,多药联合诱导治疗已经成为一种标准的治疗方法,研究显示含有蛋白酶体抑制剂的三联或四联方案可以带来更好的生存获益。此外,由于维持治疗或持续的初始治疗可以显著延长患者生存,因此持续或长期治疗的概念也已经被广泛接受。在这种情况下,蛋白酶体抑制剂硼替佐米已成为MM一线治疗的主要药物之一,但非口服给药和相关副作用限制了其在真实世界中的长期使用。
伊沙佐米是首个口服蛋白酶体抑制剂,在60多个国家被批准用于治疗接受过至少一次治疗的MM患者。伊沙佐米、来那度胺和地塞米松(IRd)的全口服联合方案在3期TOURMALINE-MM1研究和真实世界中均表现出持久的有效性和良好的耐受性。根据1/2期研究(NCT01217957)的结果,IRd方案在NDMM中表现出良好的疗效和可接受的毒性特征,总有效率(ORR)为92%。此外,以伊沙佐米为基础的全口服方案联合环磷酰胺和地塞米松(ICd)在第2阶段研究中显示了良好的疗效。
但鉴于常规临床实践存在的多方面原因,以伊沙佐米为基础的一线治疗相关数据有限。本次报道了国内14个中心应用伊沙佐米一线治疗NDMM患者的初步疗效和安全性,以期为临床决策的制定提供参考数据。
患者及方法
该项全国性、多中心、回顾性、观察性研究分析了85例在实际临床中接受含伊沙佐米方案诱导治疗的NDMM患者的临床资料。进入该研究的患者必须根据2014年国际骨髓瘤工作组(IMWG)标准诊断为MM,并且在接受至少1个周期伊沙佐米治疗前未接受过治疗。
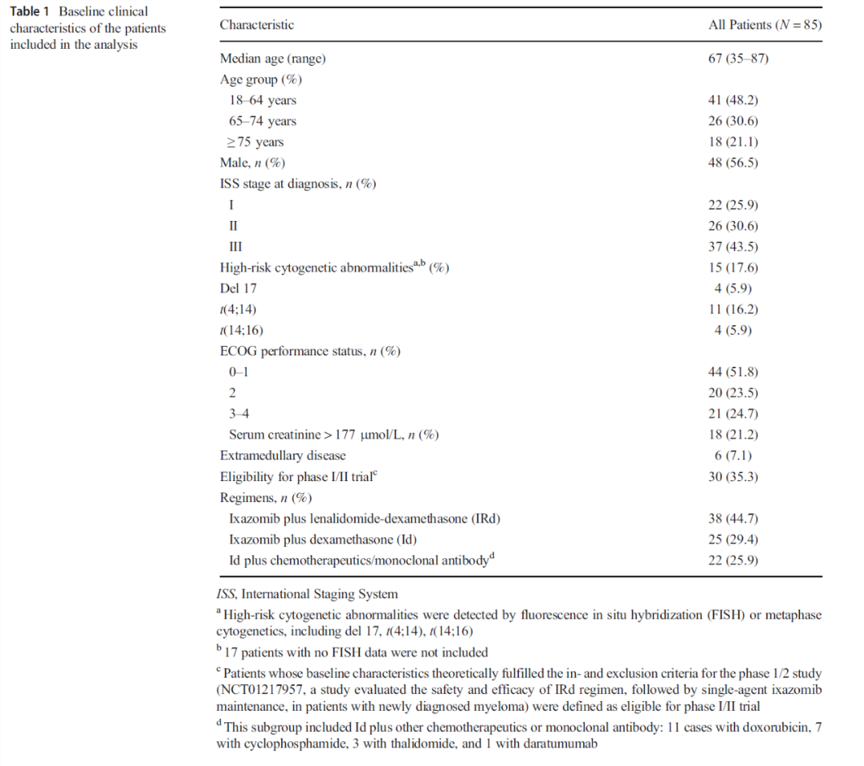
该项分析的主要目的是为了明确真实世界中,一线使用含伊沙佐米方案的客观有效率(ORR,部分缓解[PR]或更好的缓解)、完全缓解(CR)或非常好的PR(VGPR)。次要终点包括无进展生存(PFS)、总生存(OS)和根据FISH或中期细胞遗传学定义的细胞遗传学风险分层患者亚组的应答率。高危细胞遗传学异常包括del17、t(4;14)、t(14;16)。同时,该项分析也评估了安全性,包括常见不良事件和严重不良事件的发生率、治疗暴露时间、停药率及其原因等。
该研究分析的含伊沙佐米的方案包括IRd方案、Id方案以及与其他化疗药物或单克隆抗体联合的方案等。选择的患者在接受长达12个周期的伊沙佐米诱导治疗后,接受长期伊沙佐米单药维持治疗。患者接受以伊沙佐米为基础的方案的持续治疗,直至疾病进展,或发生不能耐受的毒性,或患者/医生决定结束治疗。
研究结果
共有来自14家医疗中心的85例NDMM患者接受了至少1个周期以伊沙佐米为基础的方案的一线诱导治疗。诊断时中位年龄为67岁。43.5%的患者为晚期ISS III期,48.2%的患者ECOG评分≥2。细胞遗传学和FISH分析(68例患者的数据可用),17.6%的患者被确定为高危CA。
根据1/2期研究排除标准,评估NDMM的IRd方案,30例(35.3%)患者不符合本临床试验的条件。不符合临床试验的标准包括ECOG评分超过2、2级或更高级别的周围神经病变、过去6个月内未控制的心血管疾病、2年内既往恶性肿瘤和其他。
数据截止时,所有患者的平均随访时间为10.3个月。数据截止期,56.5%(48/85)的患者仍在接受伊沙佐米治疗,其中90%(9/10)的患者接受伊沙佐米单药维持治疗。停止治疗的原因包括不良事件、疾病进展以及其他原因如继续进行SCT、替代治疗、依从性差、经济压力以及COVID-19期间药物可及性差。
疗效分析
85例患者的最佳确定ORR为95.3%,其中VGPR≥65.9%,CR(包括sCR)29.5%。第一次记录应答的中位时间为30天,最佳应答的中位时间为64天。随着时间的推移,反应加深(图1)。
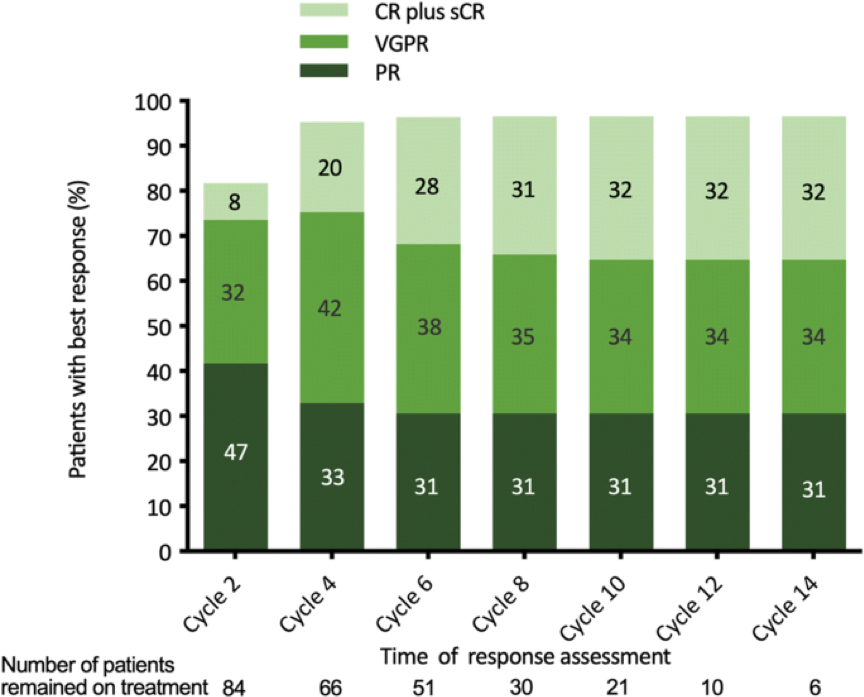
在15例高危CA患者中,ORR为86.7%,其中VGPR为33.3%,CR为13.3%。尽管高危CA亚组的ORR与总体人群相当,但CR率和≥VGPR率更低(p=0.016)。接受不同治疗方案的患者在最佳确诊反应和反应时间方面没有显著差异。
在OS和PFS方面,在整个人群和任何一个亚组中,中位OS和PFS不可估计(NE)。数据截止时, 11例(12.9%)患者出现疾病进展。在landmark 分析中,整体的12个月PFS和OS分别为86.3%和95.3%。对于CA不同危险分层的患者、接受不同治疗方案的患者以及年龄超过75岁的患者,未发现统计学上的显著差异。然而,根据纳入/排除标准、ECOGPS > 2和不符合新诊断MM IRd 1/2期试验(NCT01217957)的患者表现出较差的PFS(p<0.05);见下图2。
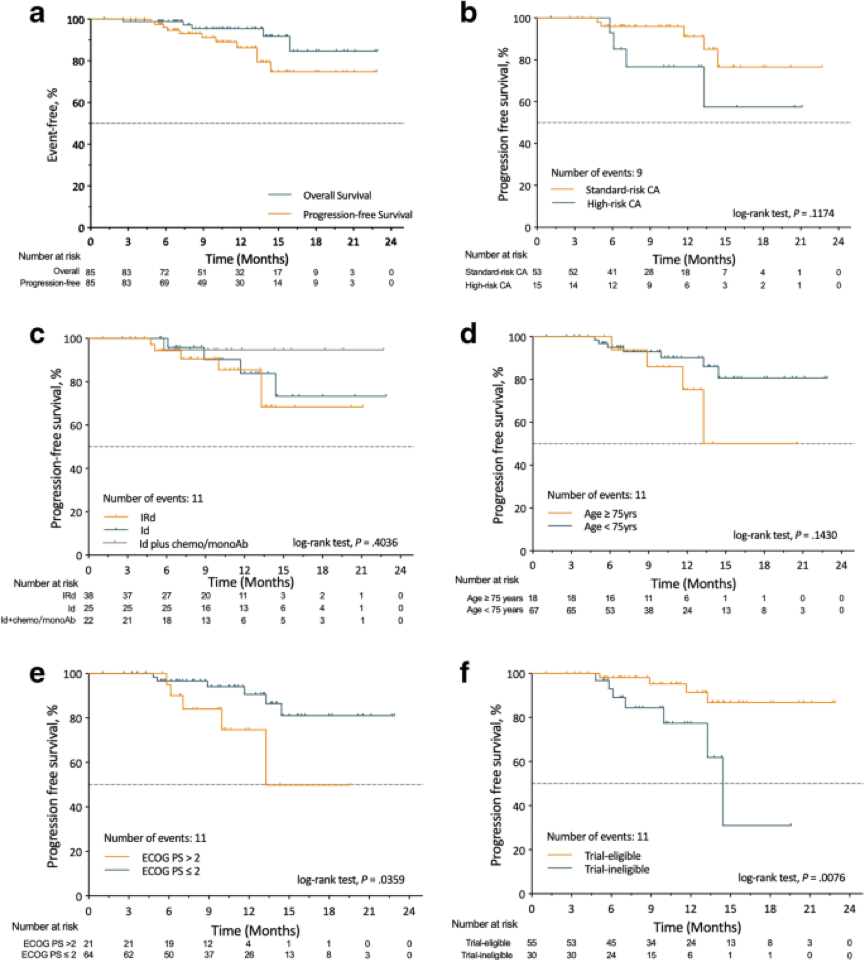
安全性分析
整个研究中,29.4%的患者出现严重不良事件(≥3级),包括血小板减少症、淋巴细胞减少症、腹泻、肺炎等。5例患者发生周围神经病变,但未发生3/4级周围神经病变,但由于这项分析的回顾性,有些轻度PN的病例可能被漏检。对于13例因不良反应停药的患者,其中9例患者至少经历了1次3~4级不良反应,包括感染、腹泻、血小板减少、腹胀。
研究结论
本次报告了第一个真实世界、多中心研究的数据,探讨了含伊沙佐米方案一线治疗NDMM患者的有效性和安全性。该项多中心、回顾性、观察性研究强调了含伊沙佐米方案一线治疗NDMM患者在真实世界中的疗效、可行性和耐受性。另外,该分析结果与NDMM中IRd的1/2阶段临床试验(NCT01217957)的结果具有可比性。伊沙佐米于2018年4月在中国上市,该研究的结果令人鼓舞,虽然随访时间短,但实际数据证实基于伊沙佐米的治疗方案在NDMM的常规治疗中安全有效。
参考文献
Jing Li , Li Bao, Zhongjun Xia,et al, Ixazomib-based frontline therapy in patients with newly diagnosed multiple myeloma in real-life practice showed comparable efficacy and safety profile with those reported in clinical trial: a multi-center study.Ann Hematol. 2020 Sep 6;1-10.