免疫检查点抑制剂相关结肠炎你了解吗?
【摘要】免疫检查点抑制剂(immune checkpoint inhibitors ,ICIs)主要包括抗细胞毒T淋巴细胞相关抗原-4(cytotoxic T-lymphocyte antigen 4, CTLA-4)及程序性死亡受体-1及其配体(anti-programmed cell death 1/anti-programmed cell death 1 ligand 1,PD-1/PD-L1) 抗体。随着ICIs在肿瘤的免疫治疗中的广泛应用,对ICIs导致的免疫相关不良事件(immune-related adverse events, irAEs)的认识也愈发深入。消化道是irAEs的常见受累部位,通常表现为腹泻及结肠炎,是导致ICIs停用的最常见irAE之一。本文旨在对免疫检查点抑制剂相关结肠炎的流行病学、临床管理及研究进展作一阐述。
ICIs通过阻断免疫检查点信号通路的抑制性免疫调节,增强免疫细胞功能,进而发挥抗肿瘤作用。irAEs可发生于人体多个系统,但总体发生率较低,多数可以通过停药及治疗逆转,因此,对irAEs的早期管理至为重要。免疫检查点抑制剂相关结肠炎作为常见的irAEs,近年来随着各类ICIs的上市,对其认识也越发深入。
1、免疫检查点抑制剂相关结肠炎的流行病学
消化道是irAEs常见的受累部位,最典型表现为腹泻及结肠炎,其他表现包括腹痛、便血、恶心、呕吐等,3级以上的免疫相关消化道毒性是导致ICIs停用的常见原因。参考美国国立癌症研究所常见不良事件评价标准5.0版(Common Terminology Criteria for Adverse Events v5.0,CTCAE v5.0),可根据临床表现将结肠炎及腹泻严重程度分为5级(见表1)

目前美国食品药品管理局(Food and Drug Administration ,FDA)已批准7种ICIs用于癌症的治疗,包括:ipilimumab(靶点CTLA-4),pembrolizu-mab、nivolumab 和cemiplimab(靶点PD-1),atezolizumab,avelumab和durvalumab(靶点PD-L1),国内上市的替雷利珠单抗、卡瑞丽珠单抗、信迪利单抗、特瑞普利单抗均为抗PD-1抗体。
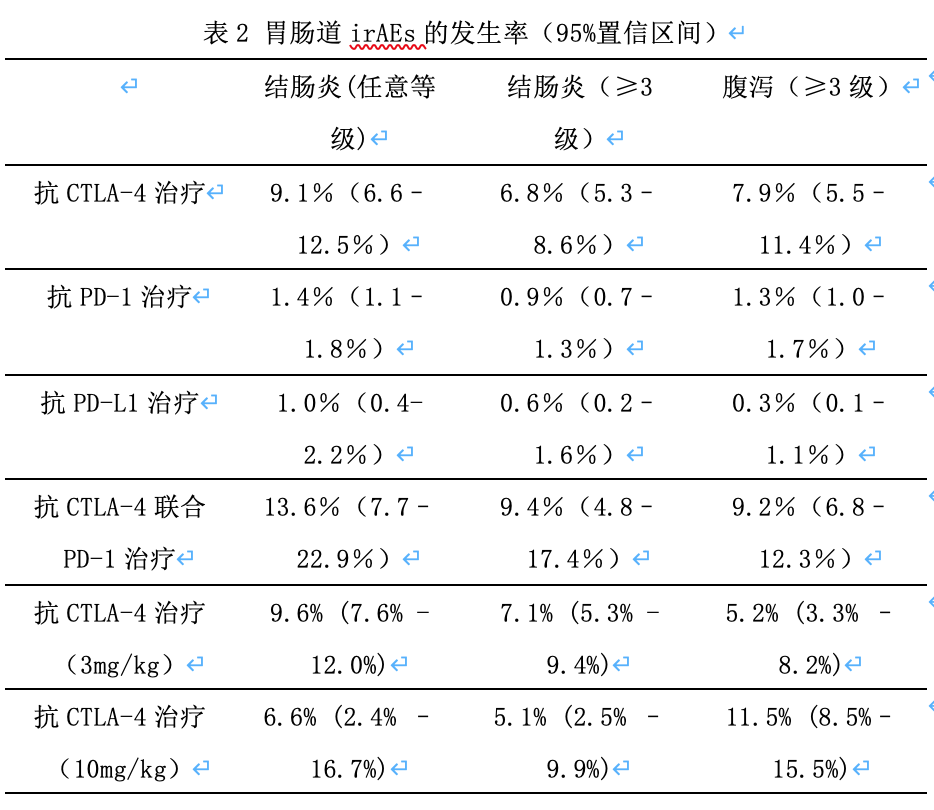
胃肠道毒性可出现在抗CTLA-4治疗中的任意时间,结肠炎通常发生于首次用药后的4-8周,从发现结肠炎到末次用药的中位时间为11天,最长时间不超过2个月,对于接受PD-1/PD-L1抑制剂治疗的患者,出现胃肠道毒性的中位时间约为3个月。在一项纳入了34项临床研究(n=8863)的荟萃分析中指出,接受抗CTLA-4治疗的患者消化道相关irAEs的发生率及严重程度明显高于接受抗PD-1/PD-L1治疗的患者,同时严重腹泻的发生率与剂量正相关,且抗CTLA-4联合抗PD-1治疗比使用ICIs单药治疗具有更强的胃肠道毒性,对于接受不同单药或联合治疗的患者,胃肠道毒性的发生率如下。
2、免疫检查点抑制剂相关结肠炎的临床症状及诊断
免疫检查点抑制剂相关结肠炎的临床表现不具有特异性,需要与消化道感染及原发肿瘤症状鉴别,诊断依赖于临床症状与用药的时间关系、实验室检查及内镜、组织学特征。
免疫检查点抑制剂相关结肠炎患者通常出现贫血、低白蛋白血症及血清C-反应蛋白升高,少数患者可出现抗中性粒细胞胞浆抗体(antineutrophil cytoplasmic antibody, ANCA)等免疫性抗体阳性。对于出现腹泻及结肠炎的患者,应通过血常规、电解质、肝肾功能等血液学检查评估一般情况,并完善粪便病原学检查除外感染。此外,一些粪便生物标志物对免疫检查点抑制剂相关结肠炎诊断具有参考价值,乳铁蛋白(lactoferrin,LF)及钙卫蛋白(calprotectin)被用于炎症性肠病((Inflammatory bowel disease,IBD)的诊断、活动性及疗效评估、复发预测等方面,MD Anderson癌症中心的一项回顾性研究表明对于接受乳铁蛋白检测的结肠炎患者,内镜下炎症的检测敏感度为70%,组织学炎症的检测敏感度为90%。另一方面溃疡患者的粪便钙卫蛋白(calprotectin)的平均值为465mcg/g粪便,而内镜特征正常的患者粪便中的钙卫蛋白值为152mcg/g,如果以粪便钙卫蛋白> 150mcg/g为标准,内镜异常特征的敏感度为68%,组织学炎症的敏感度为86%。美国国立综合癌症网络(NCCN)指南建议对出现胃肠道毒性的患者完善乳铁蛋白/钙卫蛋白检查。但乳铁蛋白/钙卫蛋白指标对免疫检查点抑制剂相关结肠炎诊断的截断值尚未存在统一标准,对于疾病活动性的监测及疗效评估的价值仍需要进一步研究。
免疫检查点抑制剂相关结肠炎内镜下多表现为黏膜充血、血管纹理消失、糜烂和溃疡形成,病变可弥漫分布,也可呈节段性分布,多累及左半结肠。组织学图像多出现中性粒细胞、嗜酸性粒细胞浸润等急性结肠炎表现,也有部分出现慢性炎症性肠病的特征, 如单核细胞及中性粒细胞细胞浸润、肉芽肿隐窝异常(萎缩、扭曲和分支) 等。影像学检查有助判断炎症的严重程度,并除外穿孔等严重并发症,在对免疫相关性结肠炎的患者进行的回顾性研究中,分别有50%、33%和17%的患者通过CT观察到孤立性乙状结肠炎,弥散性结肠炎和与憩室病相关的节段性结肠炎。Marthey等在一项回顾性分析中指出,内镜检查的时机是影响预后的重要因素,对于在症状发作30天内完善内镜检查的患者,激素治疗的时间、复发几率、接受重症监护及使用生物制剂治疗比例较低。另一项研究表明,通过CT评估组织学阳性的结肠炎的阳性预测值高达96%,对于需要使用糖皮质激素缓解症状的结肠炎阳性预测值为92%。因此,对于存在2级及2级以上的胃肠道毒性的患者,应及时完善内镜检查评估病情,3级及3级以上的患者,建议完善腹部盆腔增强CT。
3、免疫检查点抑制剂相关结肠炎的临床管理
免疫检查点抑制剂相关结肠炎处理原则是及时有效控制症状、减少复发及并发症、最大化ICIs对肿瘤治疗的获益。轻度免疫检查点抑制剂相关结肠炎患者的症状可通过对症治疗缓解,对于持续不缓解的患者使用口服糖皮质激素具有良好效果。症状严重者需要静脉应用甲基泼尼松龙,症状缓解后可改为口服并逐渐减量。对于糖皮质激素反应不佳的患者,可以给予肿瘤坏死因子-&α;(Tumor Necrosis Factor-&α;,TNF-&α;)拮抗剂英夫利昔单抗治疗,同时可减少长期使用糖皮质激素的风险,短期使用不会影响ICIs的临床获益。Vedolizumab是一类作用于&α;4&β;7整合素的单克隆抗体,可特异性作用于胃肠道,相对于英夫利昔单抗的全身不良反应更少,Hsieh报道了一例应用vedolizumab治疗难治性免疫检查点抑制剂相关结肠炎的病例,患者在用药6周后临床症状缓解,实现内镜下粘膜愈合。另一项研究纳入了28名难治性免疫检查点抑制剂相关结肠炎患者,其中有9名(32%)对糖皮质激素或英夫利昔单抗治疗无反应,84%通过使用vedolizumab获得了持续临床缓解,同时有54%的患者达到了内镜下缓解。一项回顾性多中心研究纳入了167名恢复了ICIs治疗的结肠炎患者。34%的患者发生了复发性结肠炎,其中81%需要糖皮质激素治疗,12%需要联合用英夫利昔单抗或vedolizumab治疗。与抗PD-1/PD-L1治疗相比,抗CTLA-4治疗后复发时间更早,但严重性没有显著差异。
对于1级的轻度患者,可继续ICIs治疗,必要时予以补液、洛哌丁胺止泻等对症治疗,同时避免高纤维/乳糖饮食以免加重症状。2级的中度患者应暂停ICIs,初始口服糖皮质激素1mg/(kg·d),若48-72小时内症状无明显缓解,激素加量至2mg/(kg·d),必要时使用英夫利昔单抗。对于3级及3级以上的重度患者,应静脉使用甲基强的松龙2mg/(kg·d),如症状在48小时内未缓解,应加用英夫利昔单抗或vedolizumab。3级不良反应的患者应停抗CLTA-4治疗,在症状缓解后可考虑改用抗PD-1/PD-L1治疗,出现4级不良反应的患者应永久停止免疫治疗。对于使用糖皮质激素有效的患者,中度患者应在2-4周时间内逐渐减停,重度患者调整为口服后在4-8周内减停,并监测血糖,补充维生素D和钙,以减少感染、骨质疏松等激素相关不良事件的风险。英夫利昔单抗适用于激素治疗无效的患者,通常剂量为5mg/kg,由于存在加重感染和心力衰竭的风险,应在使用前完善相关检查除外穿孔、结核、严重感染及心功能不全等因素。vedolizumab作为选择性肠道整合素抑制剂,相对于英夫利昔单抗的全身影响以及对潜伏性结核再激活的风险更小,但起效时间较慢。
4、免疫检查点抑制剂相关结肠炎的研究进展
(1)粪便菌群移植
粪便菌群移植(fecal microbiota transplantation,FMT)通过转移从粪便样本中提取到的菌群到另一名患者的体内,用以改善接受者体内的肠道菌群,已被用于治疗艰难梭菌相关性肠炎及慢性炎症性肠病。此外,也有研究表明部分微生物可以强化抗原呈递从而增强抗肿瘤免疫应答,并改善外周和肿瘤微环境中的效应T细胞功能,从而改善肿瘤患者对免疫治疗的反。2018年报道了2例通过FMT达到完全缓解的免疫检查点抑制剂相关结肠炎病例,两名患者在接受了免疫治疗后出现严重的结肠炎,且激素和免疫抑制剂治疗无效,在接受了FMT治疗后临床症状完全缓解,内镜检查提示溃疡消退,炎症明显减轻,组织学提示CD8 T细胞亚型数量减少。一项回顾性分析(n=826)提示在接受ICIs治疗后使用厌氧菌活性的抗生素会增加发生免疫检查点抑制剂相关结肠炎的风险,并导致OS下降。尽管取得了以上发现,FMT的应用仍存在诸多问题。首先,FMT的疗效并不明确。其次,FMT的安全性也难以保证,尽管既往FMT的不良事件相对罕见,但2019年发表的个案报道披露,有两位不同临床试验的病人因接受了同一供者的粪便发生了产超广谱&β;-内酰胺酶(Extended broad spectrum &β;-lactamases,EBSL)大肠杆菌菌血症,并导致其中一人死亡,细菌培养显示来自此供者的粪便胶囊中均存在产EBSL大肠杆菌,两位患者接受FMT之前的粪便培养结果为阴性,而基因测序显示受者血液样本中细菌与供者粪便中的细菌具有遗传相关性,证实患者因FMT导致严重感染。目前仍需要进一步研究确定与肿瘤及免疫检查点抑制剂相关结肠炎良好预后相关的细菌菌群,评估FMT对预防免疫检查点抑制剂相关结肠炎及其复发的作用,此外FMT的质控和标准化仍然任重道远。
(2) TNF-&α;抑制剂与ICIs联合治疗
英夫利昔单抗通常用于糖皮质激素无效的难治性肠炎。临床前研究表明,对于联合抗CTLA-4及抗PD-1治疗的肿瘤小鼠模型,实验过程中加入TNF抑制剂的组在生存率上有明显的优势,对肿瘤也有更强的抑制作用,实验发现抑制TNF可以显著增强肿瘤特异性CD8+T细胞向肿瘤微环境和引流淋巴结的浸润,同时阻断TNF还可以减慢T细胞激活所诱导的细胞死亡,从而提高抗肿瘤效果,并减少结肠炎的风险。基于以上发现,Yousef等发表了接受ICIs及TNF-&α;抑制剂合并用药的个案报道,5名患者在ICIs之后出现免疫检查点抑制剂相关结肠炎并依赖糖皮质激素治疗,为防止恢复ICIs治疗后长时间使用激素及预防复发,治疗方案改为ICIs联合英夫利昔单抗。此后所有患者未出现复发性结肠炎,其中3名患者内镜提示急性炎症消失,4名患者疾病稳定。目前纳武利尤单抗、依匹木单抗联合英夫利昔单抗治疗晚期黑色素瘤的I期临床试验仍在进行中(NCT03293784)。
(3)免疫检查点抑制剂相关结肠炎的预测指标
目前尚没有可以预测免疫检查点抑制剂相关结肠炎的常规生物标志物。研究表明,免疫治疗前肠道微生物组的组成与胃肠道毒性相关,基线微生物组富含厚壁菌属的患者应用抗CTLA-4治疗有更好的预后及更高的结肠炎风险。此外,细胞因子水平也可用于预测CTLA-4抗体治疗后发生严重胃肠道毒性的可能,Ahmad等研究发现,基线的高IL-17水平与治疗后3级腹泻及结肠炎的发生率正相关,Lim等]通过评估接受抗PD-1治疗或者抗PD-1联合抗CTLA-4治疗6周内患者细胞因子的表达情况,发现共有11种细胞因子的表达升高与严重irAEs相关,并就此整合为CYTOX评分,用于预测免疫治疗中的严重irAEs,验证队列显示了良好的相关性(P<0.05)。然而与具有相似临床特征的炎症性肠病相比,免疫检查点抑制剂相关结肠炎易感基因的研究甚少,一方面具有典型胃肠道毒性表现的患者样本量较少,另一方面也可能与环境暴露及治疗方案的异质性有关。
5、结语
ICIs已经深刻地改变了肿瘤治疗领域,不同于传统的化疗及靶向药物,ICIs导致的irAEs表现出截然不同的临床特点。随着免疫治疗市场的扩大及抗CTLA-4药物的临近上市,对免疫检查点抑制剂相关结肠炎的诊治提出了更高的要求。免疫检查点抑制剂相关结肠炎的诊断、评估主要依赖于临床症状、内镜、影像检查及病理组织学活检。糖皮质激素是中重度肠炎的主要治疗手段,而英夫利昔单抗和vedolizumab对难治性结肠炎的治疗取得了良好效果。目前对于难治性肠炎的最佳药物、剂量及给药时间还没有定论,其他新型生物制剂用于免疫检查点抑制剂相关结肠炎治疗也在研究中。未来能否通过生物标志物筛选高危人群、评价疾病活动性及疗效,如何制定最佳的免疫抑制策略减少治疗对ICIs效果的影响都值得进一步探索。