晚期复发卵巢癌化疗外的新选择
晚期复发上皮性卵巢癌的去化疗治疗一直备受争议,虽然早已得到NCCN指南推荐,但仍未在临床广泛应用。近日,刚刚举行的ESMO大会报道了另一项新的PARP抑制剂pamiparib在复发卵巢癌的临床研究结果,pamiparib有可能成为国内继奥拉帕利、尼拉帕利、fluzoparib之后上市的第四款PARP抑制剂,为晚期复发上皮性卵巢癌患者的治疗提供新的选择。
【摘要820P】Pamiparib治疗中国晚期卵巢癌患者的一项Ⅱ期临床研究
背景
Pamiparib是一款自主研发的、针对PAPR1/2酶的高选择性抑制剂,并对PARP-DNA复合物具有捕获能力。其首个临床研究(NCT02361723)将pamiparib的临床剂量确定为60 mg po bid;并且不论是否具有BRCA基因突变,不论铂敏感复发或铂耐药复发,pamiparib在所有晚期卵巢癌患者中表现出临床活性。本次ESMO大会发布了pamiparib另一项在中国晚期实体瘤患者中正在进行的(NCT03333915)的Ⅱ期研究的结果。
方法
入选具有已知/疑似致病的gBRCA1/2突变且经过≥2线化疗后进展的晚期卵巢癌患者,分为铂敏感(队列1)和铂耐药(队列2)两个队列,采用pamiparib 60mg bid口服治疗,直至疾病进展。主要终点是由孤立评审委员会根据RECIST v1.1评估的客观缓解率(ORRIRC)。
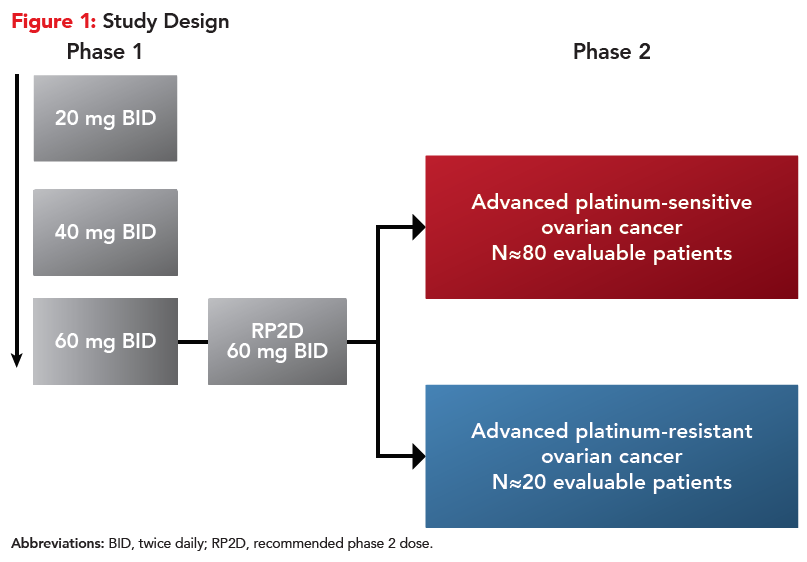
结果
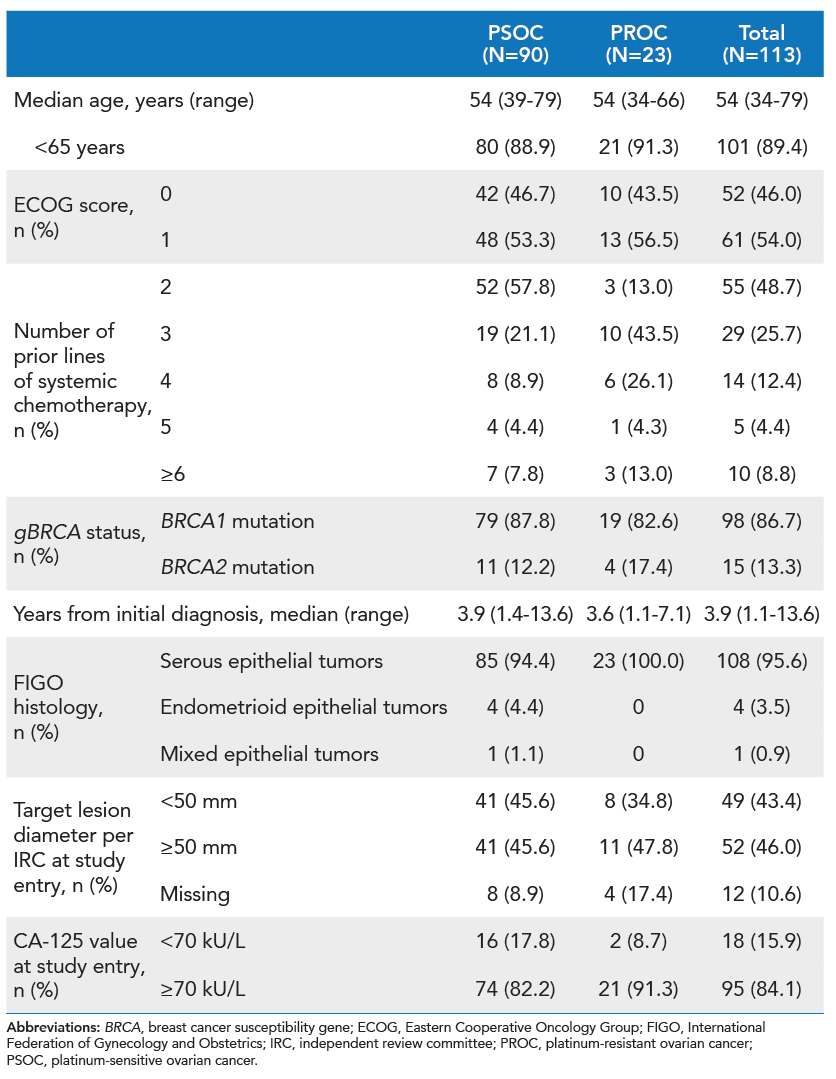
截至2020年2月2日,一共入组113名患者(队列1,n=90;队列2,n=23),入组患者的中位年龄为54岁(范围:34~79岁),其中25.6%(n=29)的患者接受过4次以上全身化疗,54.0%(n=61)的患者在研究开始时的ECOG评分为1。
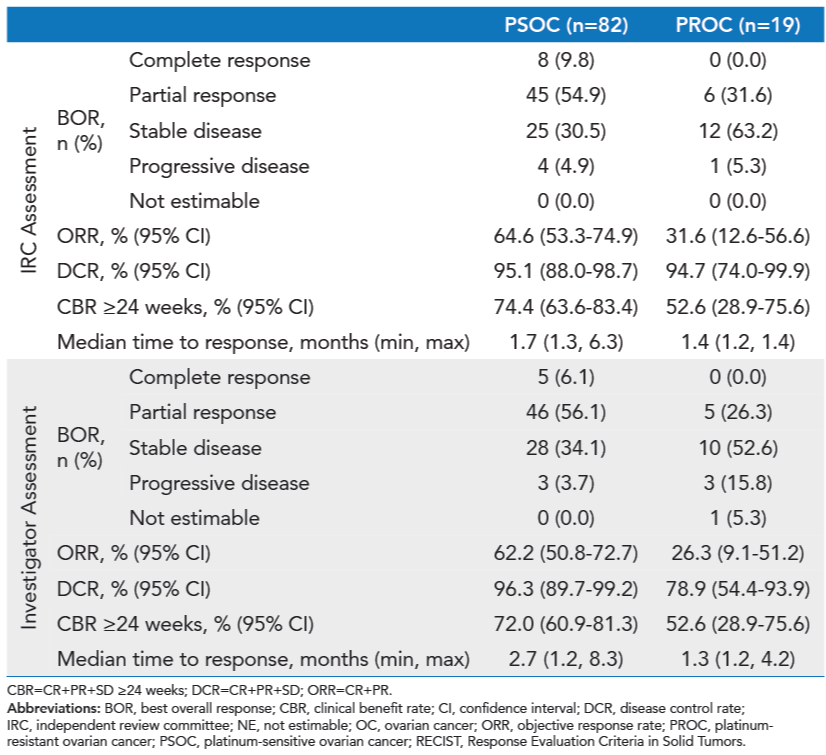
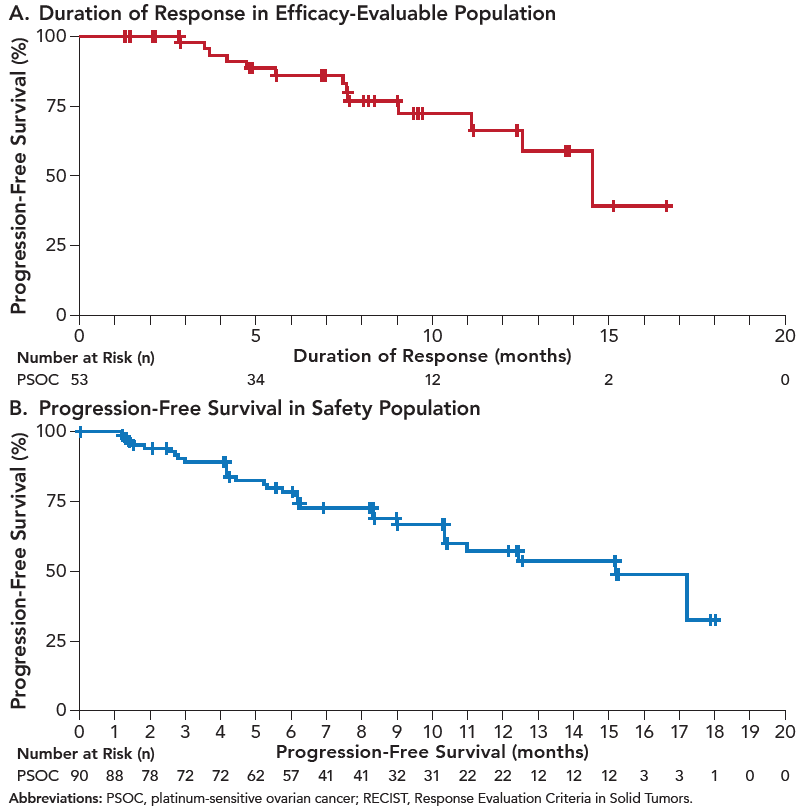
数据截止时,中位随访时间为12.2个月(范围:0.2~21.5个月)。在两个队列中,pamiparib均显示出初步的抗肿瘤活性。在队列1中,证实的ORRIRC为64.6%,中位缓解持续时间(DOR)为14.5个月(95%CI,11.1个月~NE),中位无进展生存期(PFS)为15.2个月(95%CI,10.35个月~NE),中位总生存期(OS)尚未成熟。队列2中,证实的ORR IRC为31.6%,中位DOR为11.1个月(95%CI,4.21个月~NE),中位PFS为6.2个月(95%CI,4.11个月~NE),中位OS为13.6个月(95%CI,7.13个月~NE)。
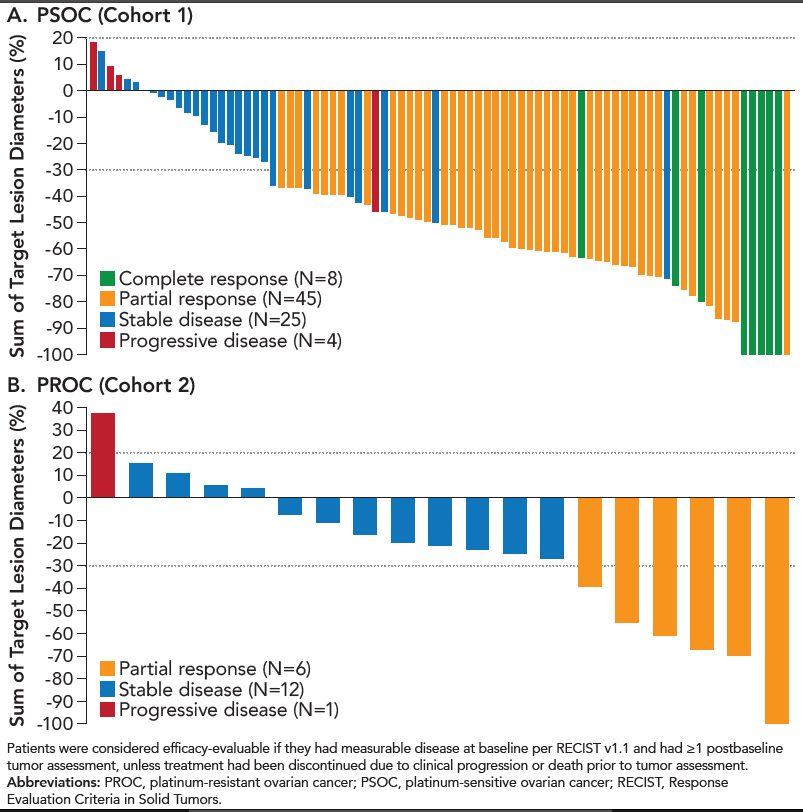
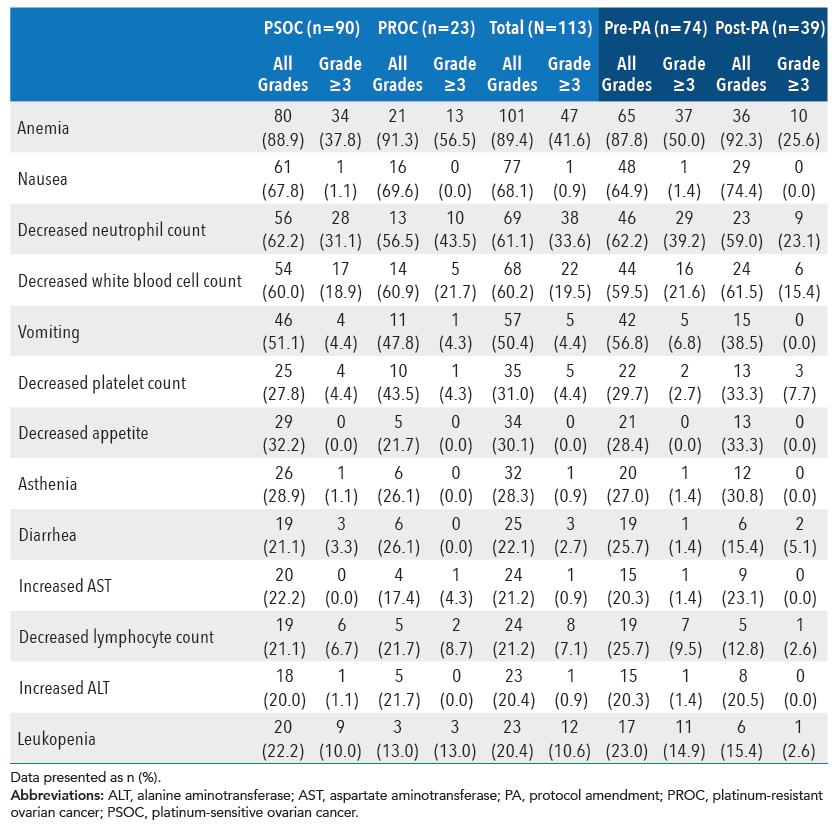
总的来说,最常见的治疗相关不良事件是贫血(任何级别,89%;3级以上,42%);按照研究方案进行剂量调整后,3级以上贫血的发生率降低到25.6%。
结论
Pamiparib在铂敏感/耐药晚期卵巢癌患者中具有良好的抗肿瘤活性,并且毒性可耐受,与之前公布的Ⅰ期研究数据相比,未出现新的安全信号。
相关阅读
Pamiparib是百济神州自主研发的一款对PARP1/2酶具有高度选择性的PARP抑制剂,并且可通过血脑屏障。2017年ESMO大会pamiparib首次公布了其在实体瘤患者中Ⅰ期剂量爬坡临床试验的数据[1]。此后百济神州公司对其继续进行开发,于2018年AACR公布了102研究的Ⅰ期研究数据[2]。2020年7月,基于102研究的Ⅱ期临床研究数据,pamiparib用于治疗晚期卵巢癌、输卵管癌或原发腹膜癌患者的NDA被受理并纳入优先审评。

此外,pamiparib在中国晚期卵巢癌患者中展开的另一项Ⅲ期临床试验(BGB-290-302)也正在进行中。

参考文献
[1] Lickliter J, Mileshkin L, Voskoboynik M, et al. Dose escalation/expansion study to investigate the safety, pharmacokinetics, food effect, and antitumor activity of BGB-290 in patients with advanced solid tumors. 2017 ESMO, 368PD.
[2] Xu B H, Yin Y M, Song Y, et al. A phase I dose escalation study of BGB-290 in Chinese subjects with advanced ovarian, fallopian, and primary peritoneal, or advanced triple-negative breast cancer. 2018 AACR, CT050.