2020年三阴乳腺癌免疫治疗新进展盘点

根据国家癌症中心2019年发布的最新报告,2015年中国女性乳腺癌发病率约为45.29/10万人,每年新发病人数约30.4万人,为全国女性肿瘤发病数首位;其中,三阴乳腺癌(TNBC)约占15-20%,即约每年新发4.56-6万人。
尽管TNBC是个小众的瘤种,因为对内分泌和靶向治疗不敏感,多年来化疗一直是TNBC的标准治疗方法,中位生存时间为12-18个月,且复发转移率高,毒性反应较重,部分患者无法耐受、预后较差,亟需探索新的方法来改善三阴型乳腺癌。
以PD-1/PD-L1免疫检查点抑制剂为代表的免疫治疗近年在许多瘤种中都取得了重大进展,在TNBC领域也有突破,极大改善了三阴乳腺癌患者的生存,前期我们有详细介绍过三阴乳腺癌的免疫治疗,今年免疫治疗又陆续涌现出许多不错的结果,这里我们简单的回顾下。
晚期一线:免疫+化疗(PD-L1阳性)
1、无论IMpassion 130还是KEYNOTE-355都是在PD-L1表达阳性人群中获益
2020 ASCO公布的KEYNOTE-355研究,是继IMpassion 130后第二个免疫联合化疗的用于一线治疗既往未经治疗的局部复发性不可手术或转移性TNBC的随机、双盲、Ⅲ期研究(NCT02819518),采用的是帕博利珠单抗联合化疗(白蛋白紫杉醇、紫杉醇或吉西他滨/卡铂) 对比化疗。
结果显示,对于PD-L1阳性(CPS≥10)的人群,帕博利珠单抗组PFS可显著延长(9.7 vs. 5.6个月,HR 0.65),具有统计学差异及临床意义;而对于CPS≥1的人群,帕博利珠单抗组的PFS虽有延长,但未达到统计学差异。亚组分析提示对于无病间期小于1年的难治性三阴性乳腺癌,免疫治疗疗效值得考量。
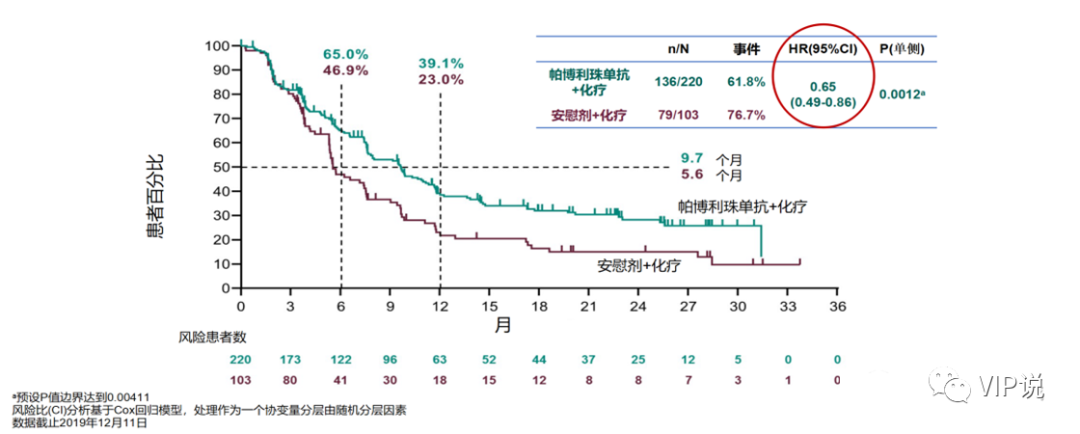
在CPS ≥10患者中,与单独化疗组相比,帕博利珠单抗+化疗显著改善了PFS,两组中的中位PFS分别为9.7个月和5.6个月(HR=0.65),达到了主要终点之一。
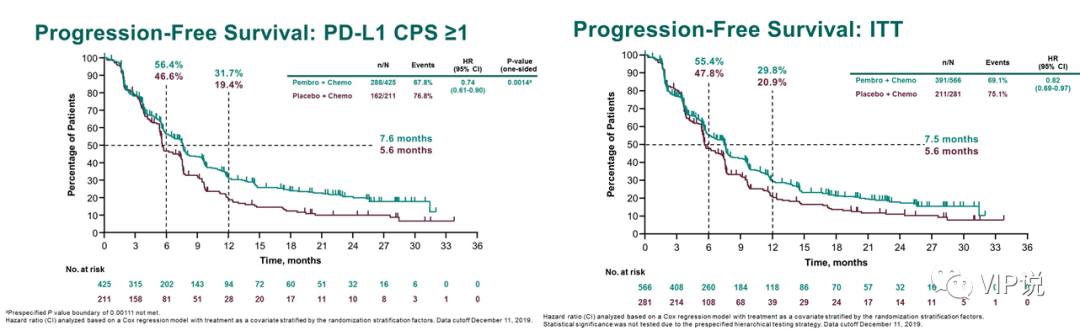
在CPS ≥1患者中,帕博利珠单抗组和单独化疗组的中位PFS分别为7.6个月和5.6个月(HR=0.74, p=0.0014),p值未达到研究预设的界值0.00111。
在ITT人群中,帕博利珠单抗组和单独化疗组的中位PFS分别为7.5个月和5.6个月(HR=0.82)。根据预设的统计学策略,在CPS ≥1患者中p值未达到研究预设的界值,故未在意向人群中评估PFS的统计学差异。

亚组分析显示,在PD-L1 CPS≥10的人群中,紫杉类化疗药物相比吉西他滨/卡铂有更多的PFS获益。
和IMpassion130对比我们可以看到,KEYNOTE-355中化疗包括白蛋白紫杉醇、紫杉醇、吉西他滨/卡铂三种化疗方案,更符合临床医师选择,IMpassion130中只有白蛋白紫杉醇一种化疗方案;KEYNOTE-355纳入了根治性治疗完成至疾病复发≥6个月的mTNBC患者,IMpassion130纳入了根治性治疗完成至疾病复发≥12个月的mTNBC患者;KEYNOTE-355使用22C3检测的CPS定义PD-L1阳性,IMPassion130使用SP142检测的IC 1%定义PD-L1阳性。
总的来说,对于晚期或转移性TNBC,IMpassion130研究和KEYNOTE-355研究都已经证实了免疫药物联合化疗方案在PD-L1阳性人群mTNBC一线治疗的有效性。
2、IMpassion 130 vs IMpassion 131 PD-L1抑制剂+ 白蛋白紫杉醇vs紫杉醇
KEYNOTE-355研究亚组分析显示紫杉类化疗药物相比吉西他滨/卡铂有更多的PFS获益,那到底白蛋白紫杉醇好还是紫杉醇好呢?我们知道PD-L1抑制剂Atezolizumab+ 白蛋白紫杉醇已经获批在一线晚期TNBC PD-L1阳性人群的适应症。
而2020年8月6日,罗氏宣布其Atezolizumab联合紫杉醇用于一线治疗PD-L1阳性、转移性三阴性乳腺癌(TNBC)的III期IMpassion131研究较安慰剂+化疗未到达无进展生存期(PFS)的主要终点。次要终点总生存期(OS)也呈阴性趋势,但目前数据还尚未成熟。罗氏表示针对OS的数据将继续随访,直到最终分析。Tecentriq联合紫杉醇的安全性与既往研究结果一致。
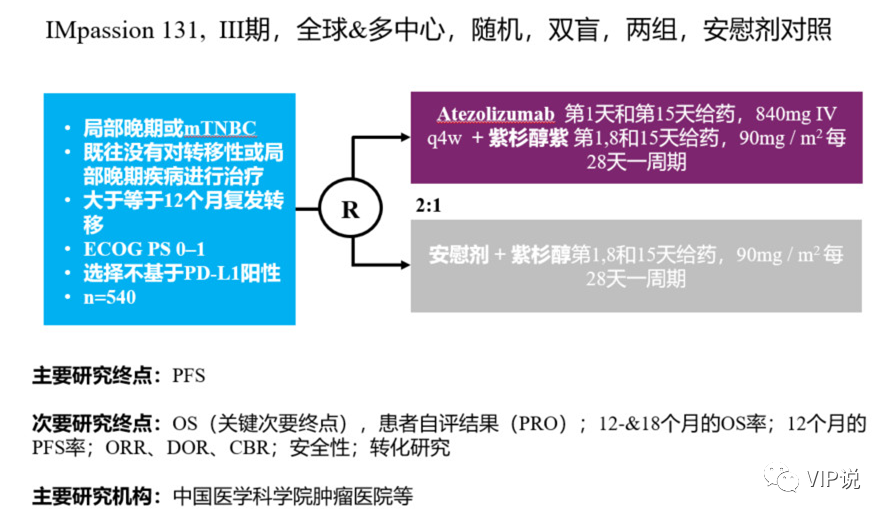
比较白蛋白紫杉醇和紫杉醇在一线TNBC中的研究不太多,2018年ESMO上报导的真实世界研究显示实际两者疗效相近,可以互换使用。
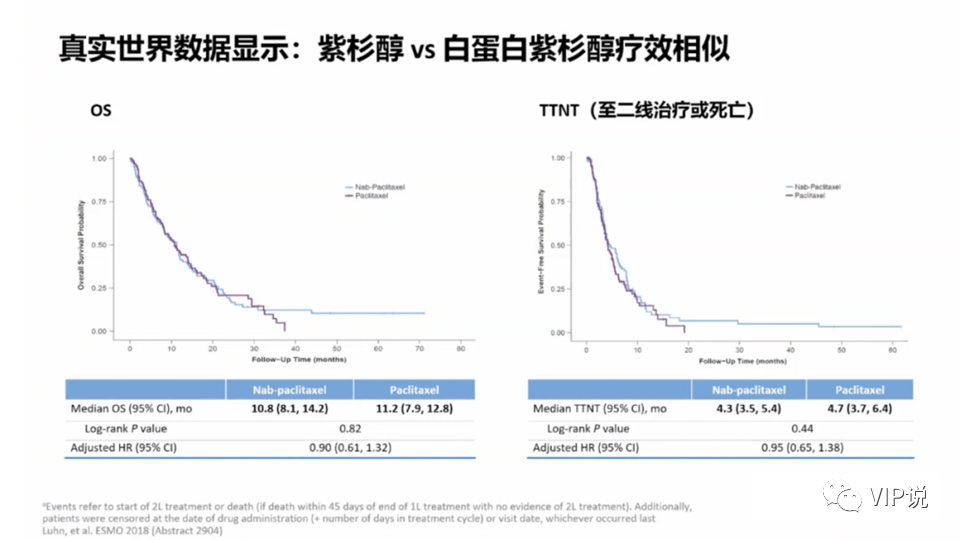
这项研究比较了白蛋白紫杉醇(n=105)和紫杉醇(n=95)在真实世界中治疗一线TNBC的生存差异。接受白蛋白紫杉醇治疗的患者中位OS为11.2个月,经紫杉醇治疗的患者中位OS为10.8个月(log-rank P= 0.82)。
调整后的Cox模型的OS风险比(HR)为0.90,表明两组之间的死亡风险相似。白紫和紫杉醇的至下次治疗时间分别为4.7和4.3个月(log-rank P= 0.44),在调整后分析中无差异HR = 0.95。研究表明两者在一线TNBC治疗中结果相似,提示可以互换。
那为什么IMpassion 130(白蛋白紫杉醇)vs IMpassion 131(紫杉醇),相同的免疫治疗药物,在相同的TNBC人群,而且采用相同的生物学标记物(PD-L1+),联合的也是同一类型化疗药,却取得相反的结果呢?
虽然白蛋白结合型紫杉醇和紫杉醇是同一类药物,但是剂型不同与免疫治疗药物联合可能会导致疗效的差别,可能常规溶剂型紫杉醇需要进行激素的预处理,而激素的使用会影响免疫治疗的效果。具体原因还需要IMpassion 131完整结果公布我们才能进一步分析,同时目前包括国产PD-1在内也有很多大型Ⅲ期研究正在开展中,例如罗氏IMpassion 132、君实CT26等等,期待他们的结果来进一步验证。
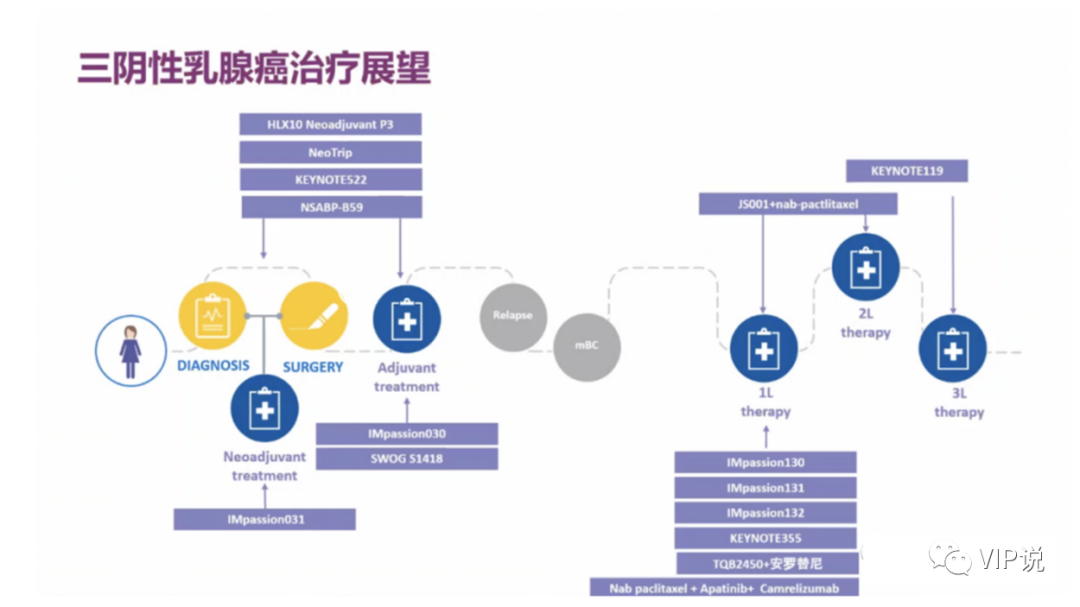
除了化疗药物,其他药物乃至放疗能否与免疫治疗联合也需要进一步探索,更为重要的是还需要更加精准的找到免疫治疗的优势人群,目前将PD-L1+考虑为免疫治疗的目标人群。
晚期三阴乳腺癌一线后维持治疗
我们知道PACIFIC研究,度伐利尤单抗1年的维持治疗奠定不可切除的局部晚期NSCLC标准治疗地位。但小细胞肺癌的一线后维持治疗的CHECKMATE-451研究却失败没有达到主要终点。尿路上皮癌一线后维持治疗的JAVELIN Bladder 100研究相比大量失败的晚期一线研究(IMvigor130、Keynote 361等)显著延长患者的OS和PFS,可能成为局部晚期或转移性UC一线化疗后未出现疾病进展的患者新标准治疗。
那三阴乳腺癌呢?免疫治疗联合化疗目前是局部晚期不可切除或转移性三阴乳腺的一线治疗手段,但高效低毒的维持治疗手段尚未形成,但我们也看到一些维持治疗的探索研究取得不错的结果。
SAFIR02-IMMUNO研究在2019年SABCS大会上公布,探索HER2阴性mBC化疗后序贯Duvalumab的2期研究入组了199例无突变位点的HER2阴性(ER+患者需对内分泌治疗耐药)患者在6-8个周期化疗后达到CR/PR/SD,2:1随机接受Durvalumab或化疗的维持治疗。
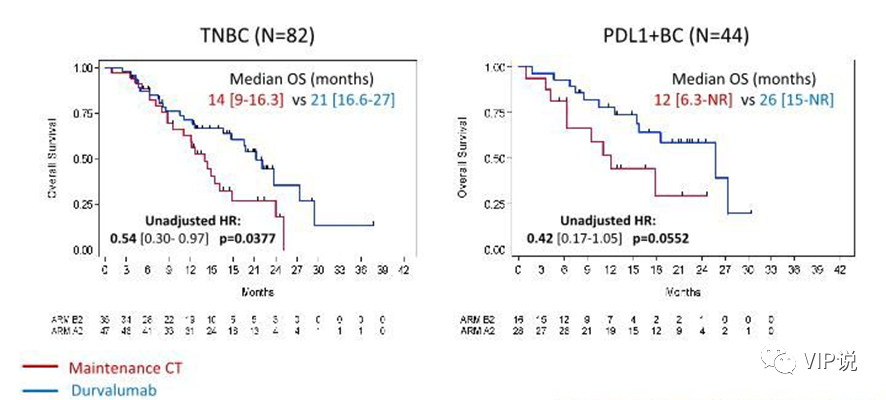
结果显示Durvalumab对比化疗的维持治疗OS未达到显著性差异(21.7个月vs 17.9个月,HR0.84,p=0.42),进一步亚组分析显示,TNBC亚组(21个月 vs 14个月,HR 0.54,p=0.0377)和PD-L1亚组(26个月vs12个月,HR 0.42,p=0.0552)获益更明显。
早期三阴乳腺癌免疫新辅助:免疫+化疗
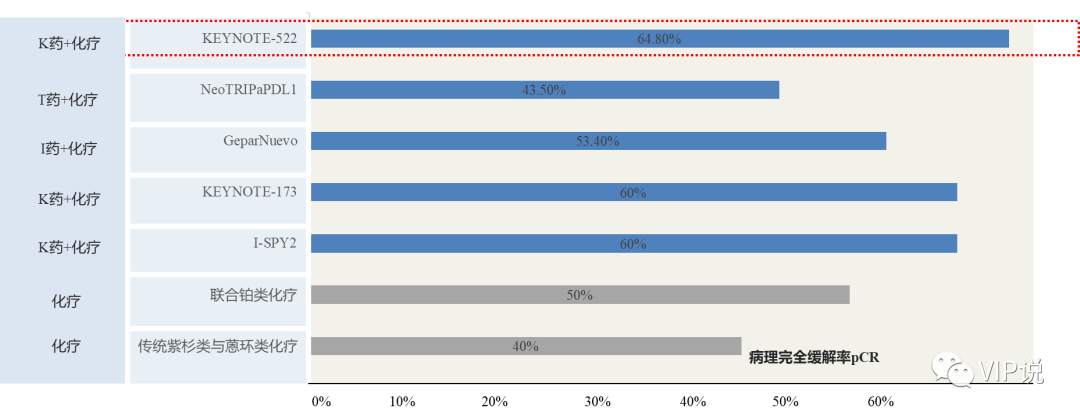
前期K药、T药和I药在三阴乳腺癌新辅助都进行过探索,KEYNOTE-522研究中免疫联合化疗新辅助治疗将pCR提高了13.6%(64.8% vs 51.2%),达到了统计学和临床意义,帕博利珠单抗新辅助+辅助治疗能延长患者18个月EFS(91.3% vs 85.3%),未达到预先设定的具有统计意义的界限,目前研究还在进行中,免疫治疗后pCR的改善对EFS改善的影响需要更长的随访呈现更多的数据。
2020年6月18日,罗氏宣布阿替利珠单抗联合化疗用于早期三阴性乳腺癌(TNBC)的III期IMpassion031研究达到病理学完全缓解(pCR)的主要终点,且无论PD-L1状态如何。详细数据将在马上召开的2020 ESMO会议上公布,期待它的结果。
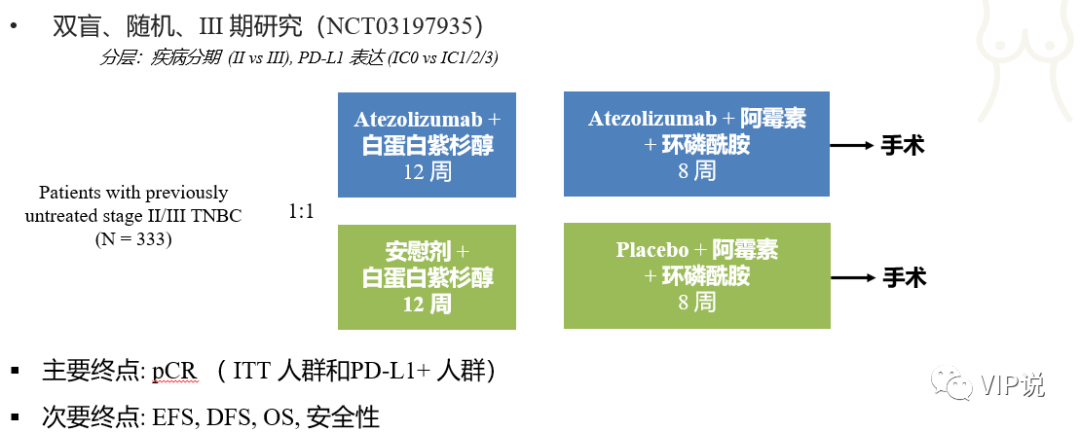
IMpassion031研究是一项多中心,随机,双盲的III期临床研究,旨在评估阿替利珠单抗联合化疗在早期TNBC新辅助治疗中的疗效和安全性。该研究共入组333例患者,1:1随机接受阿替利珠单抗+化疗或安慰剂+化疗。主要研究终点是在意向治疗(ITT)人群和PD-L1阳性人群中评估pCR,次要终点包括总生存期、无事件生存期、无病生存期和生活质量指标。
2020ASCO公布正在进行中的TNBC研究
1、KEYLYNK-009研究 2020ASCO TPS596
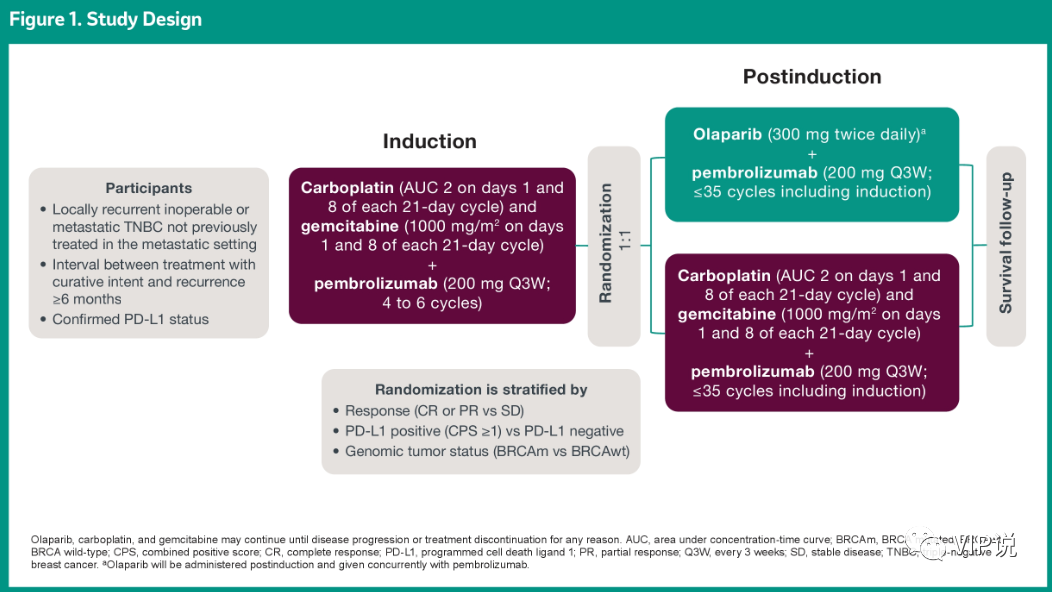
TNBC中BRCA突变患者使用奥拉帕利颇具成效,已有少量数据显示PD-1抑制剂联合奥拉帕利可取得一定疗效。KEYLYNK-009研究(TPS 596)对晚期三阴性乳腺癌患者,在帕博利珠单抗+化疗一线治疗后的维持阶段,是使用帕博利珠单抗联合奥拉帕利还是化疗进行了探索。
本研究分为II期(n=317)与III期(n=615),患者帕博利珠单抗+卡铂+吉西他滨诱导化疗后,再按1:1分组应用帕博利珠单抗联合奥拉帕利或者化疗进行维持治疗,主要终点为PFS和OS,次要终点为BRCA突变人群的PFS和OS,以及患者生存质量及安全性,目前该研究仍在入组中。
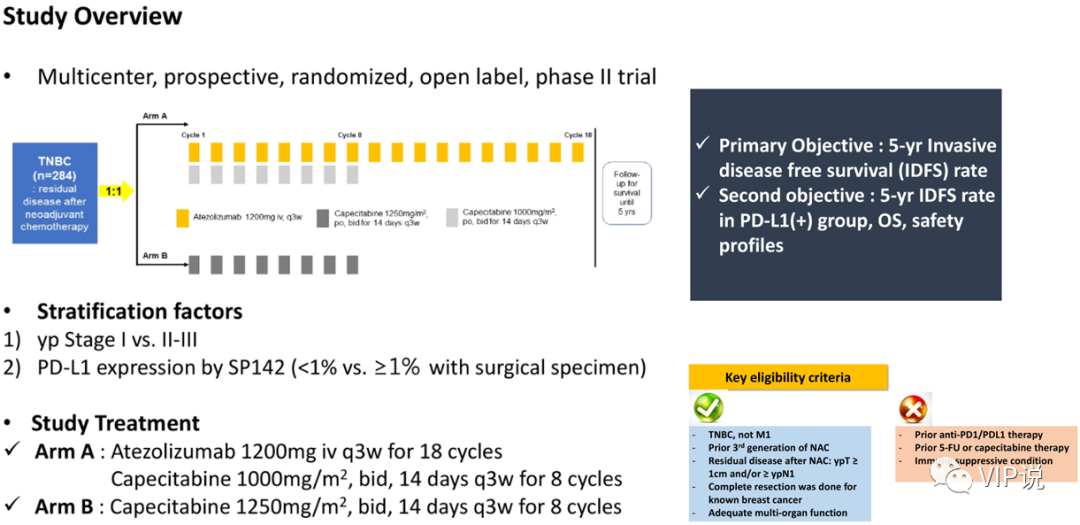
2、MIRINAE研究 2020ASCOTPS597
这是一项多中心,随机,开放标签的Ⅱ期研究,比较Atezolizumab+卡培他滨vs卡培他滨治疗新辅助术后未pCR的高危TNBC人群的疗效和安全性。
3、A-BRAVE研究 2020ASCO TPS598
这是一项III期、多中心、研究者发起的随机研究,对完成原发性TNBC根治性治疗(包括手术和化学治疗)患者,比较后续采用抗PD-L1 avelumab治疗1年与观察的疗效。

免疫治疗在早期和晚期TNBC治疗的数据均令人鼓舞,除了针对TNBC的大量免疫治疗研究,针对HER2阳性、HR阳性的乳腺癌的PD-1/PD-L1治疗的相关临床研究也在接踵而至,期待将来这些研究能找出有效的疗效预测生物标志物和适宜人群,增强免疫治疗优势,为乳腺癌患者带来新的治疗曙光和希望。