疗效大不同 克唑替尼治疗ROS1重排或MET阳性NSCLC疗效比较
美国FDA已经批准了克唑替尼应用于ALK重排、ROS1重排以及MET 14外显子跳跃突变非小细胞肺癌(NSCLC)患者。目前已经有多项探索克唑替尼用于这类患者疗效的临床研究发表。近日,一项系统性分析克唑替尼疗效的荟萃分析研究发表于《靶向肿瘤学》(Targeted Oncology)杂志。该研究系统性筛选了克唑替尼单药治疗ROS1重排以及MET通路异常NSCLC患者的临床研究,并进行了荟萃分析。研究结果显示,克唑替尼用于ROS1重排NSCLC患者的疗效较为显著,疾病控制率(DCR)、客观缓解率(ORR)分别达到了93.2%、77.4%,中位无进展生存(PFS)和总生存时间(OS)分别为14.5个月、32.6个月。克唑替尼治疗MET通路异常NSCLC患者疗效较差,DCR、ORR仅为78.9%、40.6%,中位PFS和OS分别为5.2个月、12.7个月。

研究背景:
近年来,NSCLC的靶向药物研究进展迅速。作为NSCLC的驱动基因,MET、ROS1等少见突变也逐步成为NSCLC治疗靶点的研究重点。MET通路异常的形式较为多样,原发性MET扩增、MET 14外显子跳跃突变在NSCLC中的总体发生率约为3%;另外,在EGFR TKI治疗耐药的NSCLC患者中,MET扩增的发生率约为20%。MET剪切突变一般很少与MET扩增同时发生。ROS1基因融合则是另一类NSCLC的少见突变,在NSCLC中的总体发生率约为2%;ROS1基因融合能够引起下游通路的持续激活,从而导致癌症发生。
美国FDA于2011年批准了克唑替尼应用于ALK重排NSCLC,随后将其适应证扩展到了ROS1重排以及MET 14外显子跳跃突变NSCLC患者中。目前已经有多项探索克唑替尼用于ROS1融合或MET通路异常NSCLC的临床研究发表或者正在进行中。因此,该文章系统性筛选了相关的临床研究结果,并进行了荟萃分析。
研究方法:
研究者首先筛选了截至2020年5月之前在PubMed、Web of Science以及clinicaltrials.gov位点上发表的所有文献。检索关键词为crizotinib AND(ROS1 OR MET) AND(lung OR pulmonary OR NSCLC)。
其次,两位研究者分别孤立评估文献摘要进行二次筛选,保留报道了克唑替尼单药治疗ROS1融合或MET通路异常NSCLC患者疗效数据的临床研究。排除标准包括:(1)入组其他肺癌病理类型,比如唾液腺型肺癌等;(2)研究克唑替尼联合其他药物的疗效;(3)病例报道、文献综述;(4)会议报道、壁报展示、毕业论文或者出版书籍;(5)任何重复的研究。具体筛选流程如图1。
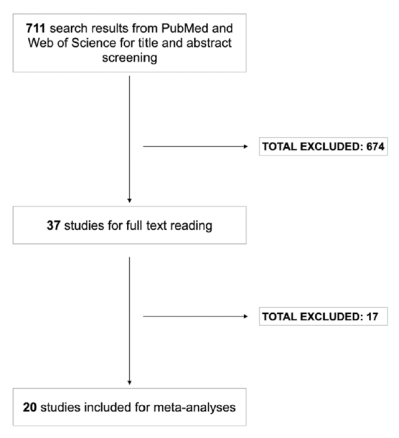
图1. 文献筛选流程
第三,研究者从入选的文献中逐个提取以下关键信息:(1)研究机构、城市、国家、研究发表年份、研究设计;(2)入组患者的年龄、性别、吸烟史、转移病灶部位、NSCLC病理亚型、ECOG PS评分、前线治疗、随访时间、治疗方案;(3)患者的最佳疗效[如完全缓解(CR)、部分缓解(PR)、疾病稳定(SD)以及疾病进展(PD)]、DCR、ORR、PFS、OS,以及不良事件(AE)。
随后,研究者采用了JAMOVI(www.jamovi.org)以及Comprehensive Meta-Analysis软件(Biostats Inc.,Englewood,NJ,USA)进行了荟萃分析。研究者分析了统计量I2,以评估不同研究之间的异质性。其中25%<I2≤50%视为异质性较低,50%<I2≤75%为中度异质性,I2>75则为高度异质性。P≤0.05为具有统计学意义。
研究结果:
1. 入组研究
研究者共筛选了711个检索结果,最终纳入了来自20个临床研究的719例NSCLC患者进行后续分析。这20个研究详见表1。在所有研究中,克唑替尼的初始治疗剂量均为250mg,每日两次。患者的疗效评估采用RECIST标准。
表1. 纳入分析的20个临床研究
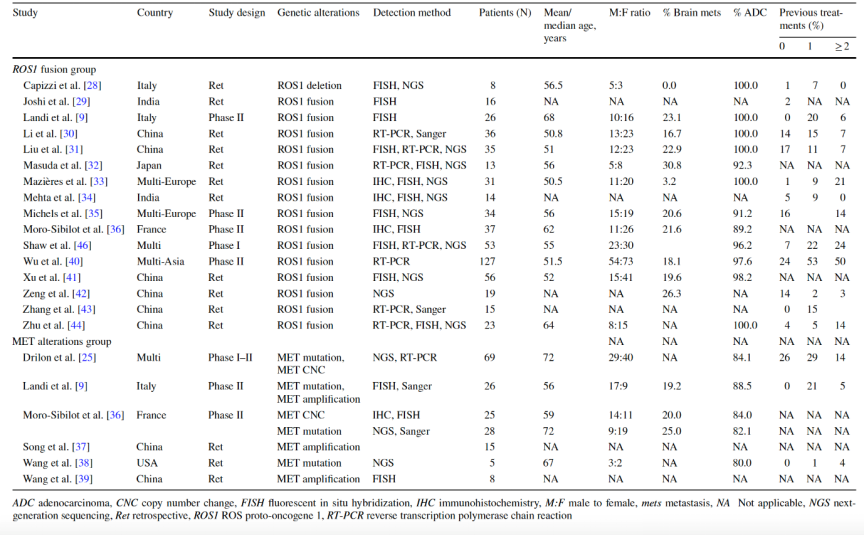
2. 克唑替尼应用于ROS1融合或缺失的NSCLC患者疗效
一共有16个研究报道了克唑替尼单药治疗ROS1融合或缺失NSCLC患者。总体而言,CR、PR、SD、PD的比例分别为4.2%(95% CI 1.9–6.4)、71.2%(95% CI 65.3–77.1)、13.4%(95% CI 9.7–17.0)以及5.8%(95% CI 3.8–7.8)。DCR达到93.2%(95% CI 90.8–95.5),ORR为77.4%(95%CI 72.8–82.1)。具体结果详见图2。不同研究之间的异质性显著(I2>25%)。
不同研究的中位PFS在5.5个月到22.8个月之间,荟萃后的中位PFS为14.5个月。大部分研究的中位OS尚未达到,在已经达到并发表了OS数据的研究中,中位OS为32.6个月。
其中有6个临床研究报道了CD-74阳性相对于CD-74阴性ROS1重排NSCLC的疗效,但是作者表示该结果在荟萃分析中并无统计学差异。
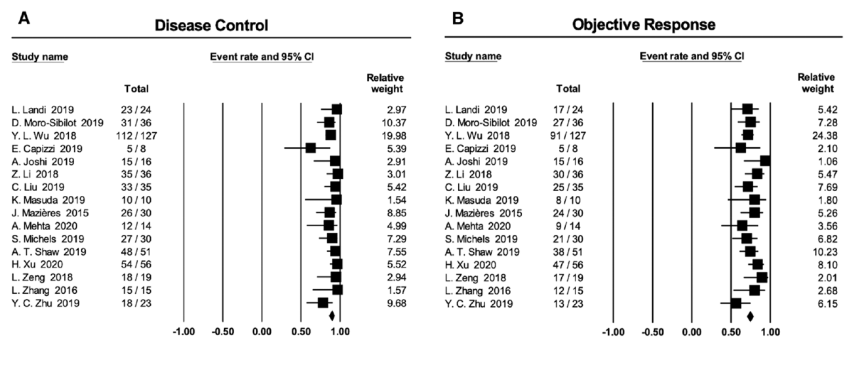
图2. 克唑替尼应用于ROS1融合或缺失NSCLC患者的DCR(A)和ORR(B)
3. 克唑替尼应用于MET通路异常NSCLC患者的疗效
一共有6个研究报道了克唑替尼单药治疗MET通路异常NSCLC患者的疗效。荟萃分析结果显示,CR、PR、SD、PD的比例分别为3.1%(95% CI 0.5–5.7)、39.3%(95% CI 25.8–52.7)、36.9%(95% CI 28.6–45.1)以及17.5%(95% CI 7.4–27.7)。
MET通路异常NSCLC患者的DCR以及ORR分别为78.9%(95% CI 70.3–87.4)、40.6%(95% CI 28.3–53.0),均低于ROS1重排NSCLC患者(具体结果详见图3)。不同研究之间的异质性也同样显著(I2>25%)。
6个研究均报道了PFS、OS数据。荟萃分析的中位PFS为5.2个月、中位OS为12.7个月。生存数据在MET扩增或MET突变NSCLC的亚组分析中并无差异。
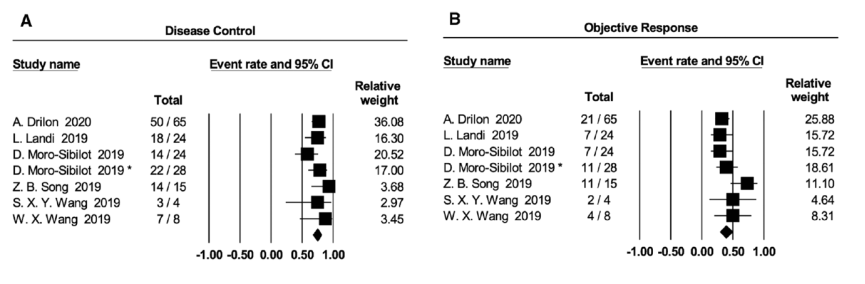
图3. 克唑替尼应用于MET通路异常NSCLC患者的DCR(A)和ORR(B)
4. 克唑替尼相关药物AE
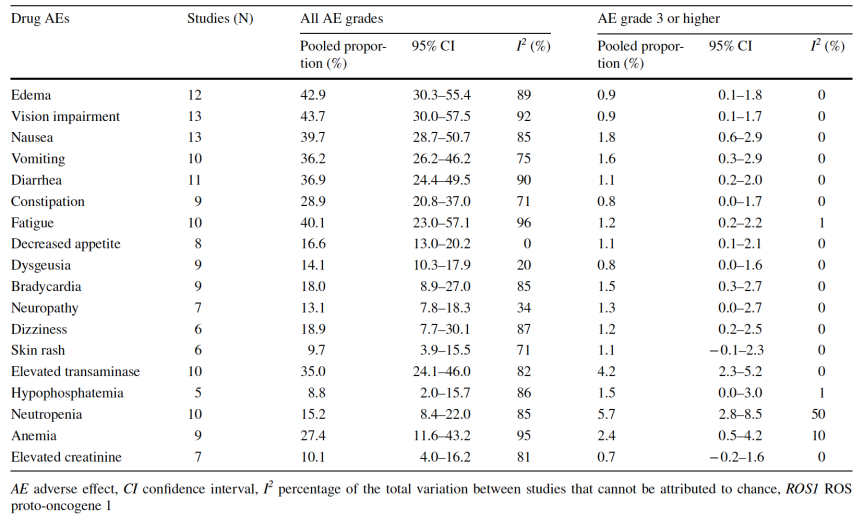
最常见的克唑替尼相关药物AE依次为视力受损(43.7%)、水肿(42.9%)、乏力(40.1%)以及常见的消化系统症状(比如恶心、呕吐、腹泻等)。发生频率最高的3级或3级以上AE为中性粒细胞减少症(5.7%)以及转氨酶升高(4.2%)。具体的克唑替尼相关AE谱详见表2。
表2. 克唑替尼相关AE谱
讨论&小结:
目前已有多项研究证实了克唑替尼治疗ALK、ROS1或MET异常型NSCLC患者的疗效。该荟萃分析首先证实了克唑替尼单药用于ROS1重排NSCLC患者的疗效,且不同的CD-74阳性或阴性亚组之间并无显著差异。克唑替尼治疗起效较快,一般在治疗2个疗程后即出现肿瘤的客观缓解,但是其获得性耐药的发生率却居高不下,约有50%的患者在研究随访期间出现疾病进展甚至死亡。ROS1重排也常常和其他肺癌驱动基因同时发生,比如合并EGFR突变、TP53突变或ALK重排,这类共存突变的肺癌患者的生存预后一般较差。关于克唑替尼耐药机制以及后线治疗的研究仍在探索中。
有研究显示,MET扩增或者MET突变肺癌患者对克唑替尼的应答率也有差异,根据既往报道,仅有MET扩增而无MET突变的肺癌是异质性较高的恶性肿瘤,更易合并NRAS、KRAS或TP53突变,其生物学行为与其共存的驱动基因突变有关。MET基因拷贝数较大的NSCLC,对MET抑制剂的应答率相对较高。
总而言之,该研究系统性筛选了克唑替尼单药治疗ROS1重排以及MET通路异常NSCLC患者的临床研究,并进行了荟萃分析。研究结果显示,克唑替尼用于ROS1重排NSCLC患者的疗效较为显著,但克唑替尼治疗MET通路异常NSCLC患者疗效差强人意,这也解释了为何克唑替尼除了ALK只获批了ROS1靶点,而MET靶点却迟迟未能获批的原因。值得注意的是,该荟萃分析纳入的临床研究之间存在显著的异质性,在数据解读的过程中仍需谨慎判断。
参考文献
1. Vuong HG, Nguyen TQ, Nguyen HC, et al. Efficacy and Safety of Crizotinib in the Treatment of Advanced Non-Small-Cell Lung Cancer with ROS1 Rearrangement or MET Alteration: A Systematic Review and Meta-Analysis [published online ahead of print, 2020 Aug 31]. Target Oncol. 2020;10.1007/s11523-020-00745-7. doi:10.1007/s11523-020-00745-7.
责任编辑:肿瘤资讯-MJ
排版编辑:肿瘤资讯-Shelley